

近日,重庆文理学院药学院宋桂廷副教授与屈川华教授团队在国际权威期刊《Organic Letters》上发表最新研究成果,发展了一种底物驱动、路径可切换的无金属级联环化策略,实现了3‑氨基吡咯与三氟甲基/氰基功能化1,2‑二氢吡嗪两类高价值氮杂环的发散式精准合成。本研究以N‑烷基烯胺为通用合成平台,通过精细调控底物电子与空间效应,在温和、无金属、敞口条件下,可控切换 [4+1] C‑插入与 [4+2] C‑N插入环化路径,突破传统烯胺固有反应选择性,实现从同一底物出发定向构筑五元/六元氮杂环。反应无需光催化剂、路易斯酸与过渡金属助剂,具有条件绿色、选择性优异、官能团耐受性广、克级制备可行等突出优势。所构建的 3‑氨基吡咯骨架广泛应用于抗菌、抗炎及抗肿瘤活性分子;而含 CF₃/CN 的 1,2‑二氢吡嗪可作为新型双齿配体应用于过渡金属催化,展现出优异的配位性能与合成潜力。机理研究表明,反应历经亚胺阳离子关键中间体,TEMPO⁺BF₄⁻兼具氧化剂与离去基团双重功能,为反应选择性调控提供了理论支撑。该工作提出的可切换、模块化、无金属杂环合成新范式,为复杂氮杂环分子的高效构建、药物分子快速衍生化及新型催化配体开发提供了强有力的合成工具。本文带您拆解其机理精妙之处与药物化学潜力。
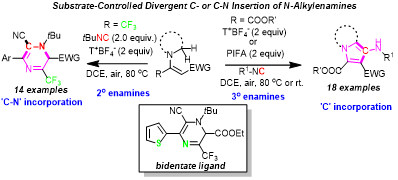
一、策略创新:“C-插入”与“C-N-插入”的选择性调控策略
在药物化学家的眼中,氮杂环骨架堪称“明星结构”——它是现代药物、催化材料、功能分子的核心基元,其高效、可控、模块化的构建,长期以来都是合成化学领域的前沿难题,更是制约新药研发与材料创新的关键卡点。
关于烯胺的转化反应,学术界早已多有报道,但长期存在一个“认知盲区”:烯胺的氮插入反应已被广泛研究,而碳插入反应却鲜有突破,始终难以实现高效构建。
此前,作者团队已在该领域取得阶段性进展:利用N-亚烷基烯胺,通过溴自由基介导的协同活化策略,成功实现了高官能化吡咯的合成(Org. Lett. 2025, 27, 11264)。但即便如此,一个核心难题仍未解决——如何实现烯胺骨架上选择性的碳插入或碳-氮插入,始终没有可行的策略。
基于课题组前期的扎实研究基础,作者团队终于取得了突破性进展:首次采用烯胺的异腈插入策略,仅通过调控烯胺的电子效应和空间位阻,就实现了发散性环化反应(见图1:“C-插入”与“C-N-插入”的选择性调控策略),彻底打破了此前的合成瓶颈。
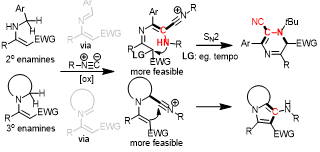
图1:“C-插入”与“C-N-插入”的选择性调控策略
这一策略的精妙之处,在于“底物决定反应走向”:二级烯胺更倾向于发生[4+2]碳-氮插入反应,而三级烯胺则会发生[4+1]碳插入反应——背后的核心驱动力,是不同过渡态的电荷稳定作用。
更值得关注的是,该反应还具备两大显著优势,极具应用价值:
✅反应条件温和:无需金属催化剂,在开放 flask 条件下即可顺利进行,大幅降低了反应成本与操作难度;
✅产物价值高:可高效制备具有药用价值的3-氨基吡咯,或三氟甲基/氰基取代的1,2-二氢吡嗪,产物收率从良好到优异,为新药研发提供了高效的合成路径。
这项工作的意义远不止于此——它是烯胺基杂环构建中,罕见的“底物控制型发散合成”案例,充分证明了:无需导向基团,无需过渡金属,仅通过分子结构设计,就能精准调控反应结果。
这一突破不仅填补了烯胺碳插入反应的研究空白,更为氮杂环骨架的高效、可控构建提供了全新思路,有望推动药物化学、催化科学与功能材料领域的进一步发展,为相关领域的创新研究注入新动力。
二、研究成果:
基于课题组在杂环合成领域长期的研究积累与技术专长,我们以烯胺1a与叔丁基异腈2a为模型体系,系统优化氧化环化反应条件,目标是构建3-氨基吡咯3(结构经单晶X射线衍射确认,CCDC:2536165)。最终,我们筛选出两种最优的开放烧瓶反应条件(均为无金属体系):
✅方法A:以PIFA为氧化剂,反应温度80℃;
✅方法B:以T+BF4⁻为氧化剂,室温下即可反应。
确定最优条件后,我们重点研究了该无金属氧化环化反应的底物适用范围(图2-4),具体分为以下几部分:
一、环状(三级)烯胺的底物适用性(图3)
1. 四氢异喹啉衍生的烯胺反应顺利,可生成二氢异喹啉并3-氨基吡咯;多数底物可同时适配方法A和方法B。
2. 乙酯/甲酯取代的烯胺,用方法A可获得高产率的产物3和4,但用方法B仅能获得中等产率的产物4。
3. 异吲哚啉衍生的烯胺,方法A可获得良好产率的稠环杂环5,而方法B产率仅为34%。
4. 两种方法均能兼容杂芳环衍生的烯胺,可制备三环/四环杂环6和7。
5. 四氢异喹啉苯环上的取代基(甲基、甲氧基、氯、溴)在方法A下耐受性良好,产物8-14产率中等至良好;而方法B适用性较窄,对空间位阻较大的底物(10-11)无法反应。
6. 其他类型烯胺(单酯取代、二级、环烷基胺衍生)均无反应活性,存在一定底物局限性;由于异腈反应活性高,含N-H键的二级烯胺通常无法兼容。
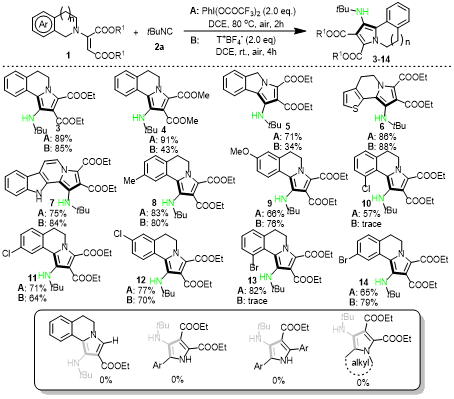
图2:3o烯胺底物范围
二、三氟甲基和酯基官能化二级烯胺的反应活性(图4)
经过大量筛选,我们发现同时含三氟甲基和酯基的二级烯胺具有独特反应活性:在二氯乙烷中,以T+BF4⁻为氧化剂、80℃条件下,多种三氟甲基类二级烯胺1'可与叔丁基异腈2a顺利发生氧化环化反应。
反应可高效生成多种含三氟甲基和氰基(均为高价值官能团)的1,2-二氢吡嗪15-28,产率良好至优异,具体特点如下:
1. 苯环上带有中性或给电子取代基的底物耐受性良好,可生成产物15-25(产物16的结构经单晶X射线衍射确认);
2. 给电子取代基取代的苯环连接吸电子核心时,反应可顺利进行,产物26产率中等;
3. 反应兼容呋喃、噻吩等杂芳环体系,生成的产物27-28具有潜在药用和合成价值;
4. 该方法不适用于缺电子苄胺衍生的二级烯胺,推测是吸电子取代基提高了氧化能垒。
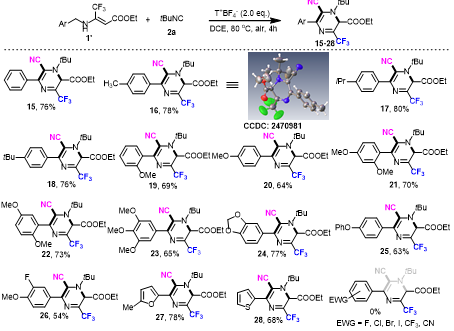
图3:2o烯胺底物范围
三、异腈的底物适用范围(图5)
我们进一步研究了环状烯胺在两种方法下的异腈适用范围,发现异腈适用范围相对较窄,且方法A的反应条件更苛刻,易在产物氨基部分引入三氟乙酰基:
1. 方法A下,异丙基异腈等二级异腈可顺利生成含三氟乙酰基的产物29;
2. 方法A下,空间位阻较大的三级异腈(如1,1,3,3-四甲基丁基异腈)会发生烷基链断裂并伴随三氟乙酰化,生成3-氨基吡咯30,这一已知反应特性有望用于制备游离氨基官能化的3-氨基吡咯衍生物;
3. 方法B下,烷基链可保持完整,生成产物31;
4. 一级异腈、苄基异腈、环戊基异腈在两种方法下均无反应活性;
5. 意外发现:方法B下,富电子芳基异腈(如对甲氧基苯基异腈)展现出新颖反应路径——与烯胺1a反应生成复杂的双杂环产物32,但与四氢咔啉衍生烯胺1e、富电子苄胺衍生烯胺1g反应时,可正常生成产物33-34。

图4:异腈底物范围
四、克级示范与后续衍生
为了验证该合成方法的实用性,我们首先开展了克级规模反应(图5),结果十分理想:在方法B条件下,4.0 mmol的烯胺1a与叔丁基异腈2a反应,以76%的产率得到3-氨基吡咯3;同理,4 mmol的二级烯胺1'n反应后,以69%的产率生成1,2-二氢吡嗪28。这一结果充分证明,我们的方法具备良好的可放大性和实际合成价值。
随后,我们进一步展示了产物的合成多功能性,具体有两大应用方向:
1. 作为合成砌块,实现高效转化
在四氢呋喃(THF)中,用氢化铝锂(LAH)在室温下处理产物3(反应2小时),可将酯基还原为伯醇35,产率高达98%——这充分体现了产物作为合成砌块的实用价值,为后续复杂分子合成提供了便捷路径。
2. 作为配体,应用于过渡金属催化反应
我们将1,2-二氢吡嗪28作为配体,应用于铜催化的环化反应中:
无配体时,苄胺36与丁炔二酸二甲酯37、2-溴-2-甲基丙酸乙酯38的偶联反应完全无法进行;而加入28作为配体后,成功以48%的产率得到产物39。
这一产率与基准配体2,2'-联吡啶(60%产率)相当,充分彰显了1,2-二氢吡嗪类化合物作为新型双齿配体,在过渡金属催化领域的巨大应用潜力。
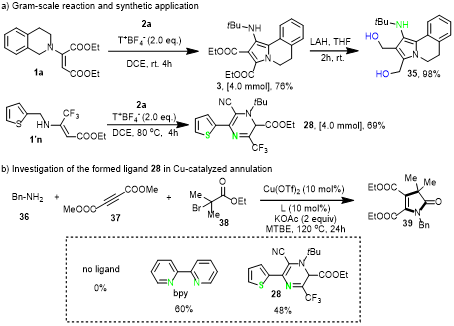
图5:克级示范与后续衍生
五、反应机理解析(以二级烯胺1'a为模型底物,图6)
结合机理研究及关键中间体的鉴定,作者提出了1,2-二氢吡嗪的形成路径,核心步骤简洁明了,具体如下:
1. 氧化引发:氧铵盐T+BF4⁻氧化二级烯胺1'a,将N=O基团插入苄基C-H键,生成α-氨基烷基羟胺中间体I;
2. 关键中间体生成:中间体I经去质子化、消除TEMPOH,得到关键亚胺中间体III;
3. 加成与异构化:两当量叔丁基异腈2a依次加成到中间体III上,生成双加合物V,随后经双键异构化形成中间体VI;
4. 氧化与环化:中间体VI消除异丁烯得到中间体VII,再经第二当量T+BF4⁻氧化,生成TEMPO加合物VIII(此处TEMPO相当于卤化物,可作为离去基团);
5. 产物生成:中间体VIII发生分子内SN2型环化反应,最终得到目标产物1,2-二氢吡嗪15。

图6:反应机理
总结展望
综综上,作者开发了一种通用、无金属的氧化环化方法,以易获取的烯胺和异腈为原料,实现了两类高价值杂环化合物的发散性合成。通过选用PIFA和T+BF4⁻两种互补氧化剂,可在温和条件下实现选择性合成:由三级烯胺制备3-氨基吡咯,由二级烯胺制备1,2-二氢吡嗪。该方法具有底物范围广、官能团耐受性好、可放大的优势;产物的实用性也得到充分验证——既能实现高效衍生化,也可作为双齿配体应用于铜催化环化反应。机理研究表明,T+BF4⁻兼具氧化剂和反应伙伴的双重作用,而TEMPO在最终环化步骤中可作为有效的离去基团。这项工作为复杂含氮杂环的构建提供了实用、模块化的新策略,在药物化学和催化领域具有广阔的应用前景。
文献详情
Switchable C or C−N Insertion into NAlkyl Enamines for Divergent 2 Synthesis of 3Aminopyrroles or CF3/CN-1,2-Dihydropyrazines
Gui-Ting Song,* Su-Ya Liu, Lin Zhu, Ying Cheng, Shi-You Xue, Rui-Xue Luo, and Chuan-Hua Qu*Org. Lett.2026, 28, DOI: 10.1021/acs.orglett.6c01107
https://doi.org/10.1021/acs.orglett.6c01107
作者简介

刘苏亚,重庆文理学院药学院制药工程2023级本科生,以第二作者在《Organic Letters》发表论文二篇,荣获国家励志奖学金、校特等奖学金及三好学生等荣誉。

朱琳,重庆文理学院药学院药学2023级本科生,2024年10月9日为实验助理,在Org. Lett.,Green Synth. Catal.,Adv. Synth. Catal. 等国际学术期刊发表论文4篇。

程莹,重庆文理学院药学院制药工程2023级本科生,曾获“东富龙-国家工程杯”第十二届全国大学生制药工程设计竞赛国家二等奖、重庆市第十四届“挑战杯”市级银奖;在《Organic Letters》发表论文二篇。

薛世友,重庆文理学院药学院制药工程2023级本科生,在《Organic Letters》发表论文二篇。

罗瑞雪,重庆文理学院药学院药学2022级本科生,在《Organic Letters》发表论文一篇。
屈川华,重庆文理学院药学院教授,硕士生导师。2011年本科毕业于四川大学华西药学院;2014年硕士毕业于四川大学华西药学院药物化学系;2017年博士毕业于南京大学化学化工学院有机化学系;2018-2021在武汉大学进行博士后研究,2018年11月加入重庆文理学院。研究兴趣为自由基参与的绿色有机合成,在国际学术期刊发表论文20余篇,授权中国发明专利3项。
宋桂廷,重庆文理学院药学院副教授,硕士生导师。2013年本科毕业于重庆师范大学化学院;2018年博士毕业于中国科学院大学有机化学系;2018-2020在重庆文理学院进行博士后研究,2020年10月加入重庆文理学院。研究方向为多组分反应、杂环合成、可见光催化,在国际学术期刊发表30余篇科研论文,其中中科院一区11篇,获得重庆市巴渝青年学者,国家自然科学青年基金等资助,长期担任Org. Lett.、J. Org. Chem.审稿人。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn