

正文
过渡金属催化的不对称氢化因其高效、易于工业化的优点,被广泛应用于手性化合物合成。近几十年来,铑、钌、铱、钯等稀有金属催化剂取得了显著成果。然而,这些金属储量有限、价格昂贵、毒性较大,严重限制了其在工业生产中的广泛应用。
针对这些挑战,近期研究重点转向利用地球储量丰富的丰产金属(如铁、钴、镍、铜)作为经济、易得且低毒的替代催化剂。尽管取得了显著进展,但与稀有金属体系相比,这些催化剂的活性普遍较低,且尚未实现工业化应用。因此,提升其催化效率成为亟待解决的核心问题。上海交通大学张万斌教授团队近年来一直致力于在丰产金属催化不对称氢化反应的研究,发现反应中存在催化剂与底物之间弱吸引相互作用的协同催化效应,据此成功开发了一系列高效的金属催化不对称氢化(Pd: Angew. Chem. Int. Ed.2013, 52, 11632; Angew. Chem. Int. Ed.2016, 55, 8444; Nat. Commun.2018, 9, 5000; Rh: Angew. Chem. Int. Ed.2019, 58, 11505;J. Am. Chem. Soc.2024, 146, 25312; Ru: J. Am. Chem. Soc. 2024, 146, 25312; Ni: Angew. Chem. Int. Ed.2019, 58, 7329; Angew. Chem. Int. Ed.2020, 59, 5371; Nat. Commun.2020, 11, 5935; Nat. Chem.2022, 14, 920;Angew. Chem. Int. Ed.2023, 62, e202214990;Nat. Commun.2024, 15, 5482;J. Am. Chem. Soc.2025, 147, 342; Co: Angew.Chem. Int. Ed.2019, 58, 15767; Cu: Angew. Chem. Int. Ed.2023, 62, e202306380; Angew. Chem. Int. Ed.2024, e202416313),通过精确调控底物与催化剂间的弱非共价相互作用,特别是CH/π···HC/π和CH···O/N相互作用来优化催化反应过程。如在手性配体中引入叔丁基(tBu)基团,成功稳定了过渡态,显著提升了地球丰产金属催化不对称氢化的反应活性,该方法有效利用了多重吸引色散作用(MADI)。
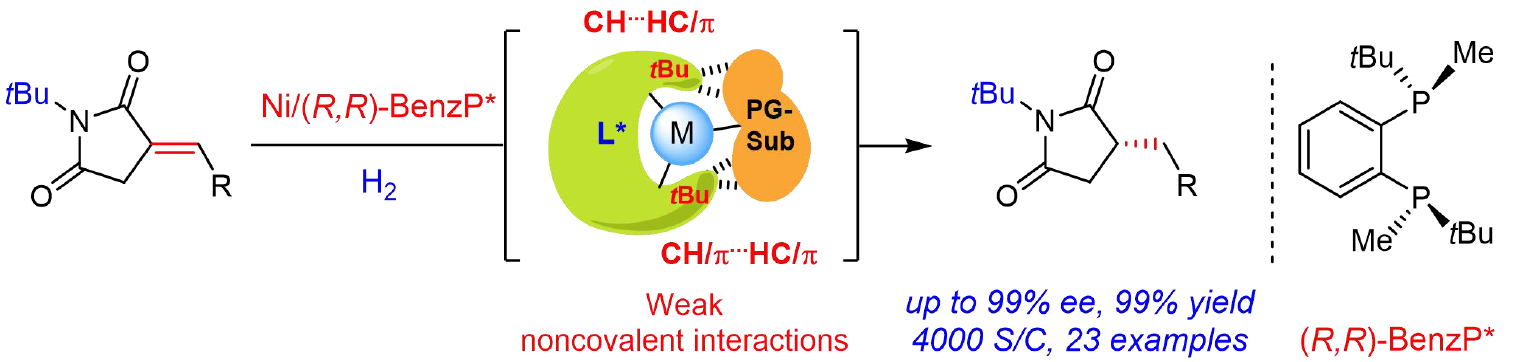
在底物中选择性引入保护基团是很多催化转化中的一种有效的常用策略,既可精准调控化学选择性,又能大幅提升催化效率。近日,该团队成功开发出一种调控底物保护基策略,实现了环外α-亚烷基琥珀酰亚胺的不对称氢化反应。通过密度泛函理论(DFT)计算结合动力学实验,系统探究了保护基对催化性能的影响机制。结果表明,保护基与催化剂之间的弱非共价相互作用在催化活性中发挥关键作用,且二者呈现出正相关。特别是在使用tBu作为保护基时,催化体系展现出优异的活性与对映选择性,表现出显著的优势。该研究不仅为理解非共价相互作用在不对称催化中的作用机制提供了新的视角,也凸显了该策略在推动绿色可持续催化向工业化转化方面的潜在潜力(图1)。
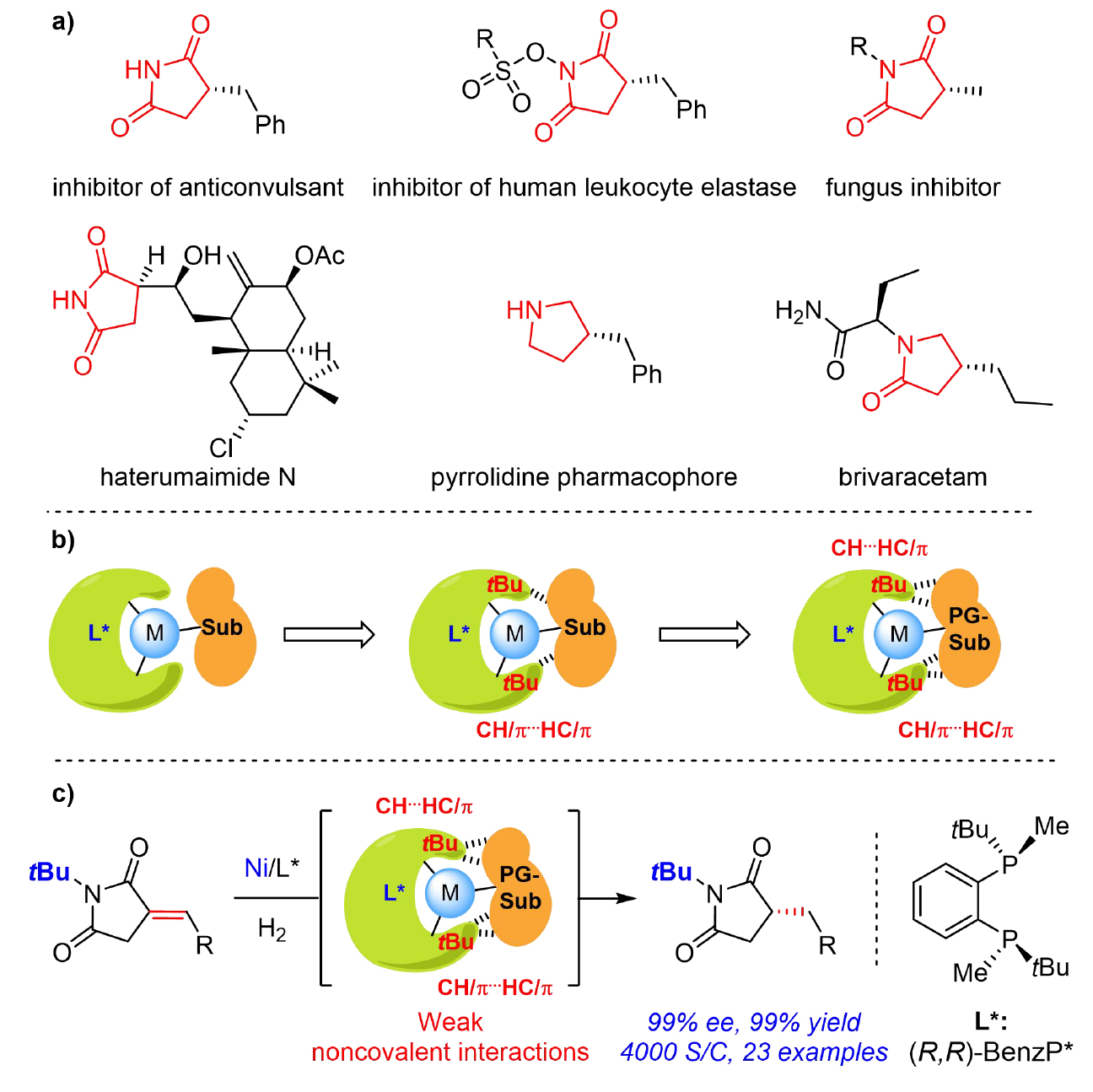
图1 手性琥珀酰亚胺衍生物及其合成方法
为研究催化剂-底物弱非共价相互作用与催化活性的关联性,作者选用了带有远端N-保护基的α-亚烷基琥珀酰亚胺类底物。这些保护基远离不饱和双键位置,可最大程度降低其对映选择性的影响。在进行密度泛函理论(DFT)计算之前,作者首先评估了氢化反应的可行性,并确定了关键过渡态结构。
在确定了最优反应条件后,作者进一步探究反应机理与决速步骤,以明确DFT计算所需的关键过渡态(图2)。首先,通过氘代标记实验确定了α-亚烷基琥珀酰亚胺还原的两个氢全部来源于氢气。反应级数实验进一步证实反应对氢气压力呈一级关系,对底物浓度呈零级关系。综合实验结果推测可能的反应机理:第一步是Ni-H复合物的负氢对α碳的直接加成(无需H2直接参与),而后续直接依赖氢气压力的氢解步骤被确认为反应的决速步。
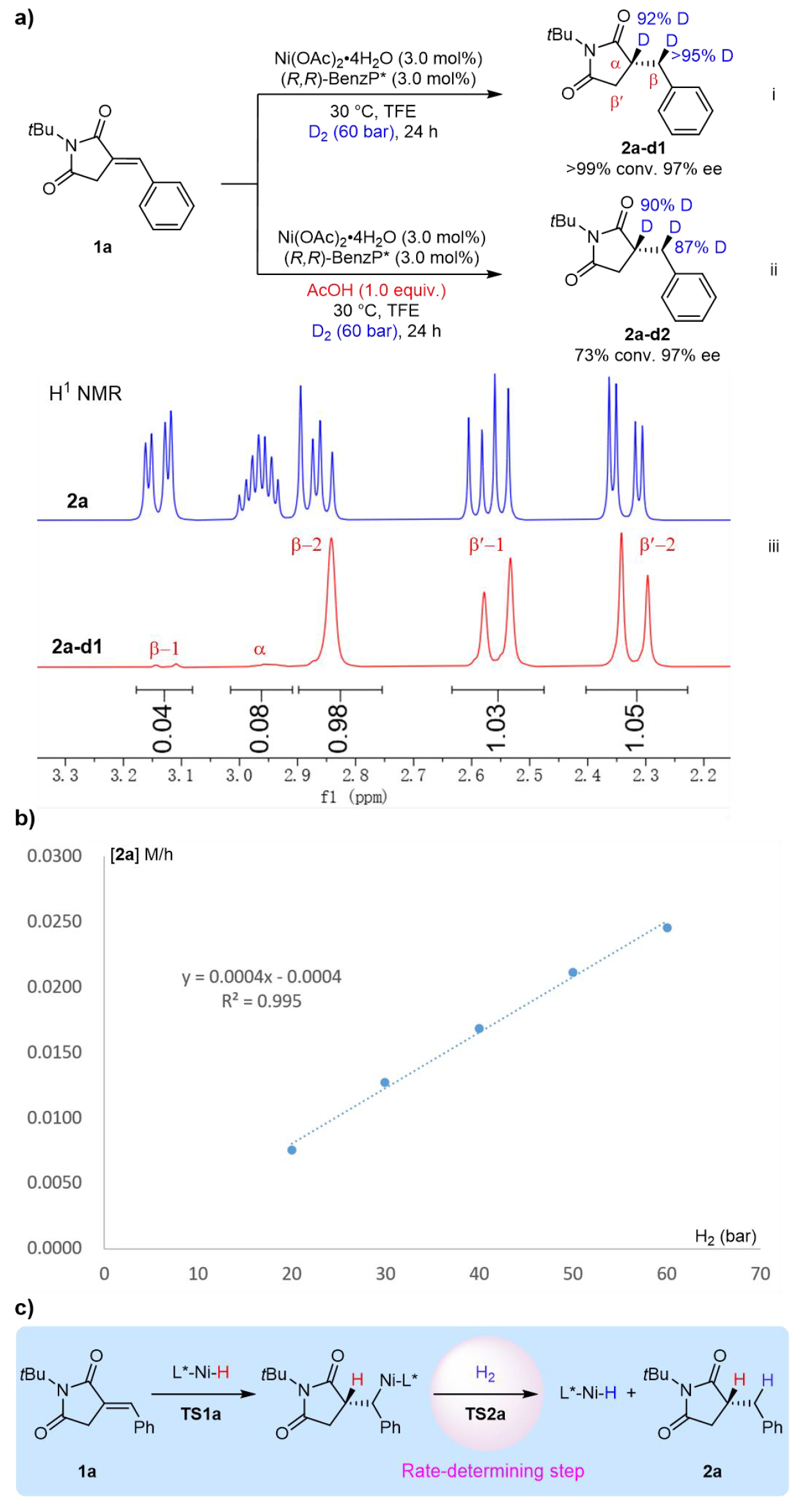
图2机理实验
在最优反应条件和反应机理研究的基础上,作者系统性地研究了N-保护基对催化剂-底物间弱非共价相互作用的影响(图3)。作者采用DFT计算(过渡态 TS2a 和TS2a1–4(R))和动力学实验,分析了带有支链(N-tBu、N-iPr)、直链(N-nPr、N-Et)以及小体积(N-Me)保护基的底物。结果显示,引入更大支链的N-tBu保护基使相互作用能显著增加2.0 kcal/mol,反应转化率也提升至13.2%/h。这一趋势与DFT计算所得的催化剂-底物间非共价相互作用能的变化一致。这些结果明确建立了相互作用强度与催化效率之间的正相关关系。此外,作者通过控制实验排除了另一种可能性:即催化活性的提升源于大位阻保护基在底物或产物强极性官能团附近产生的空间位阻效应,该效应抑制了竞争性配位。
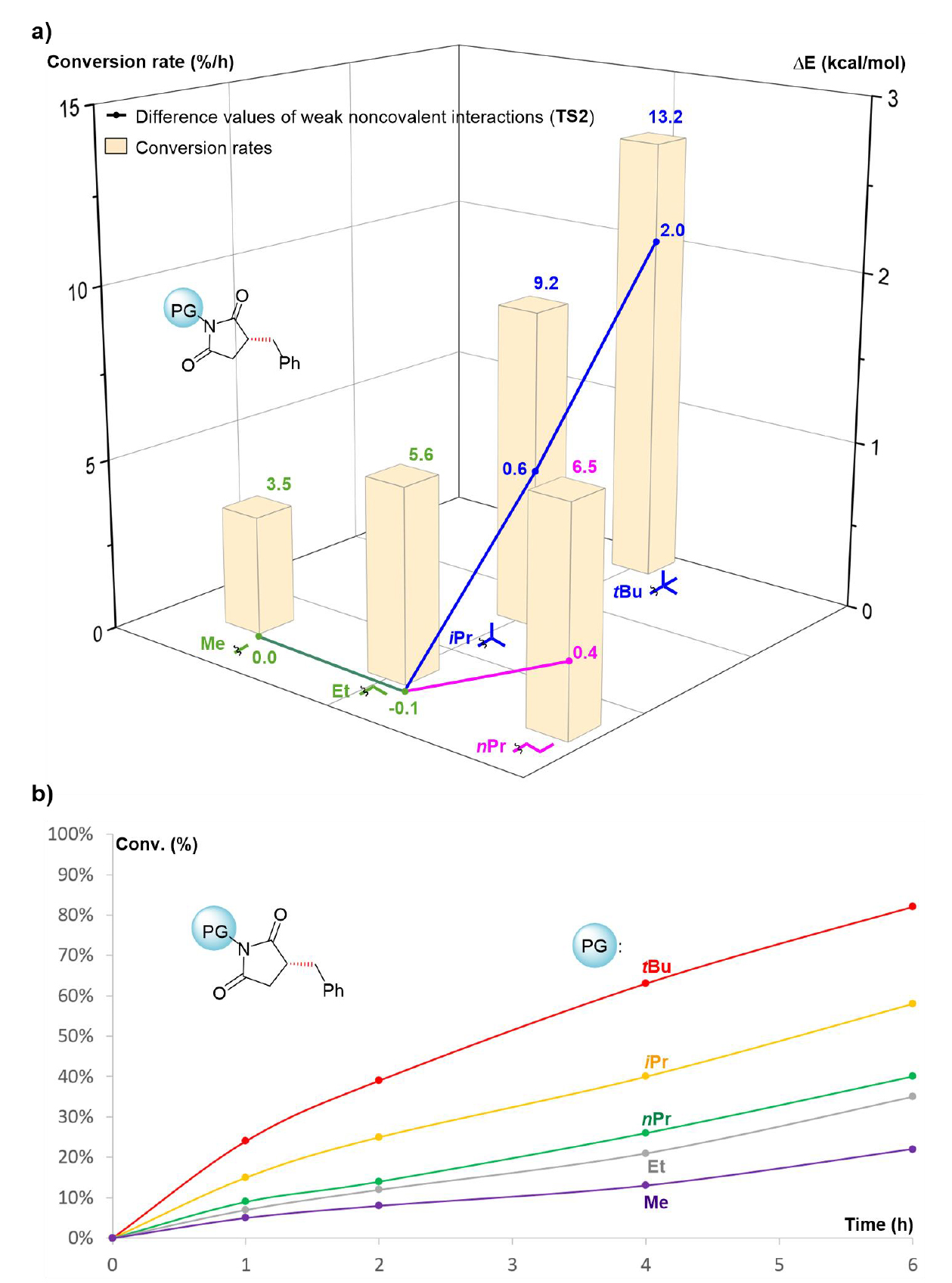
图3N-保护基效应的反应机理与动力学分析
进一步地,过渡态TS2a(R) (tBu) 与 TS2a4(R) (Me) 的结构分析揭示了丰富的弱非共价相互作用(图4)。这一发现证实了 N-tBu 体系中存在更广泛的弱非共价相互作用网络,与其增强的反应活性相符。进一步的能量分解分析 (EDA) 定量表明,TS2a(R) (tBu) 中的弱非共价相互作用比 TS2a4(R) (Me) 强 2.0 kcal/mol(−42.6 vs. −40.6 kcal/mol),显著突出了弱非共价相互作用对催化活性的关键调控作用。
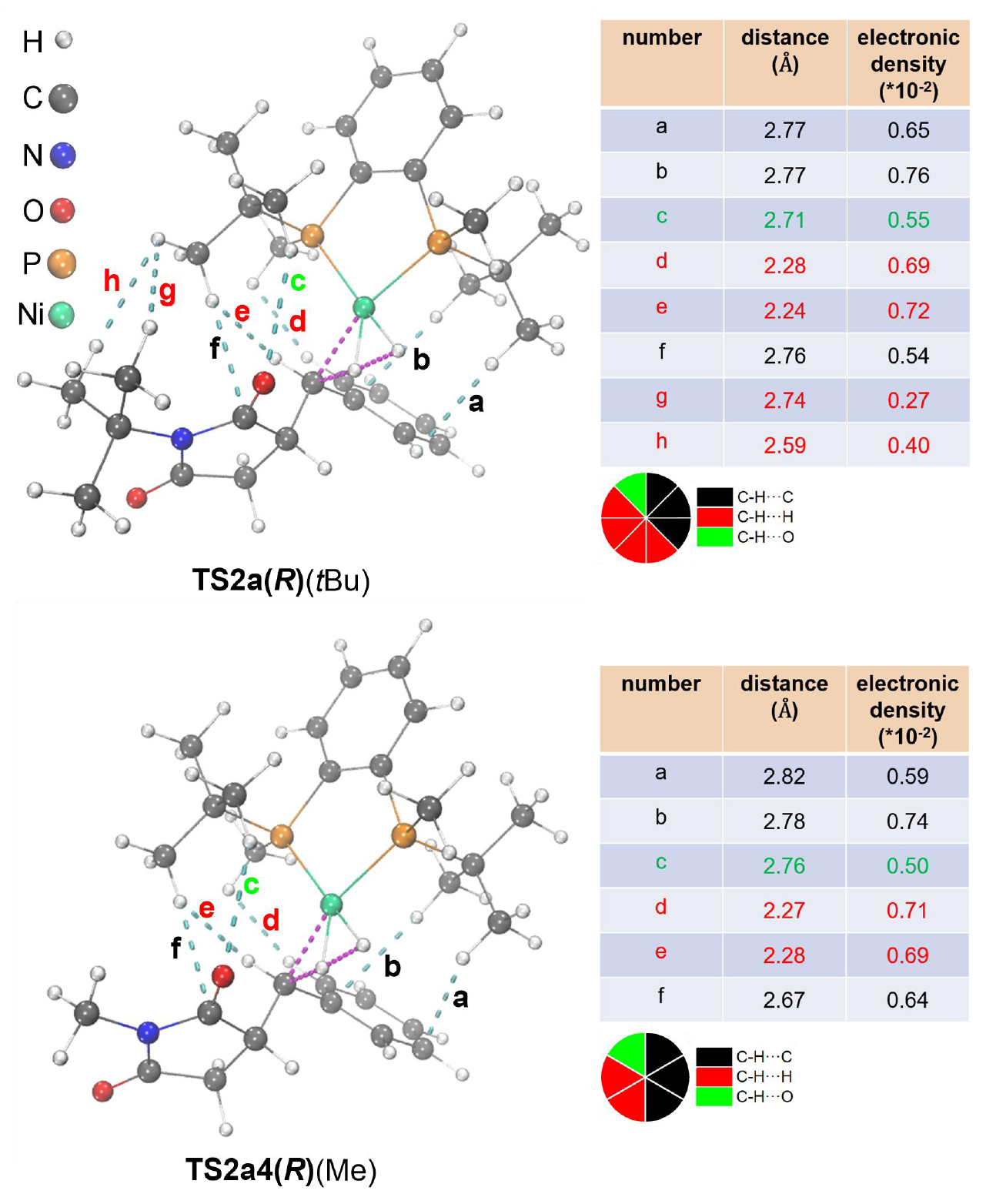
图4TS2a(R) (tBu) 和TS2a4(R) (Me)的结构
在优化反应条件的基础上,作者考察了该催化体系的底物适用范围(图5)。一系列N-tBu保护的底物被高效转化为相应的手性琥珀酰亚胺产物,具有优异的对映选择性(94–99% ee)和高产率(最高达99%)。其中,2-萘基底物(1t)表现出最高的对映选择性(99% ee)。此外,烷基取代的底物(1u–w)也顺利发生加氢反应,得到产物2u–w,产率为94–99%,对映选择性为95–98% ee。
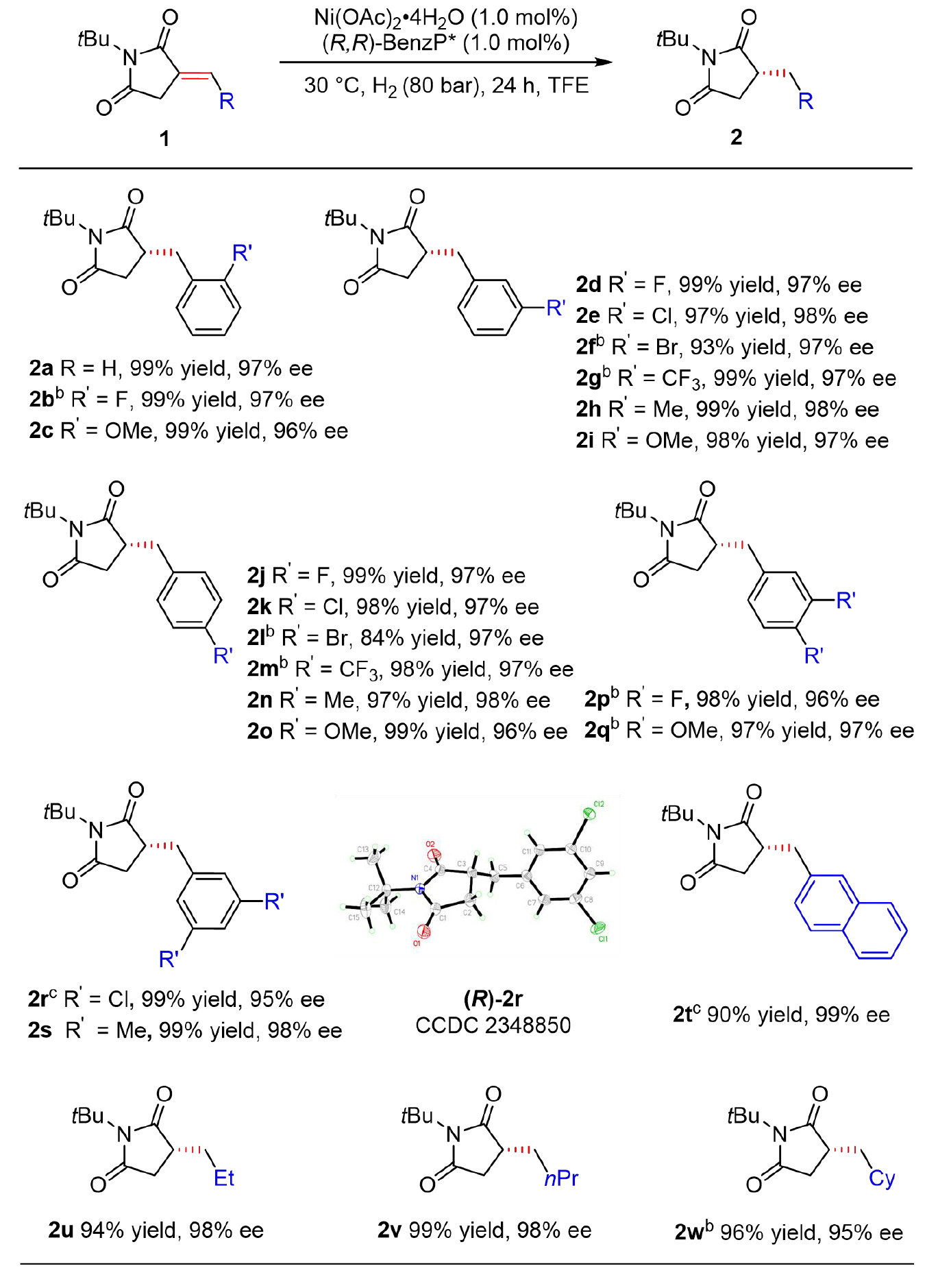
图5底物范围
为了进一步评估该反应的实用性,作者在克级规模上以底物/催化剂比例(S/C = 4000)进行了催化氢化(图6a)。使用过量的 Ni(OAc)2·4H2O,模版底物1a 以 97% 的收率和 95% ee 转化为 2a,其催化效率超越了在类似转化中使用的稀有金属体系(S/C ≤ 2000)。随后,作者探究了手性琥珀酰亚胺的各种应用与转化。包括手性抗惊厥抑制剂3(收率99%,94% ee),抗病毒药物2x(收率98%,94% ee),手性抗惊厥抑制剂4(收率 80%,98% ee),人白细胞弹性蛋白酶抑制剂6(收率 87%,90% ee),手性 3-苄基吡咯烷 8(收率71%,94% ee), RIPK1 抑制剂 11(收率 67%,>99% ee)等(图6b-c)。
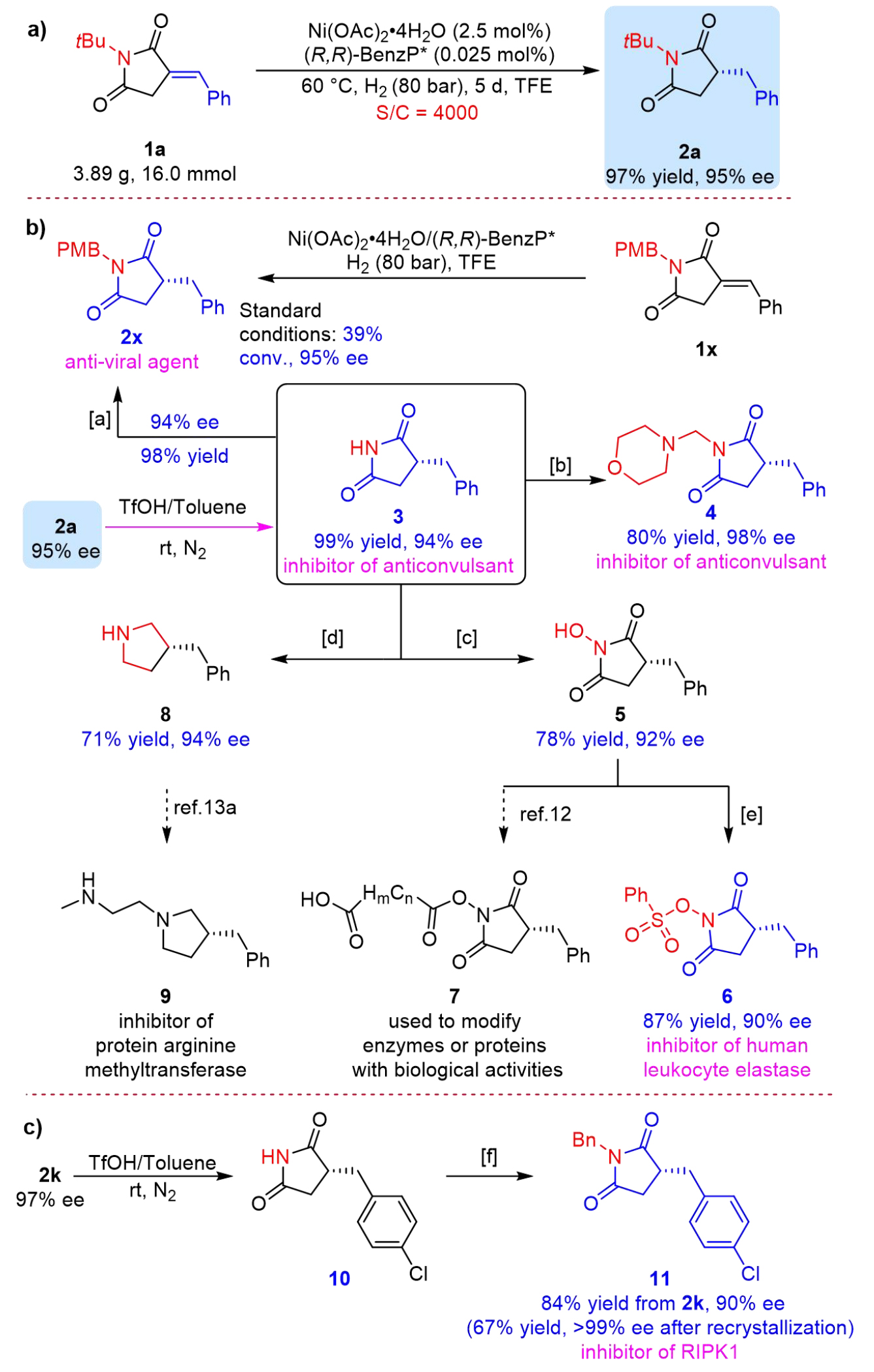
图6克级规模反应及产物的衍生应用研究
为了探究该镍催化不对称氢化反应的催化循环机理,作者进行的DFT计算(图7)。该催化循环始于中性镍氢二膦配合物I与底物1a 的配位,形成中间体II。随后发生负氢迁移,该过程经历两个竞争性的过渡态TS1a(S) 和TS1a(R),形成中间体III。接着,氢气配位到III 上生成物种IV,IV 通过速率决定步骤和对映选择性决定步骤的过渡态TS2a 释放产物2a,并再生出活性催化剂I。计算得出的R- 和S- 路径之间的ΔΔG‡ 值为 -2.7 kcal/mol,对应 98% ee 的对映选择性,这与实验结果 97% ee 高度吻合。该分析突显了过渡态 TS2a(R) 在决定对映选择性中的关键作用。
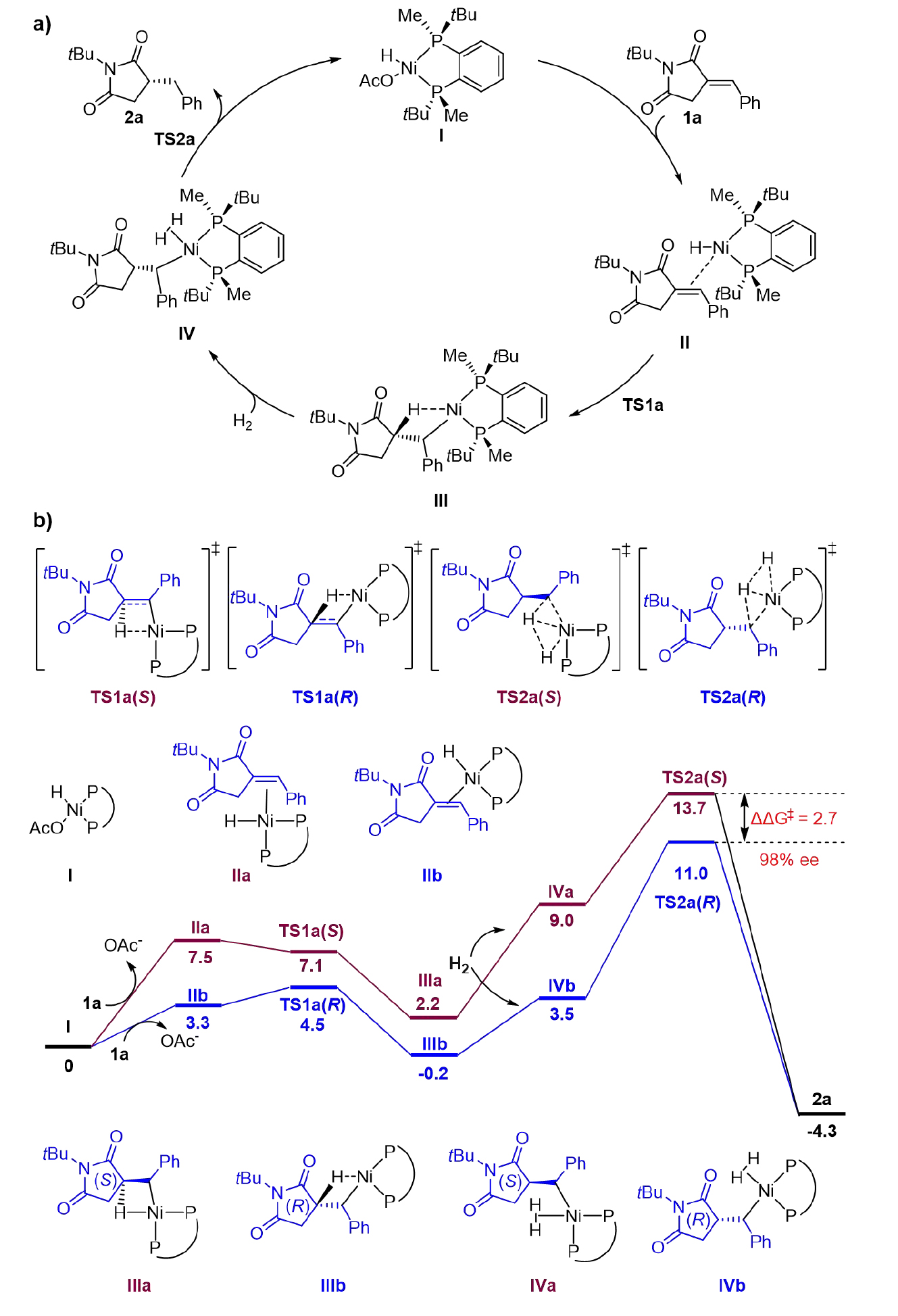
图7可能的机理及关键过渡态的DFT计算
对TS2a(R)和TS2a(S)进行的能量分解分析(EDA)表明,其对映选择性来源于不同的关键因素(图8)。虽然强相互作用能之和(EEle、EEx和 EOrb)以及变形能之和(EDist(cat)和 EDist(sub))有利于S-产物的形成,差值达 2.1 kcal/mol(TS2a(R)为 -207.7 kcal/mol vs. TS2a(S)为 -209.8 kcal/mol),但 TS2a(R)中更强的弱非共价相互作用(TS2a(R)为 -42.6 kcal/mol vs. TS2a(S)为 -39.0 kcal/mol)将总相互作用能差异缩小至 -1.5 kcal/mol。这一转变最终有利于 R-产物的形成。
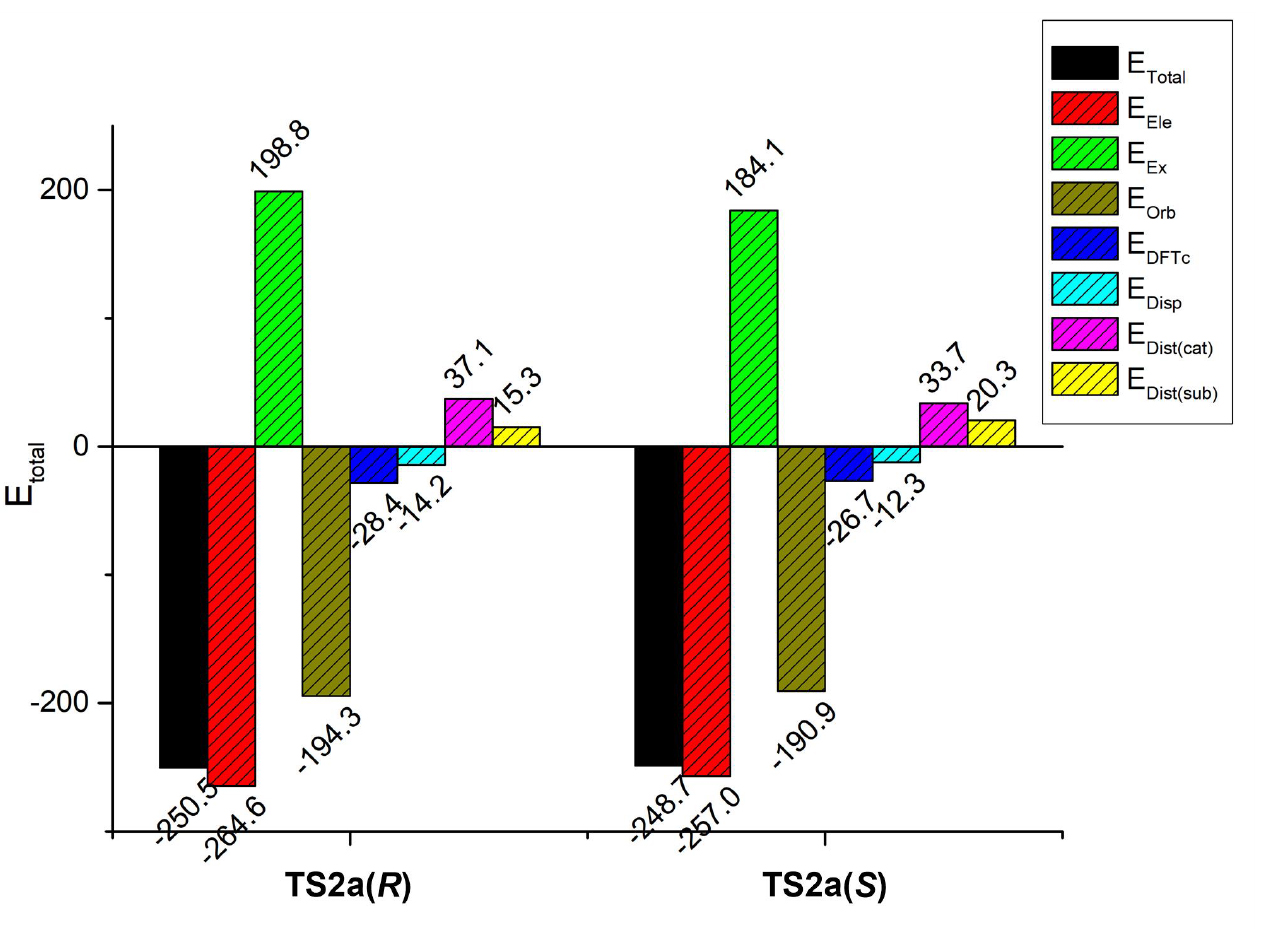
图8TS2a(R)和TS2a(S)的EDA分析
总结
综上所述,本研究突显了增强α-亚烷基琥珀酰亚胺类底物与镍催化剂之间弱非共价相互作用在催化反应中所起的重要作用。通过在底物中引入大位阻的N-保护基团,催化活性得到显著提升(S/C = 4000)。DFT计算与动力学实验证实,这些弱非共价相互作用的强度与催化效率呈相关。机理研究进一步阐明该催化循环经历α-氢加成与速率决定步骤β-氢解离的分步过程,而R-构型过渡态中增强的弱非共价相互作用为高的对映选择性提供了合理解释,也为催化剂性能表现建立了理论依据。
该成果近期发表于Angew. Chem. Int. Ed.上,上海交通大学化学化工学院博士生蔡新红为该论文的第一作者,博士生罗亦聪提供了理论计算支持,上海交通大学张万斌教授、陈建中副研究员为该论文的通讯作者。
导师介绍
张万斌,上海交通大学讲席教授,国家重点研发计划项目负责人。张万斌教授长期从事不对称催化和药物及其关键中间体的高效合成方法研究。主持国家重点研发计划项目、国家重大新药创制专项、国家自然科学基金委重大、重点及面上项目以及上海市科委、教委和经信委重大和重点科研项目等。相关研究成果已发表包括Science、Nat. Chem.、CCS Chem.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.和Nat. Commun.在内的SCI论文300余篇,获得授权发明专利50余项。在此基础上实现了贝达喹啉、青蒿素、瑞德西韦、布立西坦、薄荷醇、香芹酮和系列檀香等手性药物和香料工业化合成的关键技术突破,多项成果获得工业化应用。入选宝钢优秀教师特等奖、国家“万人计划”教学名师、中国化学会会士,上海领军人才和上海市优秀学术带头人。曾获国家自然科学二等奖,上海市自然科学奖一等奖、中国产学研合作创新成果奖一等奖和上海市产学研合作优秀项目奖特等奖等多项奖励。
课题组简介
张万斌教授课题组一直致力于新型手性配体和催化剂的设计合成和应用,以及高效不对称催化反应的开发。与此同时,课题组还与工业界紧密合作,将开发的手性配体、催化剂以及高效不对称催化反应应用于手性药物、手性香料及其关键中间体的可工业化高效合成。
张万斌课题组主页:http://wanbin.sjtu.edu.cn/
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn