


(图片来源:J. Am. Chem. Soc.)
正文
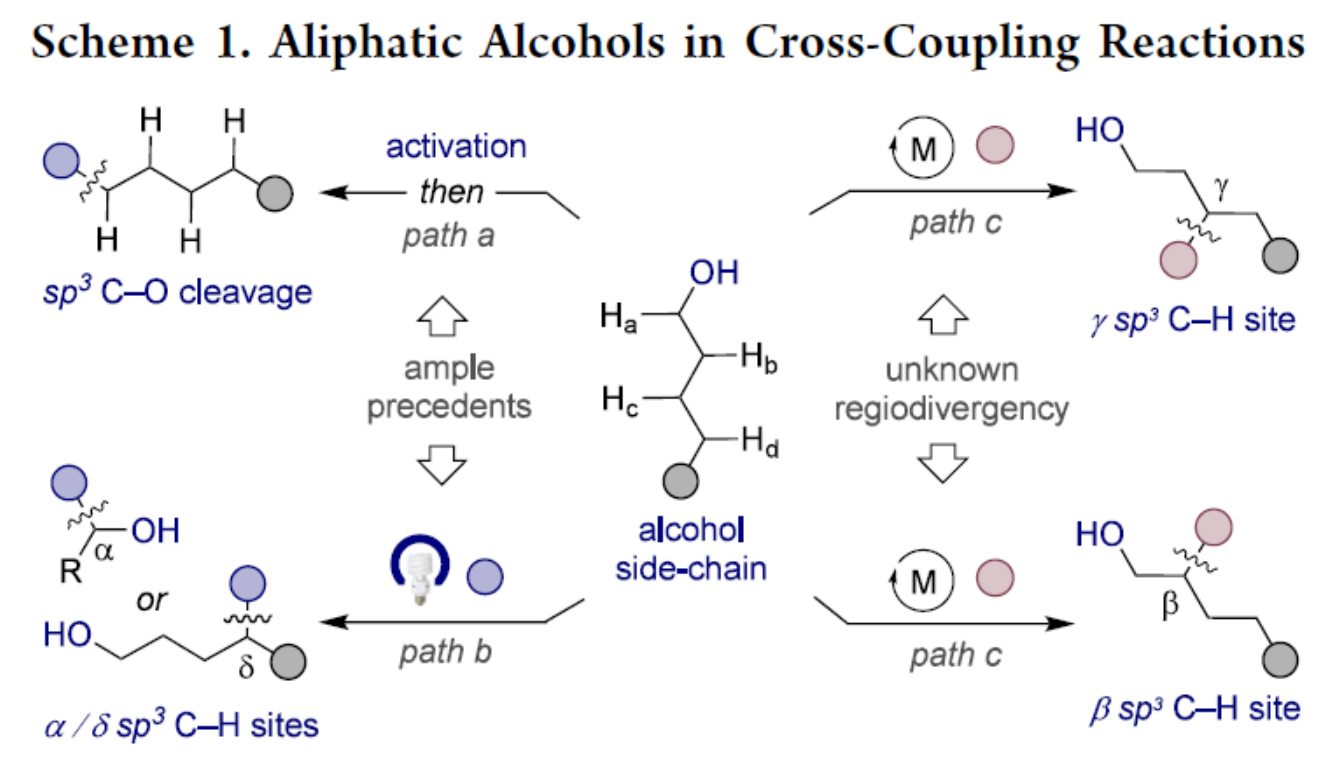
鉴于脂肪醇在众多药物分子中的广泛存在,化学家们面临设计新型催化技术的挑战:如何充分发挥脂肪醇作为关键中间体的潜力以实现深度修饰。相较于依赖预活化策略通过sp3 C−O键断裂进行的脱氧过程(Scheme 1,path a),催化sp3 C−H官能团化技术具有保留醇官能团的显著优势,从概念创新与合成应用双重视角均具有明显的优势。虽然光诱导过程已证实通过氢原子转移或配体-金属电荷转移(path b)实现了α/δ-位官能团化的可行性,但在交叉偶联领域中,利用地球丰富的金属催化剂精准调控β-或γ-位sp3 C−H键选择性插入碳/杂原子片段,进而实现区域发散性转化的系统性方案,仍有待进一步的探索(path c)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
(图片来源:J. Am. Chem. Soc.)
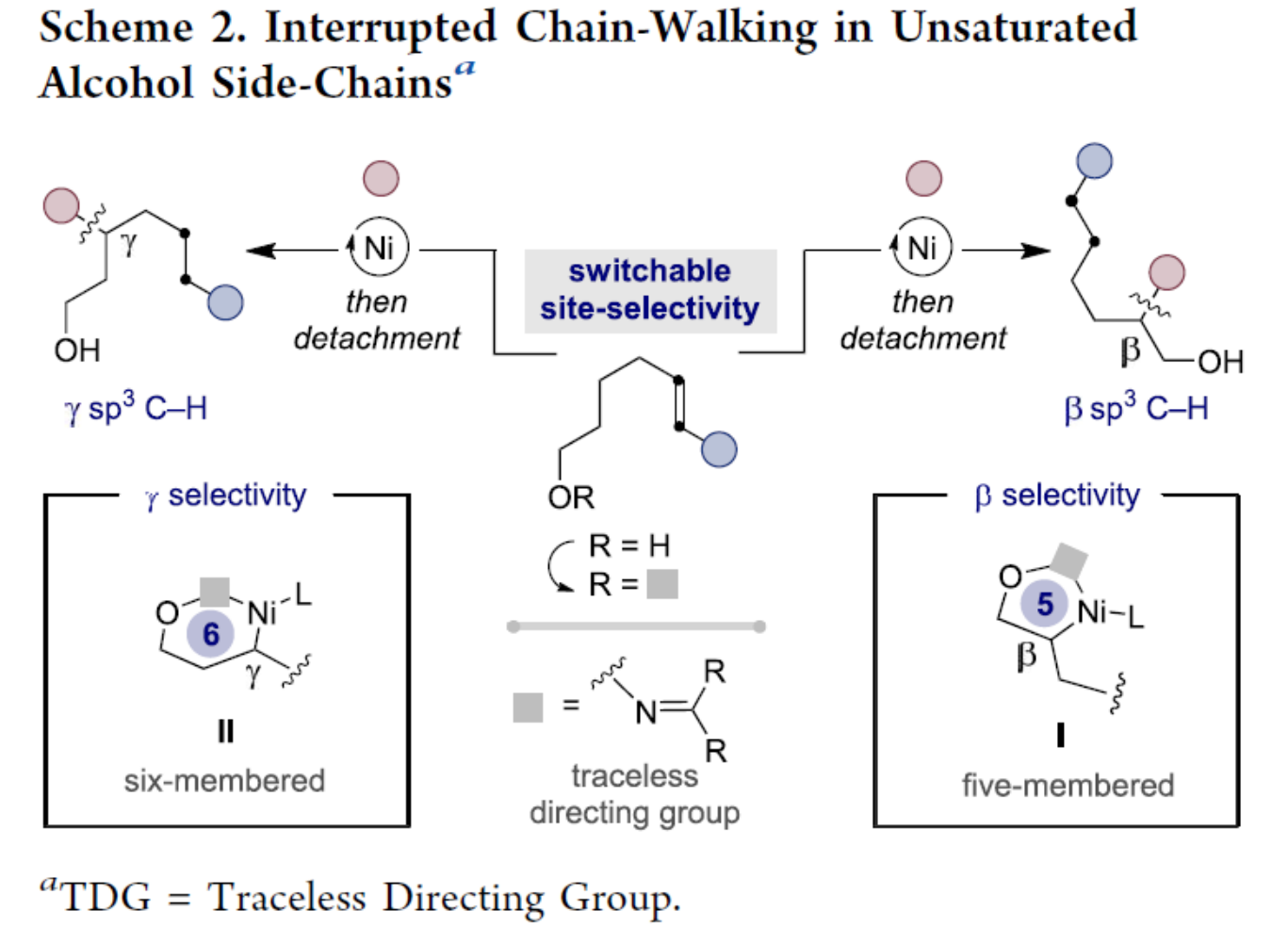
基于前期在镍催化阻断式链行走领域的最新研究进展,Martin团队设想,是否可设计一种新型的催化策略,可实现不饱和脂肪醇β-位与γ-位sp3 C−H键的化学键构建。若该策略可行,将为醇类侧链官能团化开辟全新切入点,解决传统方法难以实现的修饰难题。鉴于O-H键的高极化率及邻近氢原子的存在可能损害反应活性与位点选择性,Martin团队认为,有必要预先设计醇活化策略,再实施交叉偶联。该活化策略需满足:(a)易于在后续阶段以高化学选择性实现引入与脱除;(b)可预测选择性倾向。Martin团队设想,通过引入肟基作为无痕导向基团,利用五元/六元镍杂环(I和II)在亲电试剂偶联前的优势构型,从而可实现位点选择性的控制(Scheme 2)。近日,Martin团队开发了一种具有普适性的阻断式链行走策略,可在醇类侧链β-/γ-位sp3 C−H键上实现胺基/脂肪碳骨架的修饰,并展现精准的位点选择性。
(图片来源:J. Am. Chem. Soc.)
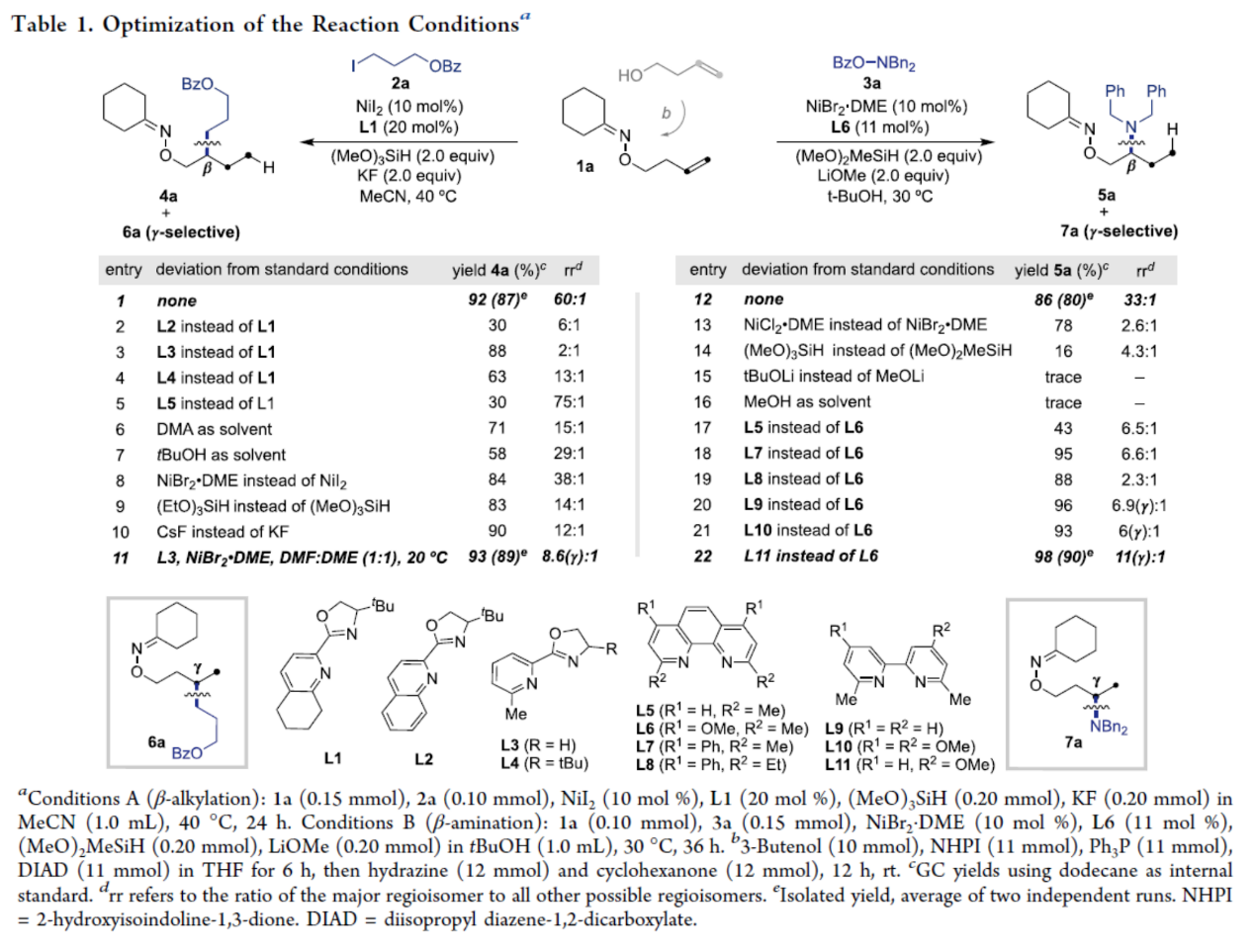
其次,作者以1a与2a作为模型底物,进行了相关反应条件的筛选(Table 1)。当以NiI2(10 mol %)作为催化剂,L1(20 mol %)作为配体,(MeO)3SiH(2 equiv)作为还原剂,KF(2 equiv)作为碱,在MeCN溶剂中40 oC反应,可以92%的收率得到β-选择性烷基产物4a,rr为60:1。与之形成鲜明对比的是,当以1a与3a作为底物,NiBr2·DME(10 mol %)作为催化剂,L6(11 mol %)作为配体,(MeO)3SiH(2 equiv)作为还原剂,LiOMe(2 equiv)作为碱,在tBuOH溶剂中30 oC反应,可以86%的收率得到β-选择性胺化产物5a,rr为33:1。值得注意的是,当使用L11作为配体时,可以98%的收率得到γ-选择性的产物7a,rr为11:1。
(图片来源:J. Am. Chem. Soc.)
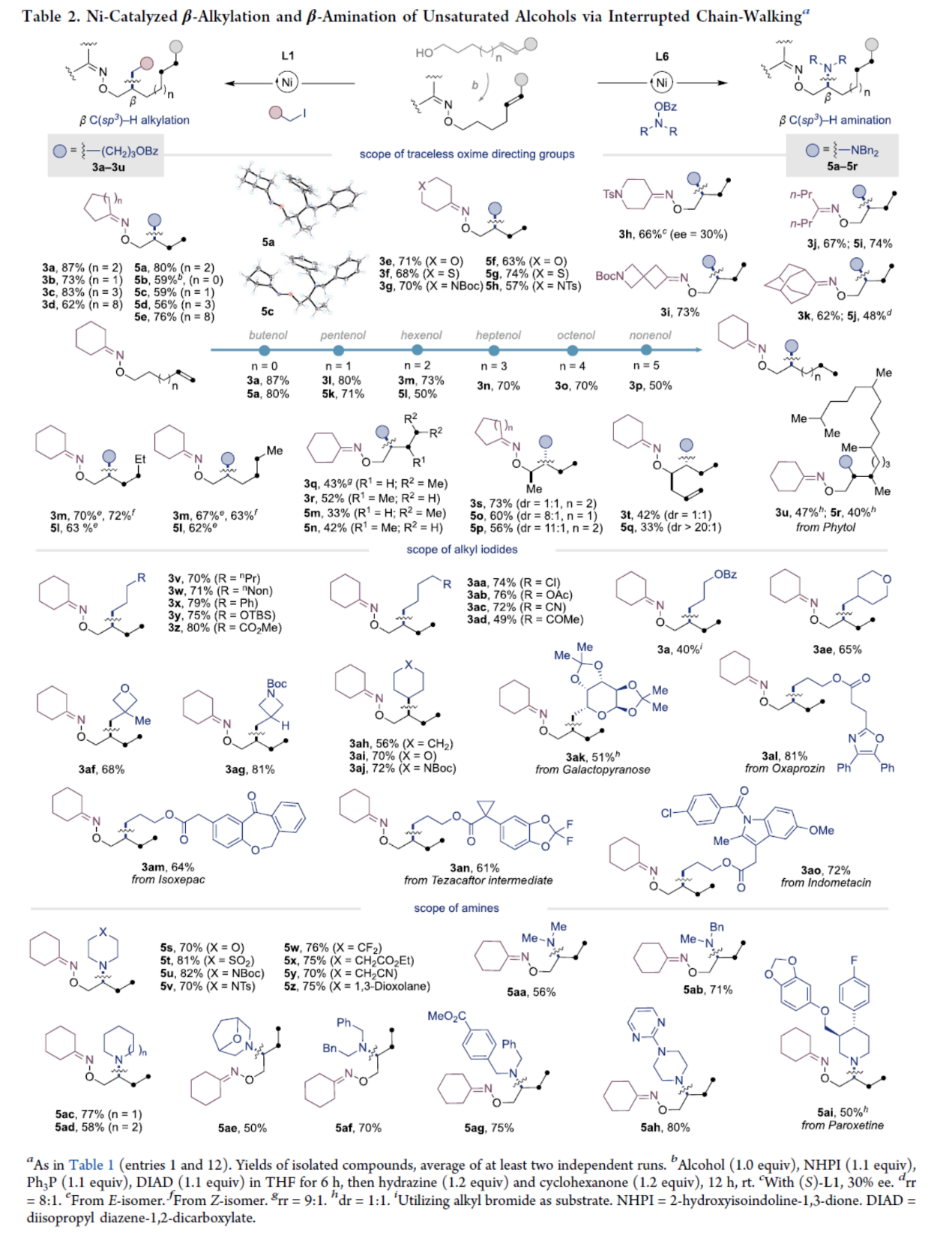
在获得上述最佳反应条件后,作者对区域发散性β C(sp3)−H烷基化和β C(sp3)−H胺化的底物范围进行了扩展(Table 2)。首先,当不饱和醇底物中的无痕导向基团中含有各种(杂)环烷基与烷基时,均可顺利反应,分别获得相应的烷基化产物3a-3k(收率为62-87%)和胺化产物5a-5j(收率为48-80%)。同时,具有不同链长度的不饱和醇底物,也能够顺利进行链行走,具有独特的β-选择性(3a和5a vs 3l-3p和5k-5l),但对于较长链的底物收率略有下降,特别是在进行β C(sp3)−H胺化时(5a vs 5k-5l)。内烯烃,也是合适的底物。值得注意的是,E-或Z-内烯烃均可用于β C(sp3)−H烷基化(3m),而β C(sp3)−H胺化(5l)只能使用E-烯烃。虽然三取代或1,1-二取代的烯烃,也是合适的底物,但收率较低(3q-3r和5m-5n),产率为42-52%。在醇官能团附近具有取代基的不饱和醇,可生成具有精确位点选择性的相应β-异构体(3s-3t和5o-5q),产率为33-73%。然而,当使用非活化烷基碘化物(3s-3u)进行反应时,仅获得非对映异构体的外消旋混合物;而在β-位C(sp3)−H胺化反应中(5o-5q)则观察到高度的非对映选择性,证明了该策略的内在复杂性。其次,一系列不同取代的烷基碘,也能够顺利进行反应,获得相应的烷基化产物3v-3z和3aa-3ao(收率为49-81%)。此外,不同烷基胺与环烷基胺,也与体系兼容,获得相应的胺化产物5s-5z和5aa-5al(收率为50-82%)。值得注意的是,一系列活性的基团,如烷氧羰基、氨基甲酸酯、腈、酮、砜和缩醛等,均与体系兼容。并且,该策略还可用于一些复杂分子的后期衍生化,如植物醇(3u和5r)、吡喃半乳糖(3ak)、奥沙普秦(3al)、奥沙西泮(3am)、替扎卡托中间体(3an)、吲哚美辛(3ao)与帕罗西汀(5ai)等,产率为40-81%。
(图片来源:J. Am. Chem. Soc.)
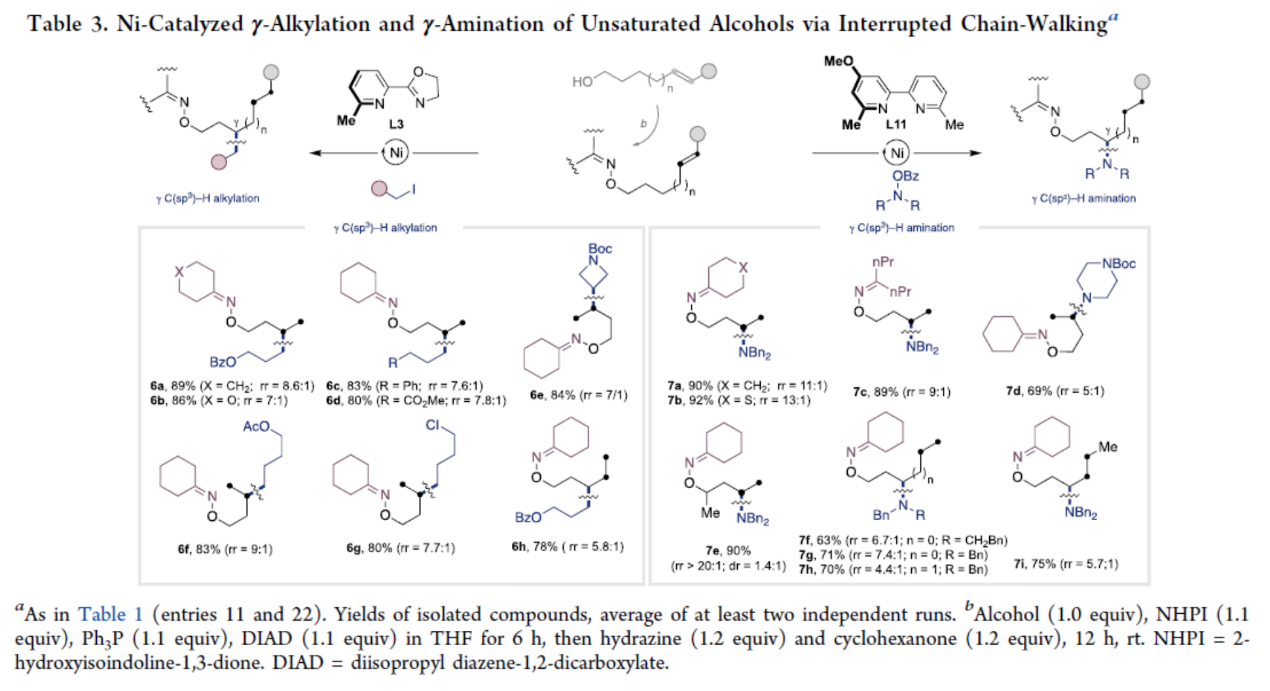
紧接着,作者对镍催化不饱和醇的γ-烷基化和γ-胺化反应的底物范围进行了扩展(Table 3)。研究结果表明,3-丁烯醇、4-己烯醇或5-庚醇分别可与多种非活化烷基碘化物及亲电胺类试剂反应,均以良好收率及区域选择性获得相应的目标产物(6a-6g、7a-7d、6h、7f-7i)。即便是含α-支链的醇类或带有内烯烃的底物,也可参与反应(7e与7i)。值得注意的是,前者呈现高度的非对映选择性,而后者则展现出明确的γ-位选择性。
(图片来源:J. Am. Chem. Soc.)
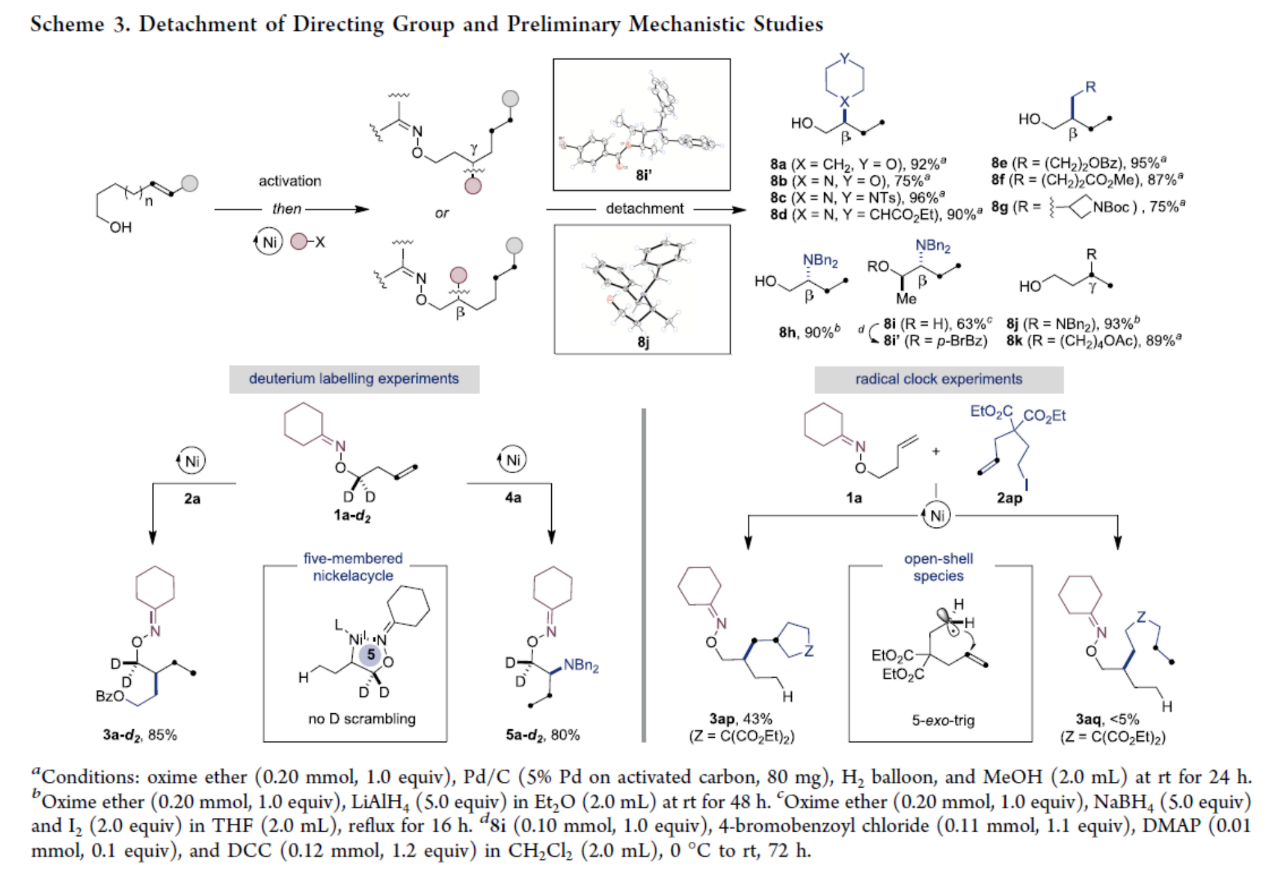
随后,作者对反应的实用性进行了研究(Scheme 3)。研究表明,无痕肟导向基团可通过两种途径实现烷基侧链的脱离:其一是暴露于H2氛围下的Pd/C催化体系(8a-8g和8k),其二是与适宜氢化物源反应(8h-8j)。X-射线衍射分析确证了化合物8j与8i′的结构,既明确了Ni/L11催化体系下的γ-位选择性(8j),又揭示了8i′的反式立体化学构型。尽管有人可能提出β-位选择性源于烯烃异构化形成乙烯基醚中间体,该中间体继而与非活化烷基卤化物或亲电胺源反应,但在实时监测1a与2a或1a与4a的反应过程中,通过¹H NMR谱分析也未检测到痕量乙烯基醚的存在。当使用氘代底物1a-d2时,在产物3a-d2和5a-d2的β-位未检测到氘原子掺入,从而进一步证实β-位选择性源于五元镍环中间体,而γ-位选择性则可能由六元镍环中间体介导(Scheme 3,bottom left)。另一方面,通过在优化的β-位烷基化条件下可使底物2ap与1a反应,间接证实了开壳层中间体的存在。在接近检测限的条件下,粗反应混合物中检测到痕量产物3aq,但同时以43%收率获得了主产物3ap(Scheme 3,bottom right)。
(图片来源:J. Am. Chem. Soc.)
总结
Ruben Martin团队开发了一种利用肟作为无痕导向基团,在不饱和醇侧链上实现可切换且可预测的阻断式链行走反应新模式。位点选择性通过精准调控配体骨架结构实现,这为在远端非官能团化的sp3 C−H键位点引入sp3结构提供了全新途径。该策略的普适性与多功能性不仅拓展了链行走反应的应用边界,更开辟了获取药物化学目标化合物的非经典逆合成解析路径。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn