

手性α-氨基酮广泛存在于药物活性分子中(图1a)。因此,发展高效地构建该类分子骨架的方法一直以来都尤为重要。然而,该过程也充满了挑战。目前比较经典的方法主要是羰基α-位的亲电胺化和亲核胺化反应(图1b)。然而,这两种方法也存在着明显的局限性。对于亲电胺化,二烷基酮类底物往往得到多种异构体,并且对于反应中的氮源也有要求,比如偶氮二甲酸酯等;对于亲核胺化,虽然可以用自由胺作为氮源,但需要先将酮转化为α-卤代酮、α-重氮酮等。因此,这两种方法均不是特别理想。显然,通过氨基α-位的C-H键的不对称酰基化反应则无疑是更加简洁高效的策略,但烷基C-H键的不对称官能团化反应一直以来都是C-H键官能团化领域的一大挑战。鉴于近些年金属与光协同催化的发展如火如荼,特别是镍催化与光催化的有效结合,可以通过单电子转移或者氢原子攫取的策略解决常规放大难以实现的烷基C-H键的官能团化反应,比如导向型的C-H键的官能团化。在此,作者利用镍催化剂与可见光协同催化的策略,从N-烷基苯甲酰胺出发,以羧酸为酰基化试剂,成功地实现了手性α-氨基酮的构建(图1c)。该工作于近日发表在化学顶级期刊J. Am. Chem. Soc.上。
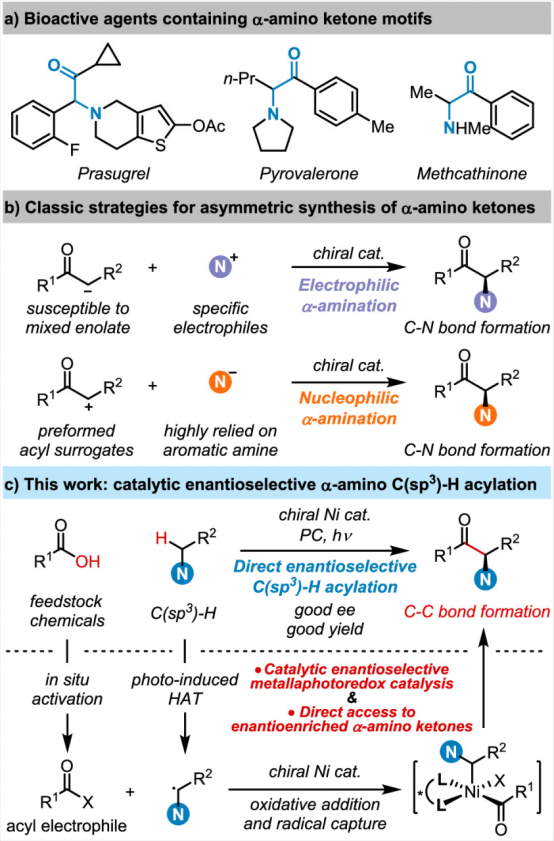
图 1:含α-氨基酮骨架的活性分子及其不对称合成 (图片来源:J. Am. Chem. Soc.)
对于条件筛选部分,作者在镍催化下,采用N-戊基苯甲酰胺为底物,丁酸为酰基化试剂,铱络合物为光敏剂,手性双噁唑啉 (R,S)-L为配体,反应能以90%的产率和92%的ee值得到α-氨基酮产物(图2)。其中,DMDC(二碳酸二甲酯)为羧酸活化剂,可以将羧酸转化为混酐。经研究发现,当不加入镍催化剂、配体、光敏剂或光时,反应均不能进行,证明了这些因素在反应中的重要性。
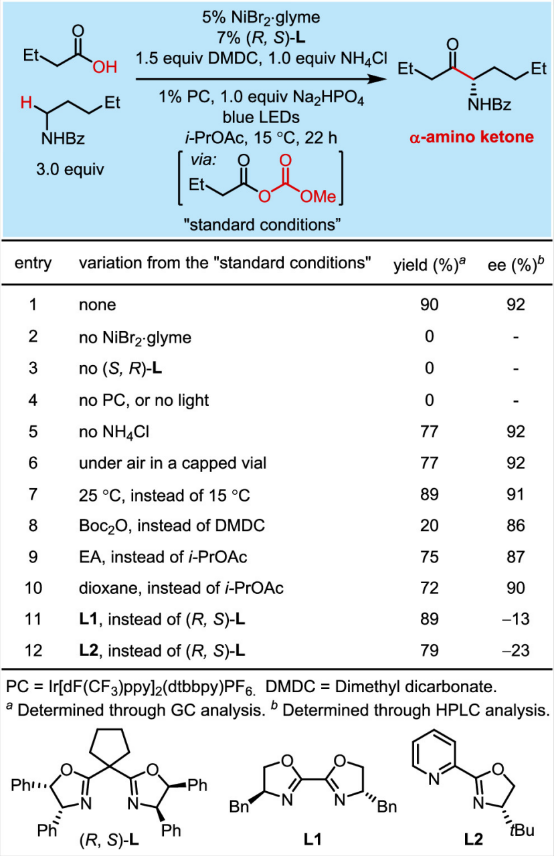
图 2:条件优化 (图片来源:J. Am. Chem. Soc.)
随后,基于如上的最优条件,作者对反应的底物范围进行了考察(图3)。作者先是研究了不同羧酸的反应情况。实验结果表明,官能团如三氟甲基、氰基、甲酯基、卤素等均能兼容,并能取得很好的收率和对映选择性(1-21)。而对于各种不同的酰胺类底物,反应也能取得良好的结果(22-37)。此外,作者还发现该方法学适用于天然产物和药物分子的后期官能团修饰中(38-49)。
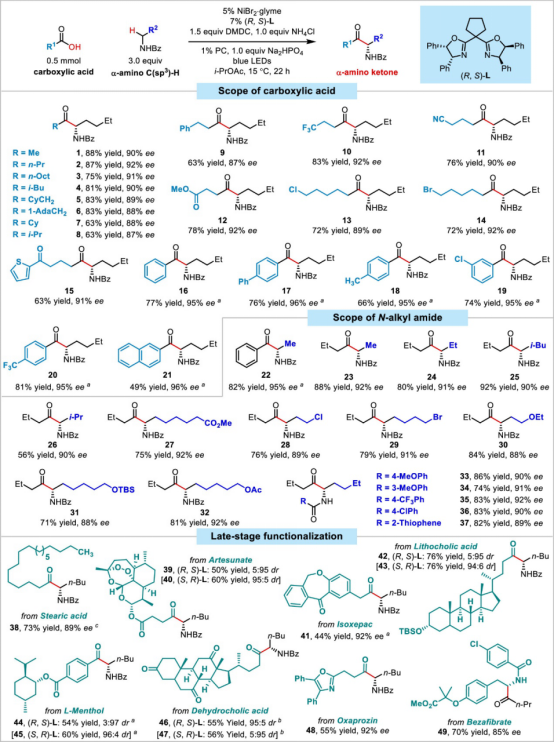
图 3:底物拓展 (图片来源:J. Am. Chem. Soc.)
为了进一步证明该方法学的应用,作者还将反应放大到克级规模,发现能以58%的收率和94%的ee值得到目标产物20。从化合物20出发,经一步简单的反应可以高效地转化为β-氨基三级醇50,β-氨基二级醇51,手性噁唑啉配体52和β-苄胺53(图4)。
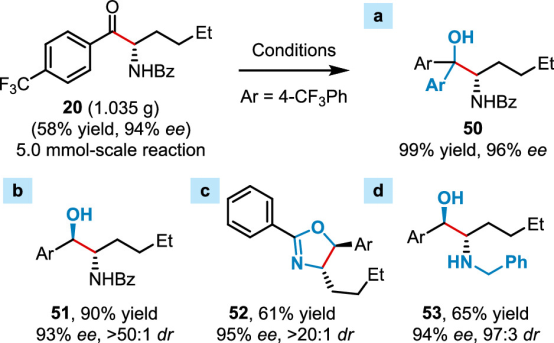
图 4:克级规模反应和转化 (图片来源:J. Am. Chem. Soc.)
为了研究反应的机理,作者开展了如下的一系列实验(图5):首先,为了证明α-氨基自由基的存在,作者加入烯丙基砜作为捕捉剂,发现反应只能以21%的收率得到消旋的加合物,过程中未观察到目标产物,这便证实了作者的猜想(图5a)。平行与竞争的KIE实验均能得到较大的KIE值,则证明了C-H键可能存在于决速步中(图5b)。对其它的镍催化剂进行研究,发现不加溴的镍催化剂只能得到小于10%的产物。有意思的是,作者发现当加入NaBr时,反应的产率和ee值均有明显的提升。这可能是由于Br离子在光化学条件下可以生成Br自由基,从而促进后续反应的进行,这在过去的文献中也有相关的报道(图5c)。
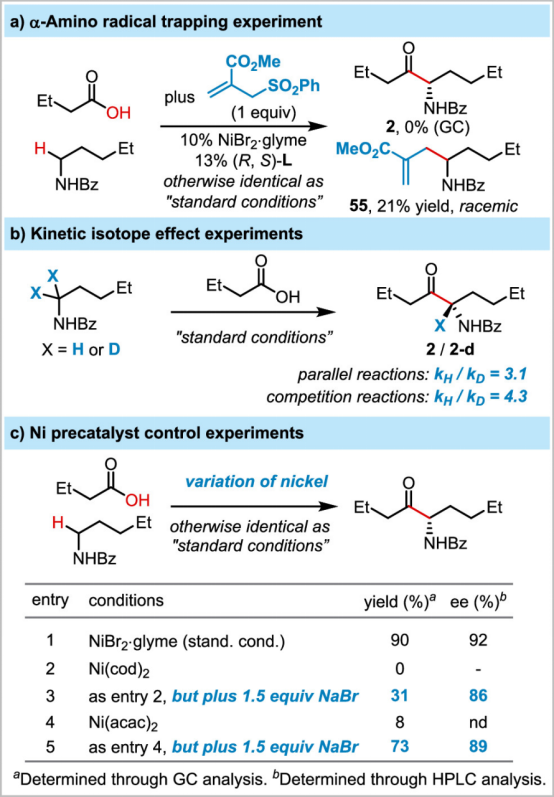
图 5:机理研究 (图片来源:J. Am. Chem. Soc.)
基于如上实验结果和文献调研,作者提出了可能的机理(图6):羧酸在DMDC的作用下可以生成混酐,后者可与Ni(0)物种I经氧化加成生成Ni(II)物种II。同时,在光化学氧化条件下可以产生溴自由基,后者与酰胺经氢原子转移生成稳定的α-氨基自由基物种。该自由基物种可以将II氧化为Ni(III)物种III。III经还原消除可以得到目标产物,生成的Ni(I)物种IV与Ir(II)经单电子转移可以重生Ni(0)物种I。
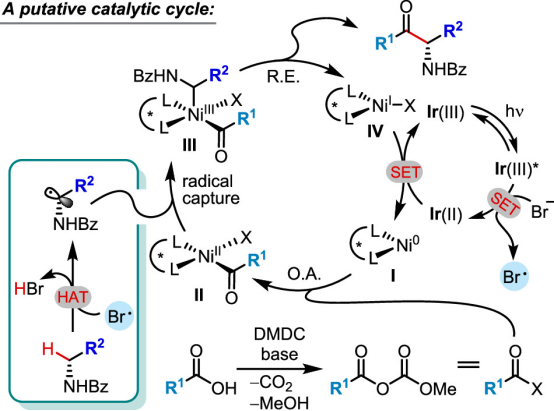
图 6:可能的机理 (图片来源:J. Am. Chem. Soc.)
总结:厦门大学的霍浩华课题组报道了金属与光协同催化的不对称烷基C-H键酰基化反应,成功地实现了手性α-氨基酮的构建。该反应采用易于获得的N-烷基酰胺为底物,羧酸为酰基化试剂,反应产率和对映选择性选优秀,条件温和。该过渡金属与光协同催化的策略为不对称烷基C-H键官能团化提供了新的思路。
文章链接: https://pubs.acs.org/doi/10.1021/jacs.0c10471
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn