

1
CMC是什么
CMC是chemistry, manufacturing, and controls的缩写,它包括的主要技术部门有三个:
Process chemistry,负责从化学合成前体(starting material)到原料药(drug substance,又称API)的部分;
Formulation,负责从原料药到成药的部分;
Analytical,负责着整个过程中所有的分析方法。
在这三个主要的技术部门之外,还有一些重要的非技术部门,例如Quality Assurance (QA),Outsourcing,Regulatory等等,在CMC project team里占有重要的地位。
CMC的职能有两大方面,一是development,把从早期研发中得到的lead compound有效地转化为可以上市的药物;另一个是manufacturing,在临床阶段以及上市后,负责把药物供给到临床研究或者市场中去。这也就是为什么现在很多的支持CMC部分的contract organization把自己叫做CDMO,contract development and manufacturing organization。
2
CMC团队在药物开发中的作用
下图比较清晰地描述了CMC在药物开发不同环节的作用:
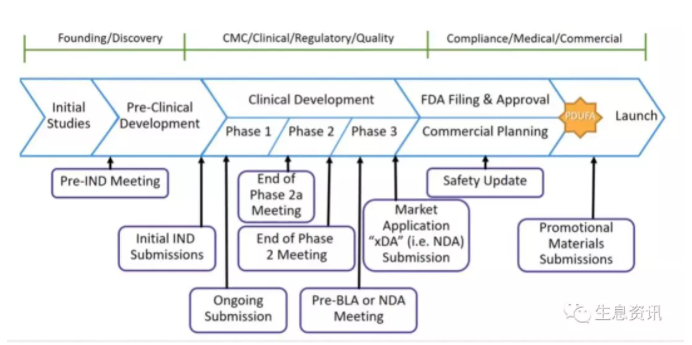
CMC的项目团队组建一般是从late stage preclinical开始的。
企业里面,当有一个lead compound,在preclinical 阶段做了大量的研究,认为这个化合物有潜力,有一定的数据可以支持安全性以及体内外proof of concept的结果后,就会提交公司内部申请立项。此时这个化合物就进入到了development的阶段,为了支持之后的生产和研发,公司就会组建CMC project team来接手。
通常来讲,一个早期的CMC project team会有起码7个成员,包括:
project lead,project manager,process lead,formulation lead,analytical
analytical lead,QA lead,和regulatory affairs lead。当然,这些成员中的一些可能同时在几个项目上,身兼数职。而每个lead身后,都有或大或小的团队来支持。当项目进行到后期,project team可能会加入新的成员,例如outsourcing,clinical supply,packaging and device等等。
在小分子化学领域,通常来讲CMC team的第一个milestone就是做出来IND enabling tox batch。这个是第一个API batch,用来供给 Phase 1 IND需要的GLP tox study,这个研究需要的材料是GMP生产的,而且合成路线最好是可以放大产量的路线。
与此同时,CMC team还要进行合成工艺放大,早期剂型的研究,Phase appropriate 分析方法的建立和验证,以及着手准备第一个phase 1 manufacturing campaign。因为在美国,IND submission是没有批准这一回事的,提交申请之后的 30天内,如果FDA没有回复,就可以立刻开展临床试验,所以这段时间是非常紧迫的。(虽然FDA 不会issue approval notice for IND application,但是FDA什么时候发现问题都可以叫停你的trial。)
从这点也可以看出来,CMC团队的时间线完全是由临床试验的计划来决定的,从一定程度上来讲,CMC在医药公司的地位多是那种只能成功不能失败的角色。因为如果临床实验失败了,人们会觉得是science还不够好,或者运气不好。但是如果是CMC跟不上节奏,人们会觉得是水平不行。(无奈)
一旦临床试验开始,CMC的主旋律就在development和manufacturing之间穿梭。用于临床实验的药物不够了,就要赶紧生产以赶上进度;在生产的间歇,需要加大力度研究生产条件的优化,方法的优化,合成路线的优化,剂型的优化等等。就analytical lead的职能来说,从分析方法设计,到validation,transfer,CRO management,再到生产过程的支持,batch release,stability以及在NDA,BLA filing过程中撰写module 2&3非常宽泛。
如果一切顺利,药物通过临床实验,要最终报批上市了,CMC也要参与。
Market application是一个庞大的package,来论证为什么这个药可以上市,为什么其效益大于风险。这个过程具体来讲就是提交上市申请,包括美国的NDA/BLA,欧洲的MAA,日本的JNDA等等。
现在大多数国家都加入了ICH (international committee for harmonization),
中国去年也刚刚加入。加入ICH的国家的上市申请一般都会遵循CTD的格式,如下图:

CTD就是common technical document,是一个文本模版,来规划上市申请的每个部分都说些什么。其中最重要的为三个部分(Module 3,4,5)。可以看到,Module 3 讲的是Quality,又叫CMC module。这个module论述以下几点:这个药是怎么做出来的,为什么要这么做,过程和结果是怎么控制的,药物稳定性怎么样。
Module 3 中的所有内容都需要CMC project team来完成,从主要章节的分工来讲:
-Process chemistry负责3.2.s中关于生产的章节,来论述合成路线的设计,起始化合物的选择,杂质的控制,潜在致癌物的控制等等。
-Formulation负责3.2.p中关于生产的章节,论述辅料的选择,剂型的设计,重金属的控制等等。如果有成药中间体,例如Spray dried dispersion,hot melt extrusion等等,也会放在3.2.p中讨论。
-Analytical负责剩下所有的章节,在Module 3里,analytical的比重是最大的,因为所有的论点都需要analytical data 来论证。同时analytical负责stability的部分,来论证原料药的retest period以及成药的保质期。
(当然每个公司的习惯不同,这些章节有时候是technical team来写,regulatory team来review,有的是倒过来,但是两个部门都会很具体的参与到讨论中去。)
在NDA filing之后,CMC team需要准备两件事,PAI(pre-approval inspection)和response to regulatory questions。第一件事,PAI就是要把所有写入FDA的数据归纳成册,以备FDA来检查的时候迅速的拿出来,同时还是一个查漏补缺的过程,做一些gap analysis。第二件事就是要准备回答FDA的问题。因为在审理的过程中,FDA可能会有这样那样的问题,会在60天,90天,120天及以后的时间点向公司提出。公司一般有30天或者更短的时间回答。这些问题又时候能够轻易的写几句话,有时候需要做实验,所以团队需要做好万全的准备回答问题。
在NDA approve之后,CMC的工作也还在继续。上市后,commercial manufacturing以及post approval market surveilance也是CMC的职责。NDA之后的一年内,项目会从development转给commercial。
可以说,一个项目从头到尾是很大的工程,一般project lead会一直跟进,development的时间取决于therapeutic area,3-10年不等。但是因为人员流动的问题,project lead也会更换。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn