

近日,陆展课题组和洪鑫课题组合作,利用一种自主设计的三功能钴催化剂——噻唑啉亚胺吡啶(TIP)碘化钴络合物,实现了烯基环丙烷的不对称串联硼氢化/异构化/硼氢化反应,合成了高对映选择性的手性1,5-二硼化合物。基于合成的手性1,5-二硼化合物,作者可以通过简单的化学转化克级规模合成市售抗精神病药物丙克拉莫,同时可以通过逐级偶联反应构建1,2,5-三芳基戊烷类化合物。
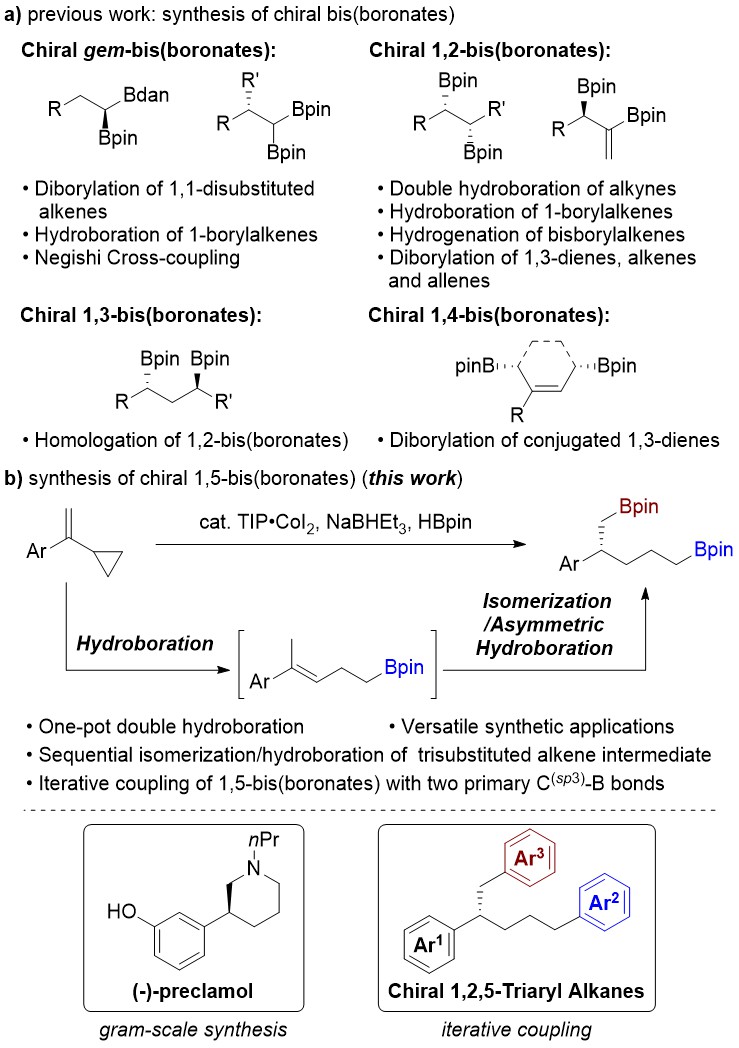
图1.手性二硼化合物的合成现状与本文工作
经过条件优化,作者对2-芳基烯基环丙烷底物的范围进行了考察。结果表明,反应对于单取代、多取代的芳基、杂芳基以及天然产物修饰的底物都能取得较好的结果,以优秀的对映选择性得到手性1,5-二硼化合物(图2)。
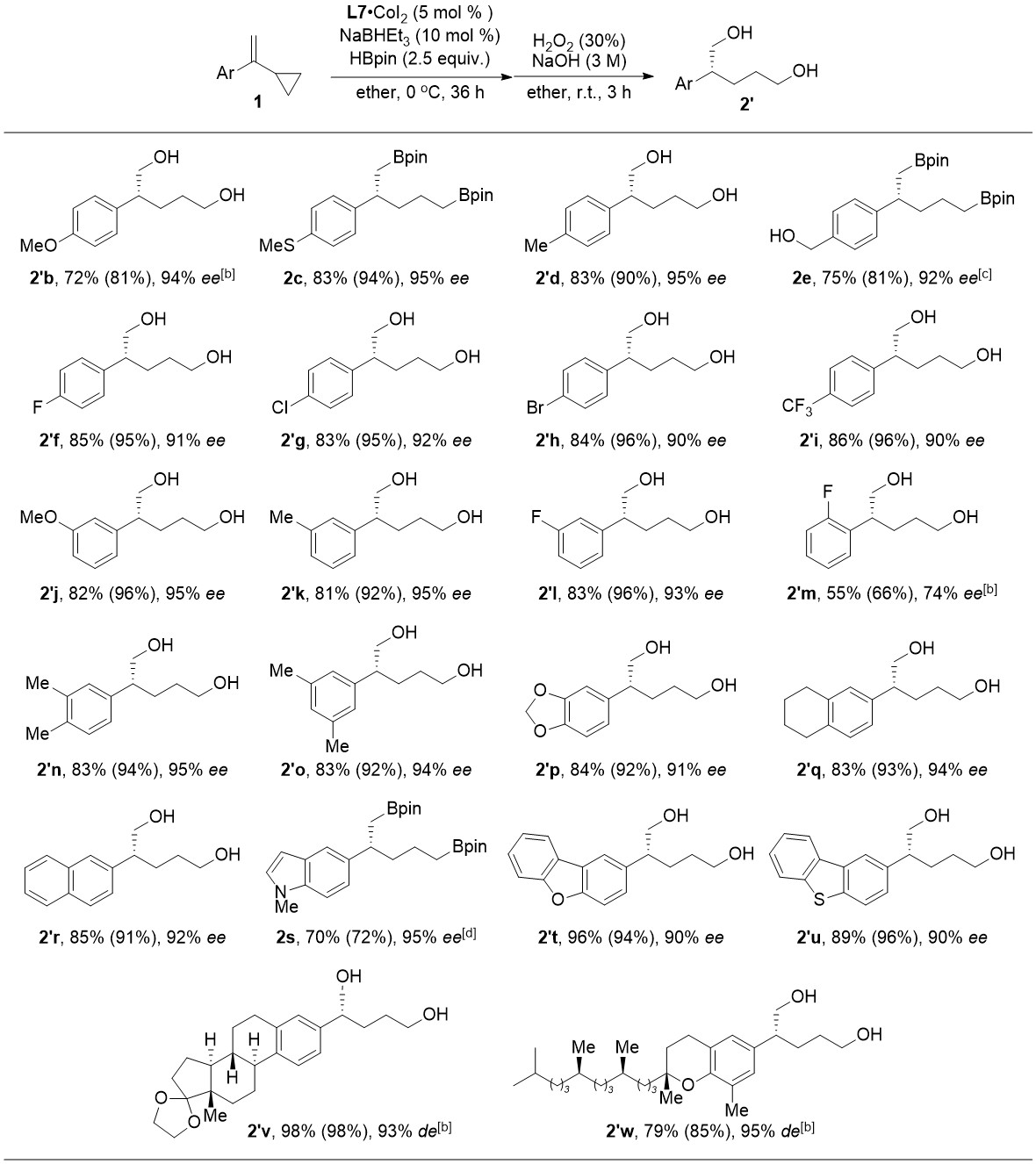
图2.底物范围考察
在探索产物的合成应用过程中,作者发现手性1,5-二硼化合物的两个不同位置的含硼基团可以在Suzuki-Miyaura偶联反应中被区分,与两个不同的芳基卤化物发生逐级偶联反应。由此作者通过逐级偶联反应,合成了一系列含有天然产物分子的多芳基化合物(图3)。
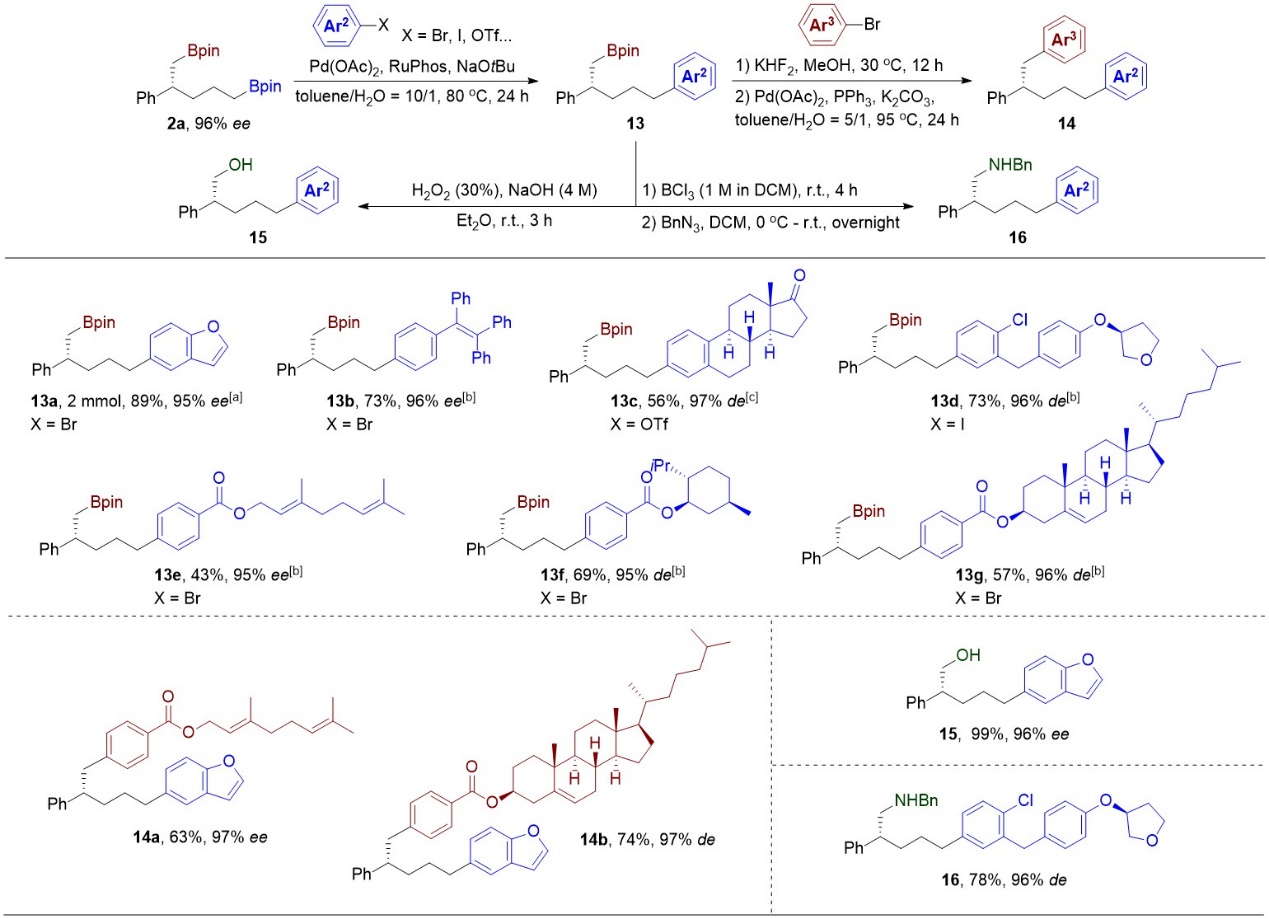
图3.手性1,5-二硼化合物的合成应用
作者接着通过理论计算阐明了该反应的机理(图4)。噻唑啉亚胺吡啶(TIP)碘化钴催化剂在三乙基硼氢化钠的作用下形成钴氢活性中间体,该活性中间体催化了第一次硼氢化反应、异构化反应和第二次硼氢化反应。中间体1,1-二取代烯烃17与钴氢活性中间体的插入反应是反应的手性决定步。在该过程中,催化剂噻唑啉上的手性基团以及2,6-二乙基苯基占据了象限图的第II、III、IV象限,同时中间体17的芳基与催化剂的2,6-二乙基苯基在第II象限存在位阻,这使得反应更倾向于生成R构型的产物。
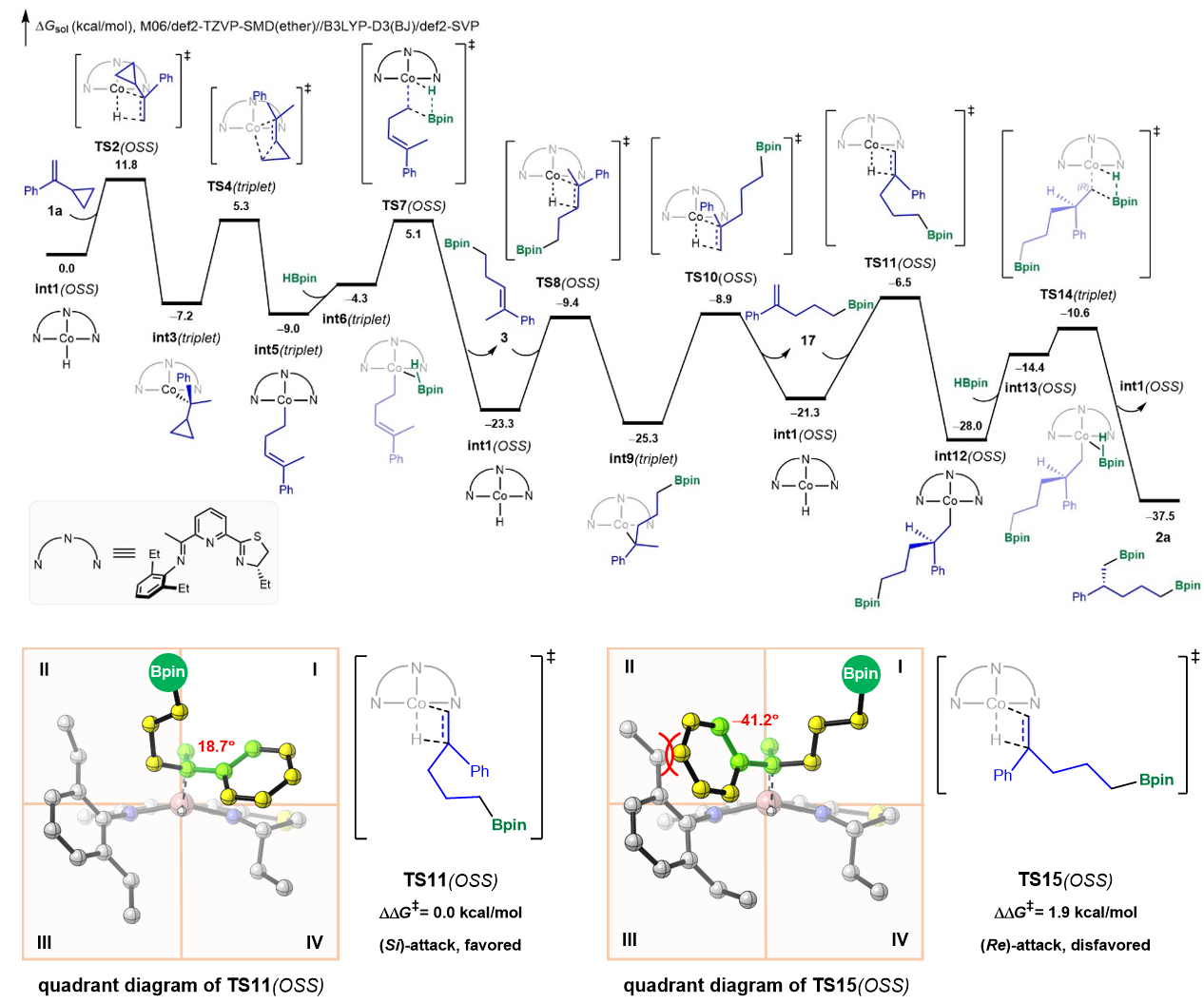
图4.反应的机理研究
综上所述,作者基于配体设计的策略,利用噻唑啉亚胺吡啶(TIP)碘化钴络合物作为催化剂,实现了烯基环丙烷的不对称双硼氢化反应,合成了一系列高对映选择性的手性1,5-二硼化合物;还通过与两个不同的芳基卤化物发生逐级偶联反应,合成了一系列含有天然产物分子的多芳基化合物。该工作的创新点在于:1)提出钴氢活性中间体同时催化了三个不同的催化循环过程,并且通过理论计算支持了这一结论;2)实现中间体三取代烯烃的串联异构化/不对称硼氢化反应,为后续三取代烯烃的不对称转化建立了基础;3)实现手性1,5-二硼化合物的逐级官能团化反应,为手性二硼化合物的应用提供了的启示。
本文的共同第一作者是浙江大学博士后陈晨辉、浙江大学博士后王洪亮和浙江大学化学系博士研究生李同彤,通讯作者是陆展教授和洪鑫研究员。该项目受到国家重点研发计划项目、国家自然科学基金优青项目和面上项目、浙江省自然科学基金、浙江大学杭州国际科创中心、北京分子科学国家实验室、西湖大学、郑州大学以及中国博士后科学基金等经费资助。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202205619
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn