

(图片来源:Angew. Chem. Int. Ed.)
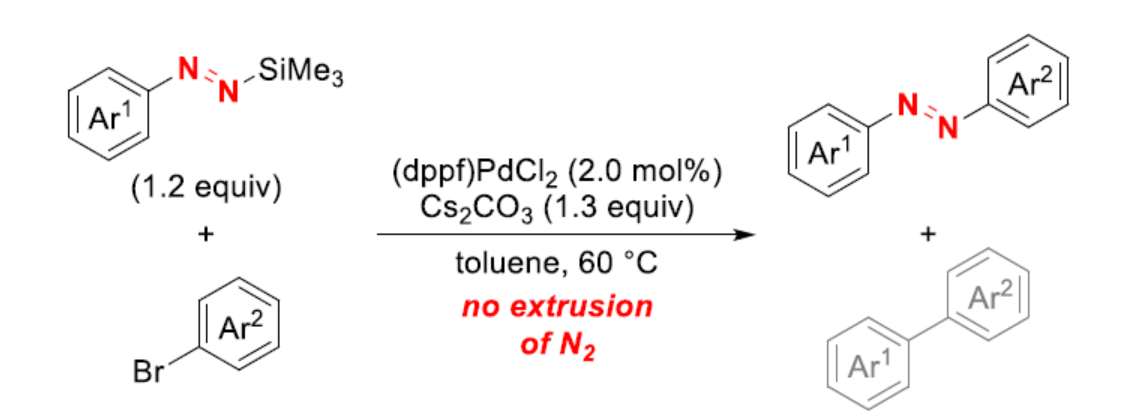
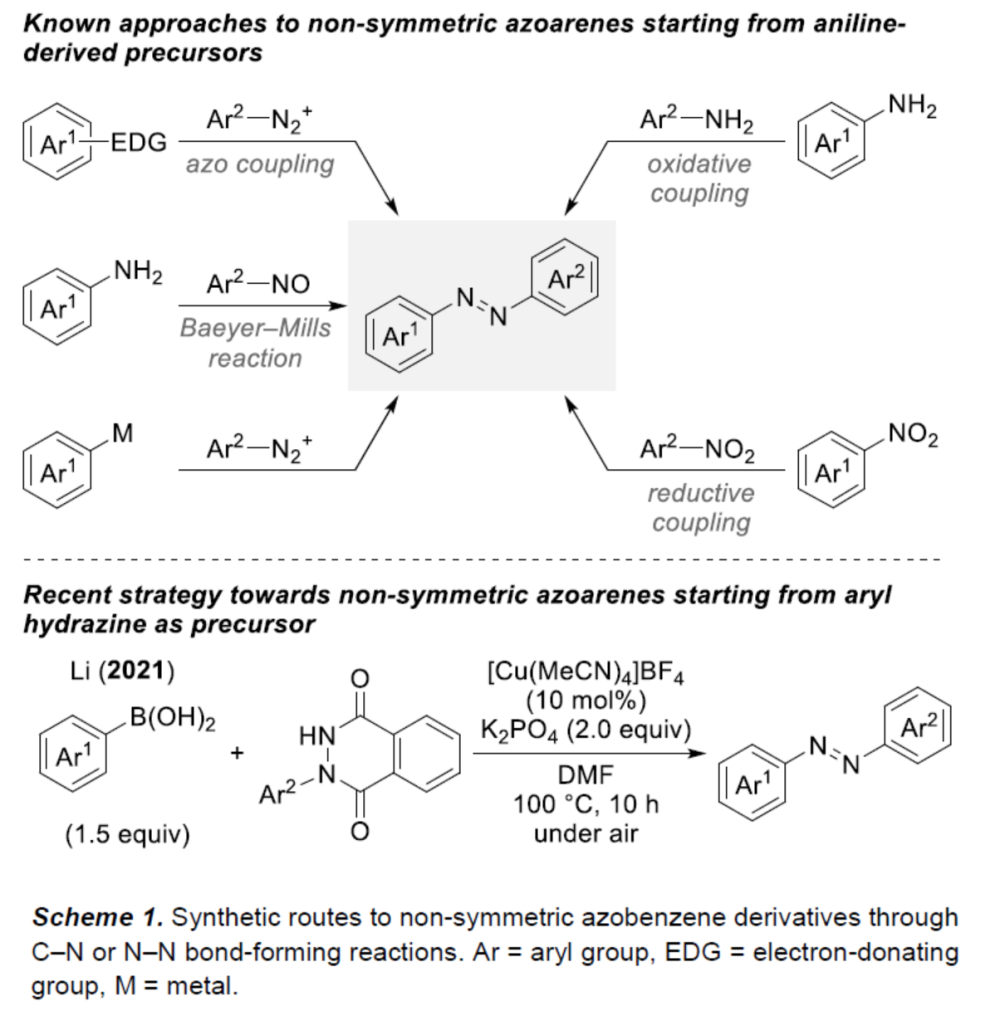
芳香族偶氮化合物由于具有调节化学和物理特性的能力,已广泛应用于有机染料、分子光开关和医疗等领域。虽然化学家们已开发了多种合成对称取代偶氮苯衍生物的方法,但对于非对称取代偶氮苯衍生物的合成则具有挑战(Scheme 1, top)。偶氮偶联是一种常用的策略,涉及重氮盐和富电子芳烃的SEAr反应。或者,亚硝基芳烃和苯胺衍生物在酸性条件下进行的偶联反应,即Baeyer-Mills反应。同时,重氮盐和金属化芳烃的偶联反应,可进一步扩展上述的底物范围。此外,通过苯胺衍生物的脱氢氧化偶联或硝基芳烃的还原异二聚化反应,也是合成非对称取代偶氮苯衍生物的有效策略。然而,对于同(homo-)和异二聚(heterodimerized)产物之间的分布通常不易控制。为了实现优先异二聚化过程,通常需使用大量过量的任一偶联底物。2021年,李世清课题组开发了一种铜催化N-芳基邻苯二甲酰肼和芳基硼酸的Chan-Evans-Lam型氧化交叉偶联,从而解决了上述的问题(Scheme 1, bottom)。
(图片来源:Angew. Chem. Int. Ed.)
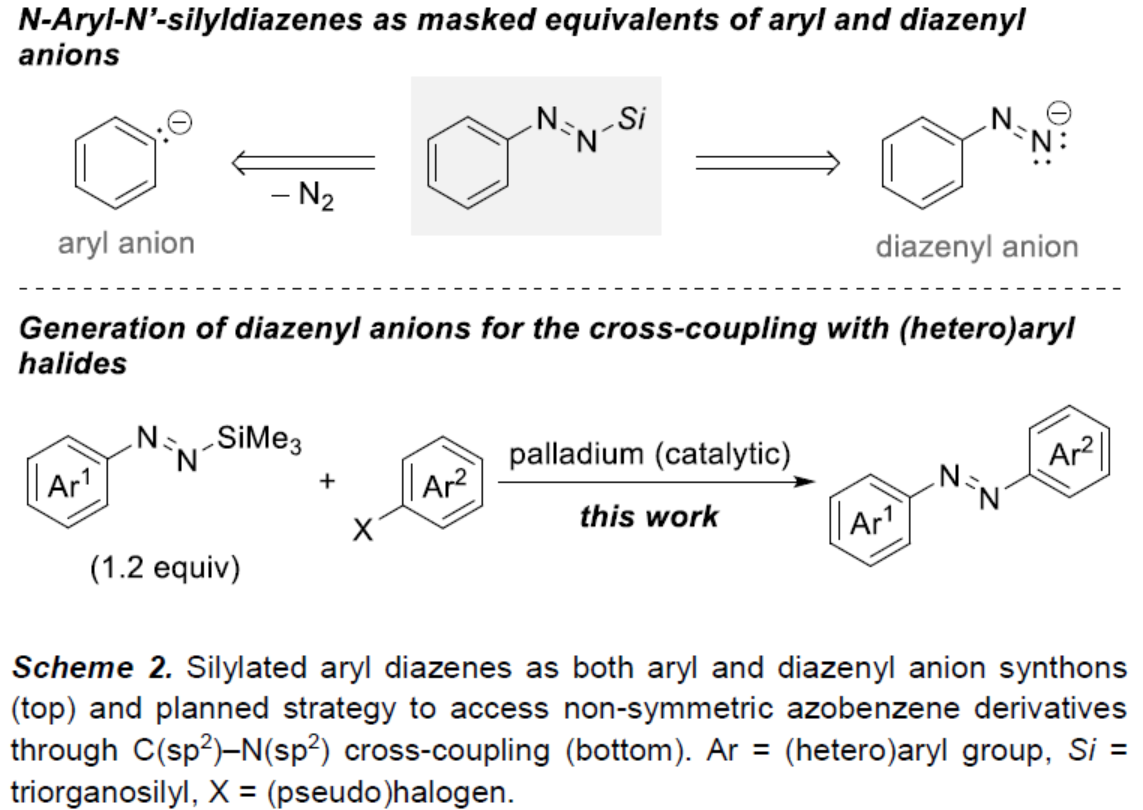
最近,Oestreich课题组发现,N-芳基-N'-硅基二氮烯在动力学上是稳定的,并可作为芳基亲核试剂,但会释放氮气。作者认为,N-芳基-N'-硅基二氮烯可作为二氮烯基阴离子的前体,且不会释放氮气(Scheme 2, top)。近日,柏林工业大学Martin Oestreich课题组报道了一种钯催化N-芳基-N'-硅基二氮烯与(杂)芳基卤之间的C(sp2)-N(sp2)键交叉偶联反应,合成了一系列非对称偶氮苯衍生物(Scheme 2, bottom)。
(图片来源:Angew. Chem. Int. Ed.)
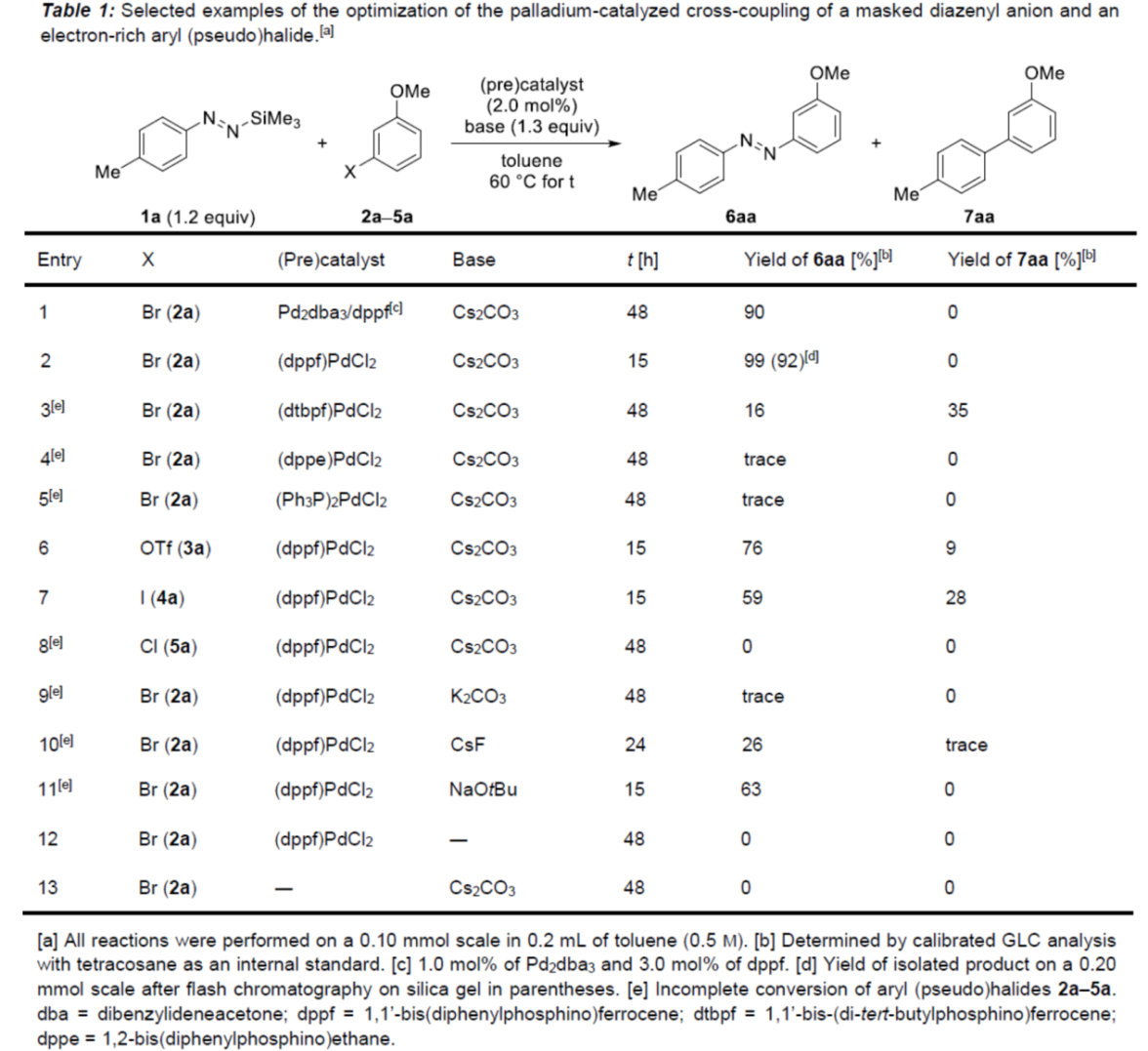
首先,作者以N-芳基-N'-硅基二氮烯衍生物1a与间卤苯甲醚2a-5a作为模型底物,进行了相关偶联反应条件的筛选(Table 1)。当以1a与2a作为底物, (dppf)PdCl2作为催化剂,Cs2CO3作为碱,在甲苯溶剂中60 oC反应15 h,可以92%的收率得到产物6aa。
(图片来源:Angew. Chem. Int. Ed.)
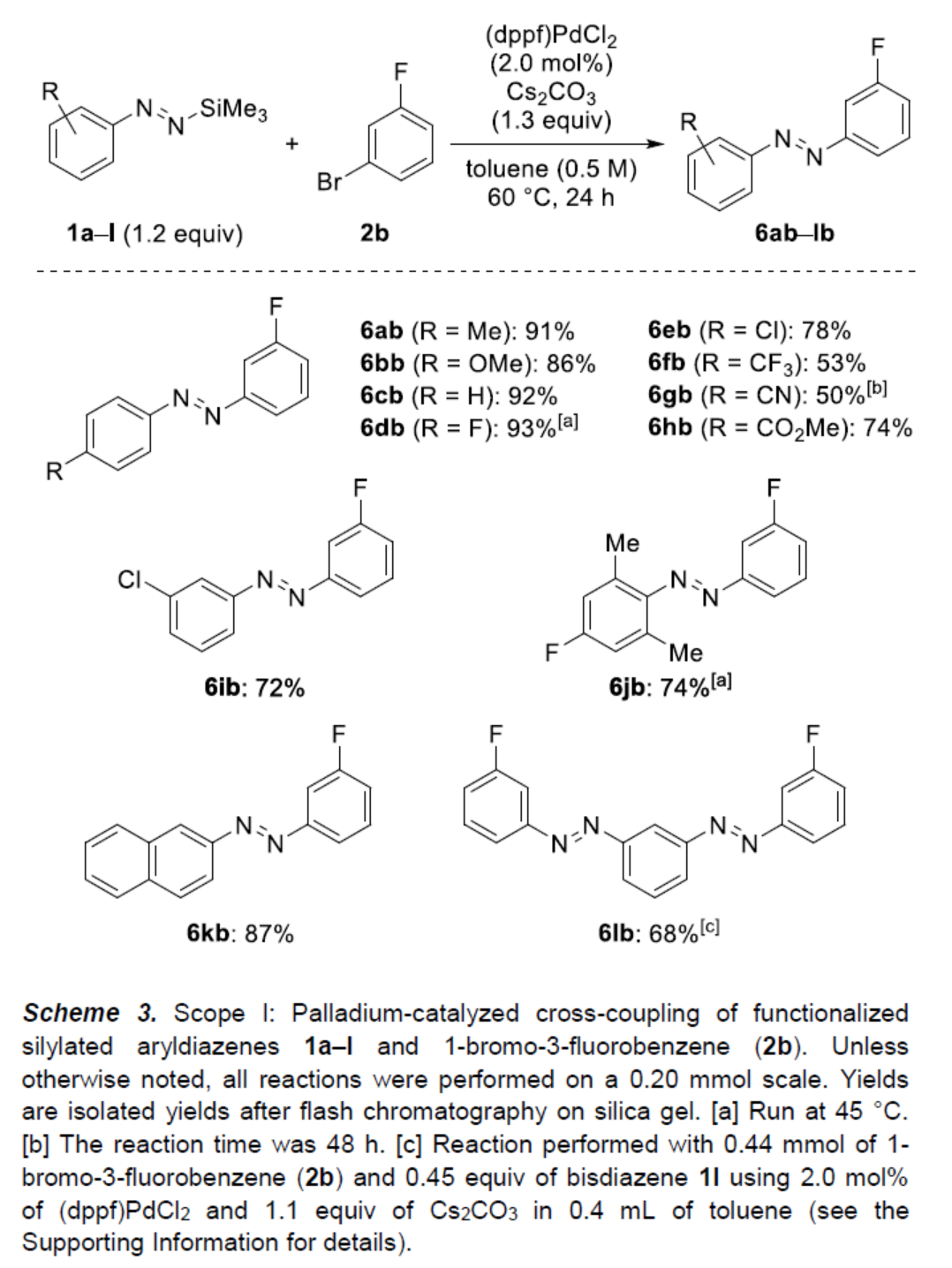
在获得上述最佳反应条件后,作者对N-芳基-N'-硅基二氮烯底物1的范围进行了扩展(Scheme 3)。首先,芳基上含有不同电性取代的底物,均可顺利与1-溴-3-氟苯(2b)反应,获得相应的产物6ab-6jb,收率为50-93%。然而,间硝基取代的二氮烯,在标准条件下未能发生反应。其次,N-萘基-N'-硅基二氮烯衍生物1k,也是合适的底物,可以87%的收率获得产物6kb。此外,1,3-双二氮烯衍生物1l,也能够顺利进行反应,可以68%的收率获得双偶联产物6lb。
(图片来源:Angew. Chem. Int. Ed.)
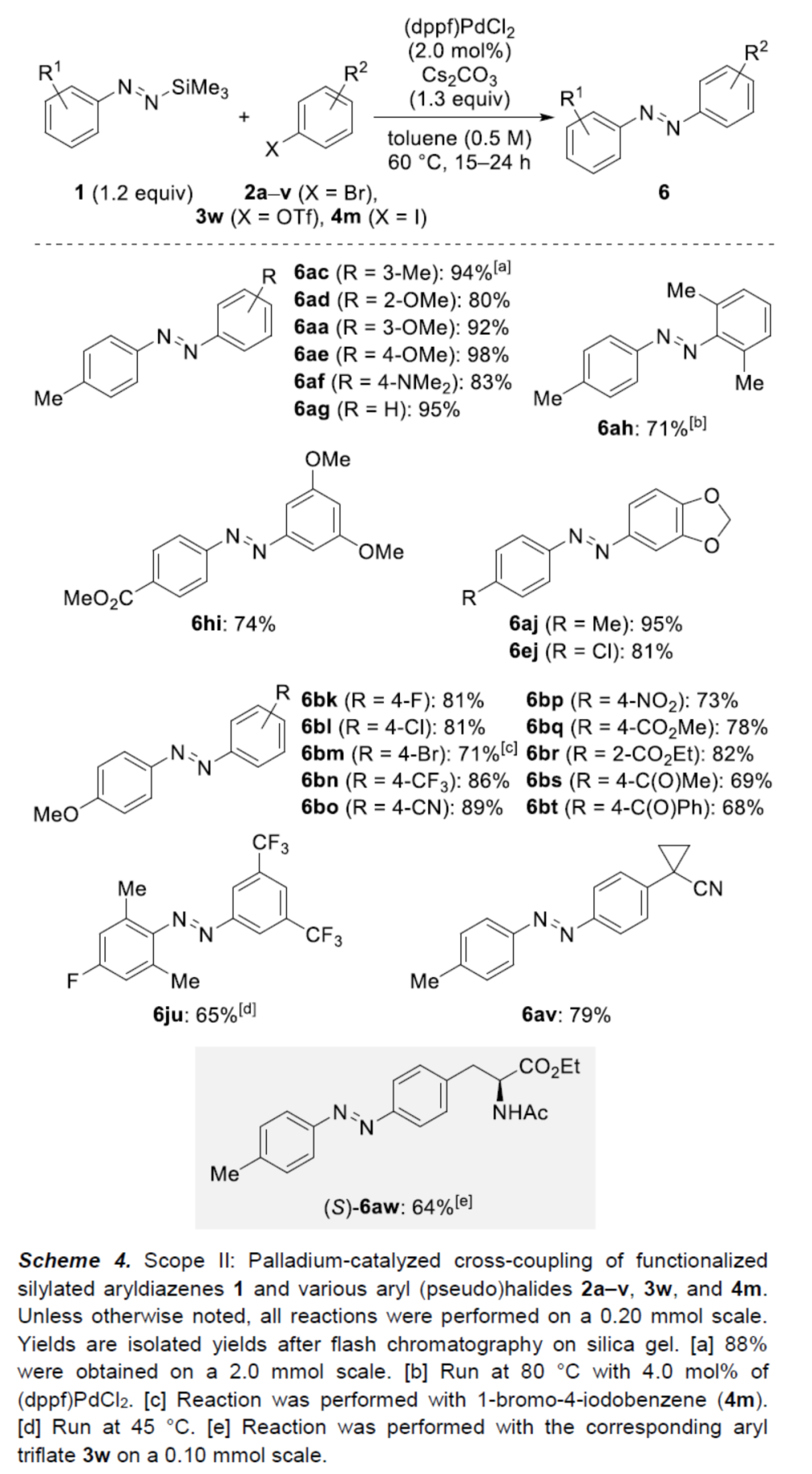
紧接着,作者对芳基卤的底物范围进行了扩展(Scheme 4)。首先,一系列具有不同电性取代的芳基溴底物,均可顺利与1反应,获得相应的产物6aa、6ac-6ah、6hi、6aj、6ej、6bk-6bl、6bn-6bt、6ju和6av,收率为65-95%。其次, 1-溴-4-碘苯4m,也是合适的底物,且反应优先选择碘取代基进行偶联,可以71%收率的获得产物6bm。然而,当使用二溴苯2m作为底物时,则获得较为复杂的混合物。此外,衍生自酪氨酸的芳基三氟甲磺酸酯3w,可以64%的收率获得相应的偶氮苯产物(S)-6aw。值得注意的是,该反应具有良好的官能团兼容性。
(图片来源:Angew. Chem. Int. Ed.)
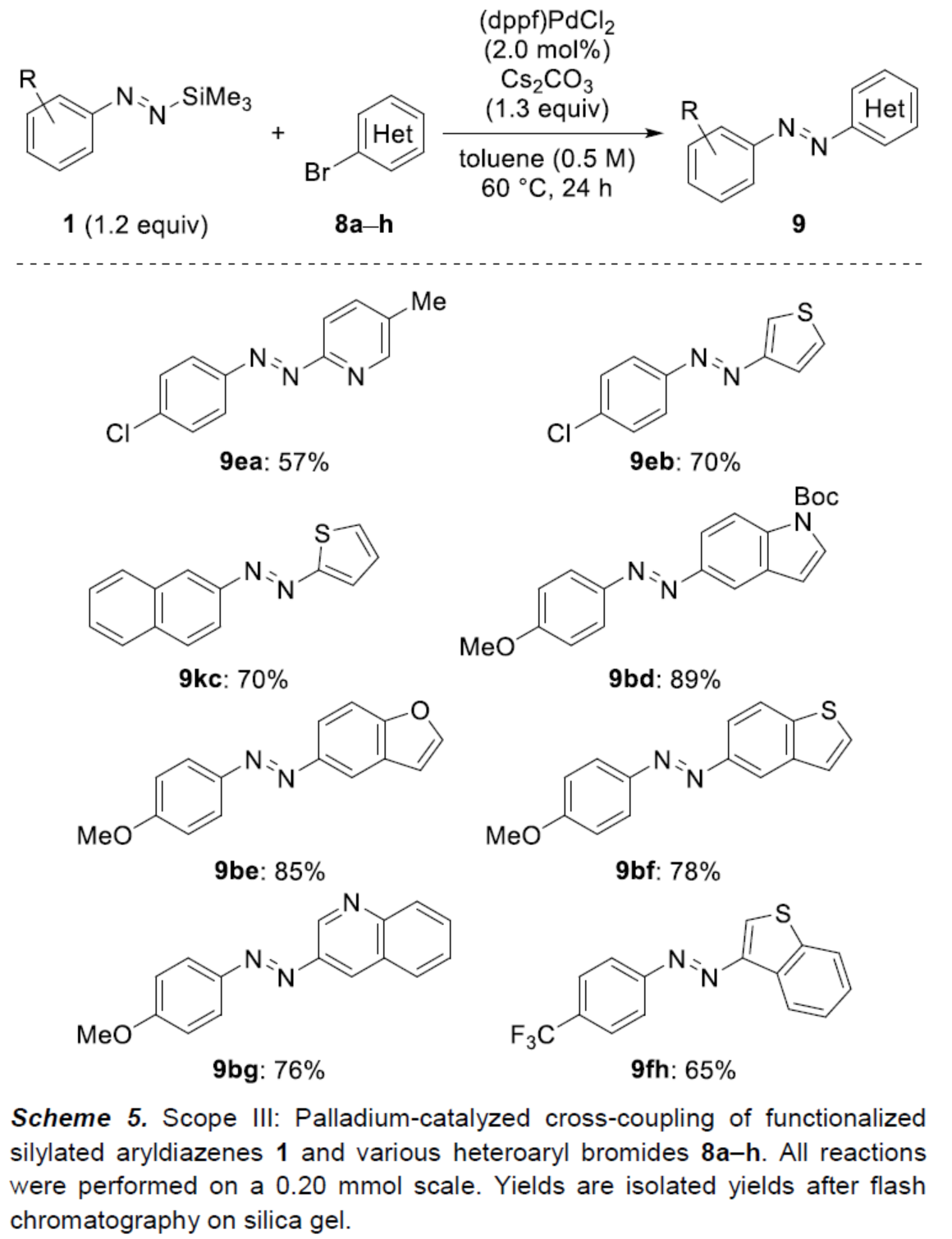
随后,作者对杂芳基溴的底物范围进行了扩展(Scheme 5)。研究表明,含有吡啶基、噻吩基、吲哚基、苯并呋喃基、苯并噻吩基和喹啉基溴化物,均可顺利与1反应,获得相应的产物9ea、9eb、9kc、9bd-9bg和9fh,收率为57-89%。
(图片来源:Angew. Chem. Int. Ed.)
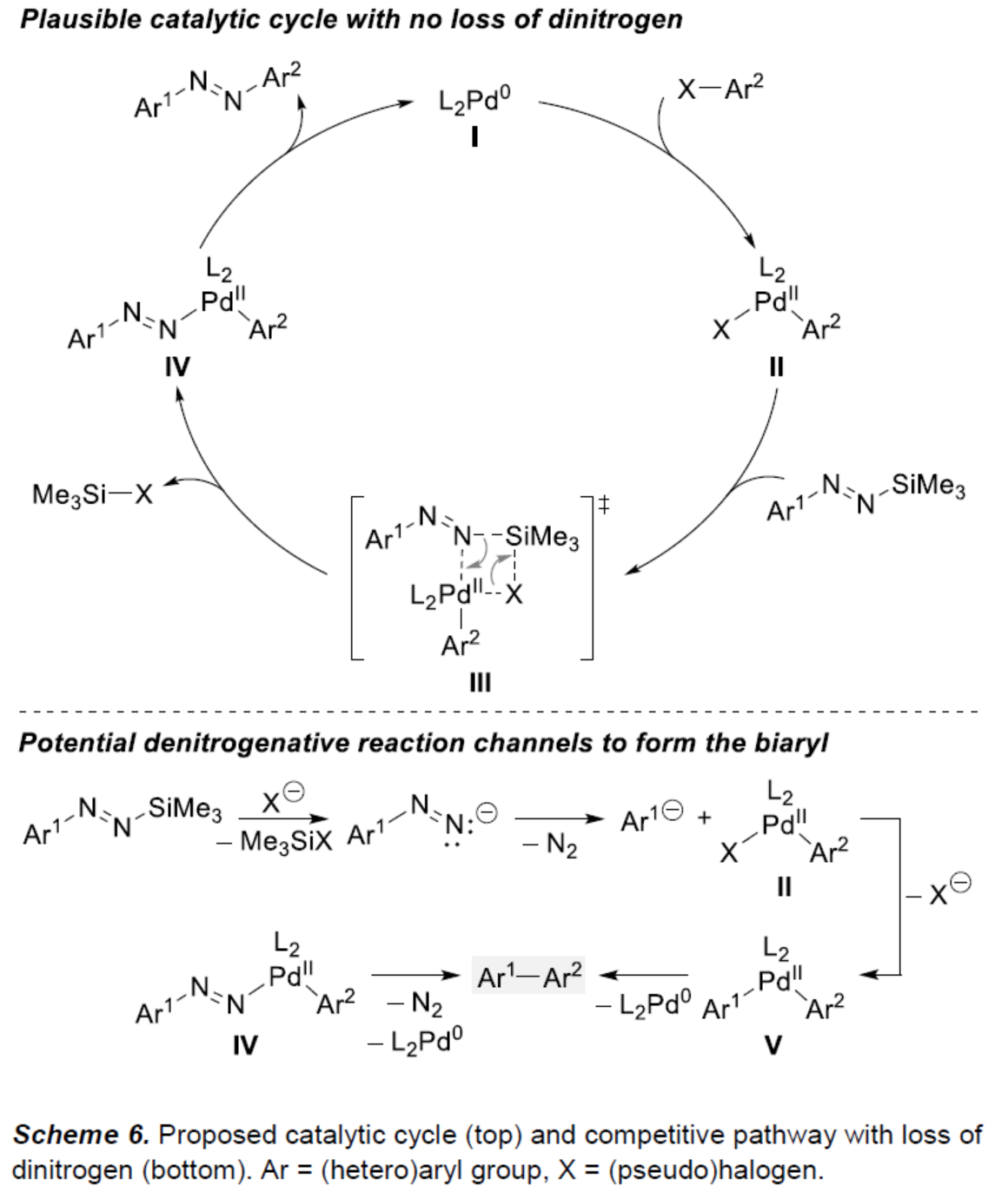
最后,作者提出了一种合理的催化循环过程(Scheme 6)。首先,L2Pd0(I)与X-Ar2进行氧化加成,生成芳基钯(II)卤化物II。虽然Hünig和Kosower课题组研究表明叔丁基取代的二氮烯基阴离子可加成至羰基化合物中,但作者认为转金属化并不涉及“游离”的二氮烯基阴离子。相反,钯(II)中间体II可与二氮烯基阴离子进行σ-键复分解,生成过渡态III。随后,过渡态III释放Me3Si-X,生成芳基(二氮烯基)钯(II)配合物IV。配合物IV经还原消除,可获得非对称的偶氮芳烃以及L2Pd0(I),从而完成了催化循环的过程。此外,氮气的释放既不会发生在中间体IV阶段,也不会发生在转金属化之前,即III。这两种途径都会通过相应的二芳基钯(II)V,生成不需要的联芳基副产物。值得注意的是,碱的存在是至关重要的,结果证明Cs2CO3是最佳的。
(图片来源:Angew. Chem. Int. Ed.)
总结:
柏林工业大学Martin Oestreich课题组报道了一种高效的钯催化二氮烯基阴离子等价物与(杂)芳基(拟)卤化物的交叉偶联反应,合成了一系列非对称偶氮苯衍生物。同时,该策略无需要使用过量的偶联底物,通常仅需1.2当量的二氮烯亲核试剂。此外,该反应具有底物范围广泛、官能团兼容性良好、反应条件温和等特点。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn