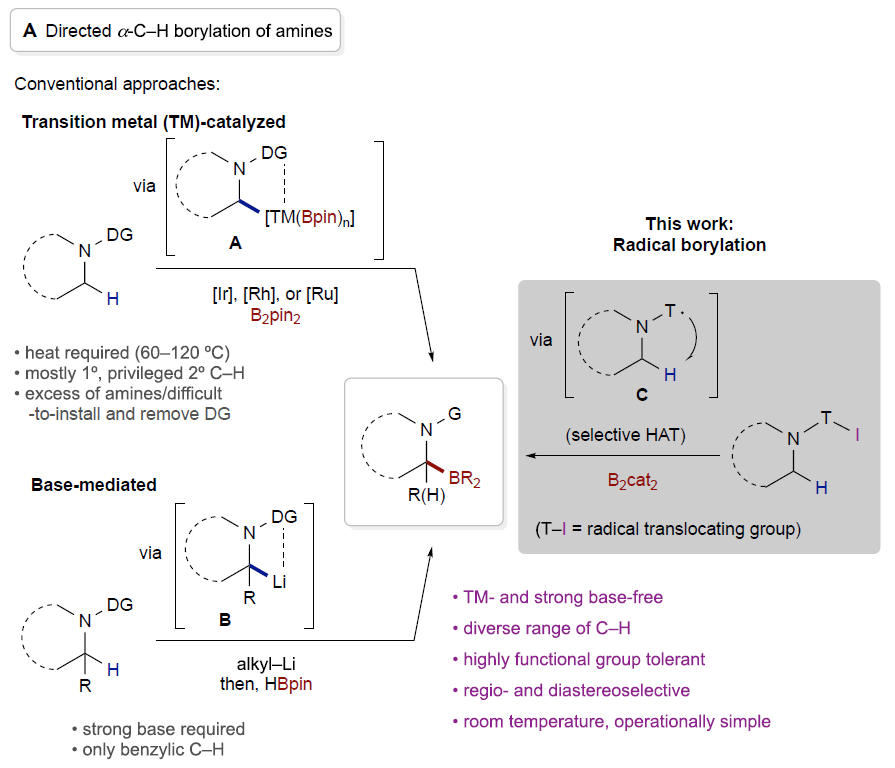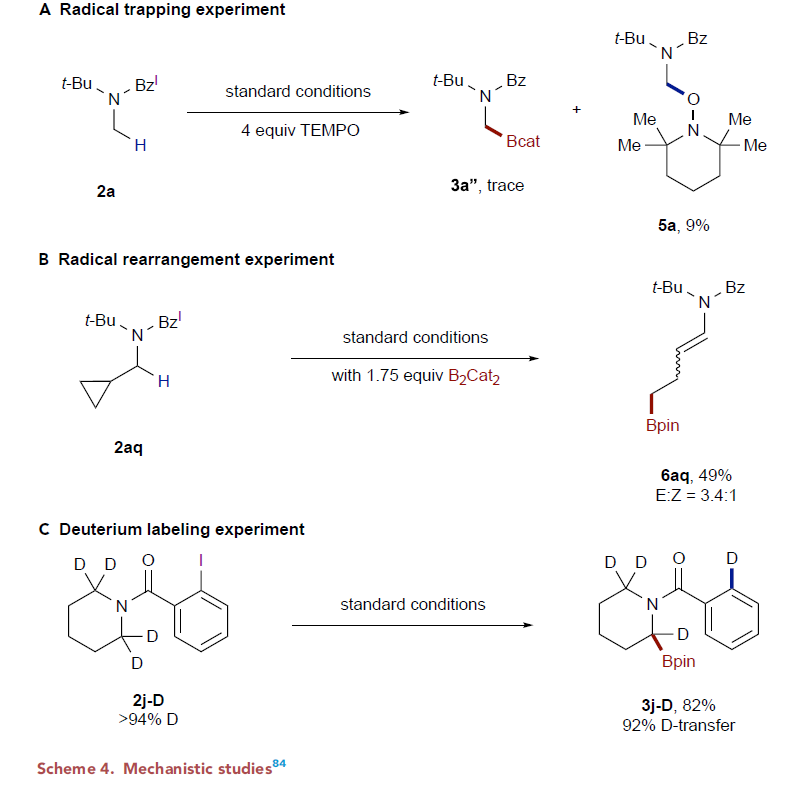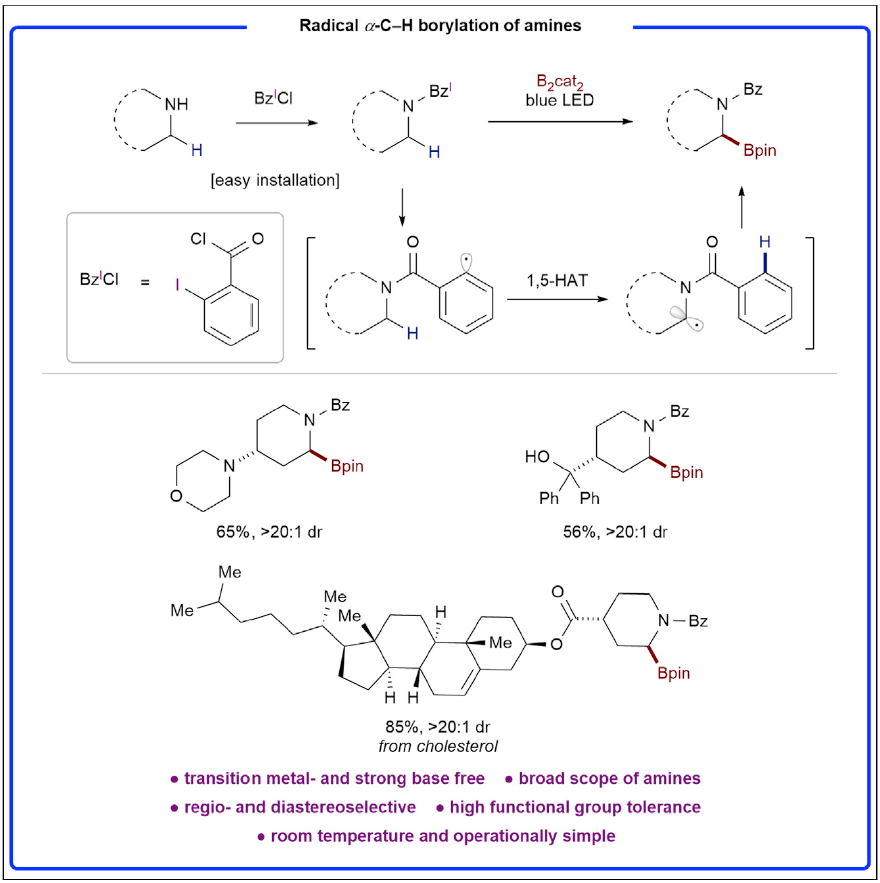
硼酸是有机合成、材料科学和药物研发中极其重要的官能团(Figure 1)。其可以通过过渡金属催化的偶联反应实现更为复杂分子结构的构建。此外,由于α-氨基硼骨架可以作为氨基酸的生物电子等排体,其广泛应用在药物研发中。而传统的α-氨基硼合成方法需要对起始原料进行预官能团化并需要经历多步合成。因此,利用简单易得的胺实现其α-C-H硼化则具有较大的优势,尽管此领域最近取得了一定的进展,但直接实现胺的α-C-H硼化过程较少,且大多数仅能得到端位或β-位硼化产物。已发展出的策略包括过渡金属催化的导向C-H活化过程和强碱条件下的去质子化过程,且这两种策略均包含碳金属中间体(A, B, Scheme 1A)。在过渡金属催化的C-H活化过程中通常使用胺作为反应试剂或者导向基团的安装或脱除较为困难。此外,官能团化的位置通常仅局限于端位或者活化的二级碳位点。在去质子化过程中通常需要强碱来实现去质子,且仅仅可以实现三级苄位的α-N-硼化过程。因此,发展一种条件温和、操作简单且通用的C-H硼化方法具有重要的意义。最近,德克萨斯大学达拉斯分校Vladimir Gevorgyan课题组发展了通用的脂肪胺α-C(sp3)-H硼化方法,高区域选择性和非对映选择性的实现了具有重要应用价值的α-氨基硼骨架的合成。此反应条件温和,且不需要使用过渡金属和强碱。作者使用商业可得且容易安装和脱除的2-碘苯甲酰基(BzI)作为导向基(DG),在光诱导下发生单电子还原后在DG上形成芳基自由基中间体D。随后在近端的C(sp3)-H处通过1,5-HAT即可得到关键的α-氨基烷基自由基中间体E后实现硼化过程,从而避免了过渡金属和强碱的使用。此外,过渡金属催化的C-H活化过程通常倾向于活化一级碳位点,而自由基途径通常倾向于活化较弱的C-H键,因此利用此反应可以实现烷基二级C-H键位点的硼化过程。实现这一过程所面临的主要挑战包括:1)芳基自由基中间体D直接硼化;2)α-氨基烷基自由基中间体E发生环化或消除;3)中间体D或E的直接质子化(Scheme 1B)。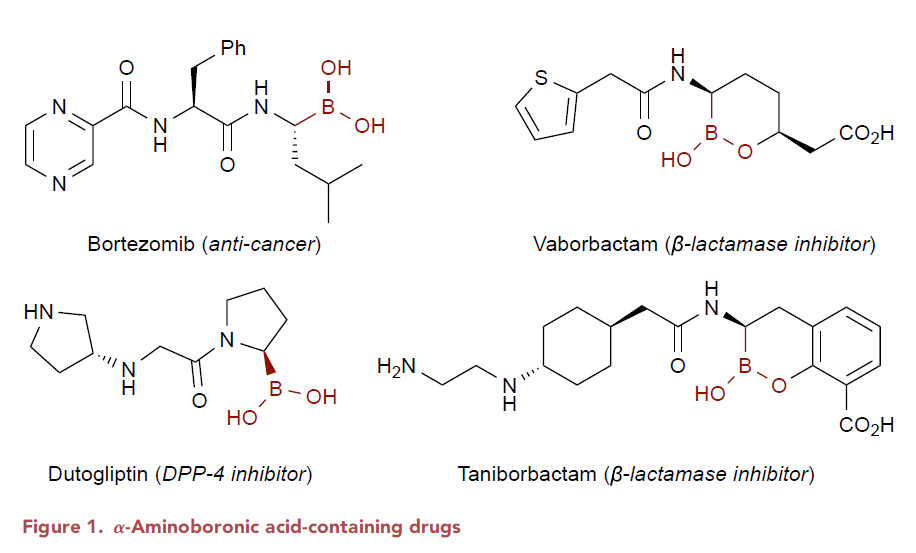 作者首先使用2-碘苯甲酰基保护的二丁基胺2c作为模板底物进行条件筛选,发现当使用 B2cat2 (3.5 equiv), Et3N (4.0 equiv), DMA (0.1 M)作溶剂,427 nm LED引发,室温下反应48小时后通过转酯化可以以80%的分离产率得到产物3(Figure 2, entry 1)。此外,作者还对不同的导向基进行了筛选,发现2-碘苯甲酰基为最优导向基(Figure 2, entries 7-11)。随后,作者对此自由基C(sp3)-H硼化反应的底物范围进行探索(Figure 3)。实验结果表明此转化具有良好的官能团兼容性和底物适用性。不同大小(6-8元环)的氮杂环均可参与转化,以61-82%的产率得到产物3j-3l。具有不同敏感官能团的氮杂环,包括醚(3m)、硫醚(3r)、砜(3s)、卤素(3t, 3u, 3x)、非保护的胺(3p)、非保护的醇(3q)、酰胺(3ac, 3ad)、磺酰胺(3ag, 3ah)、氨基甲酸酯(3ae)等也可兼容此转化。此外,作者观察到二级碳更优先发生此类C-H硼化过程(3ak)。对于复杂分子结构,如血清素拮抗剂LY426965(3ai)、meclizine(3aj)、estrone(3al)、cholesterol(3am)、ibuprofen(3an)等活性骨架也可以兼容此体系。值得注意的是,利用此方法,除了可以得到频哪醇硼酯产物外,还可以以中等的产率得到儿茶酚硼酯产物3ja和二氟化硼官能团化产物3jb。此外,利用3ja的转酯化过程还可以实现丙二醇硼酯3jc和蒎烷二醇硼酯3jd等其它硼酯产物的合成。利用此方法得到的产物(3c, 3j, 3m, α-选择性)可以和Hartwig课题组直接硼化方法(Science, 2020, 368, 736; J. Am. Chem. Soc. 2012, 134, 12422)得到的产物(3c’, 非环状胺:端位选择性;3j’, 3m’, 环状胺:β-选择性)形成互补的区域选择性(Scheme 2)。接下来,作者将此反应放大至1.0 mmol产率并未受影响(3a, 3j, 3t)。值得注意的是,当使用2v作为起始原料,并放大至35 mmol规模反应,仍可以以41%(0.2 mmol规模时产率为45%)的产率得到产物3v(Scheme 3A)。之后,作者进行了产物的衍生实验(Scheme 3B)。利用合成出的产物3a-3c可以通过Suzuki偶联实现芳基化产物的合成(4a-4c)。此外,利用Matteson同系化反应可以实现β-胺基硼4d的合成。而4d又可以进一步发生转化得到β-胺基醇衍生物4e和官能团化γ-胺基硼4f。最后,作者在温和条件下实现了产物的脱保护过程,并可以兼容多种官能团(Scheme 3C)。上述实验表明了此反应具有良好的实用性和应用性。 为了对反应有更深入的了解,作者进行了一系列控制实验。首先,自由基捕获实验(Scheme 4A)和自由基重排实验(Scheme 4B)均表明反应包含自由基中间体。随后作者通过氘代标记实验中完全的氘原子转移(2j-D→3j-D)进一步证实了选择性1,5-HAT过程的存在(Scheme 4C)。而开关灯实验结果和获得的量子产率值(2.6)表明反应可能包含自由基链式反应机理。 基于上述实验结果和文献报道,作者提出了可能的反应机理:首先2与F络合在光照下得到F*。随后F*与2发生单电子转移,使C-I键发生均裂得到亲电性的芳基自由基物种D。接着D通过1,5-HAT得到亲核性的α-氨基烷基自由基中间体E后与B2cat2发生自由基加成得到硼化产物G和硼自由基H。而硼自由基中间体H又可以与2通过卤原子转移或单电子转移机理实现自由基链传递过程。硼化产物G又可以通过转酯化过程得到最终频哪醇硼酯产物3。值得注意的是,氮原子上的苯甲酰基导向基对此反应起到了至关重要的作用:1)其提供了足够的Thorpe-Ingold效应;2)其为通过1,5-HAT生成亲核的α-氨基烷基自由基过程提供了有效的极性匹配;3)其可以有效抑制α-氨基烷基自由基生成去饱和副产物(3-B),从而有利于被二硼试剂捕获。
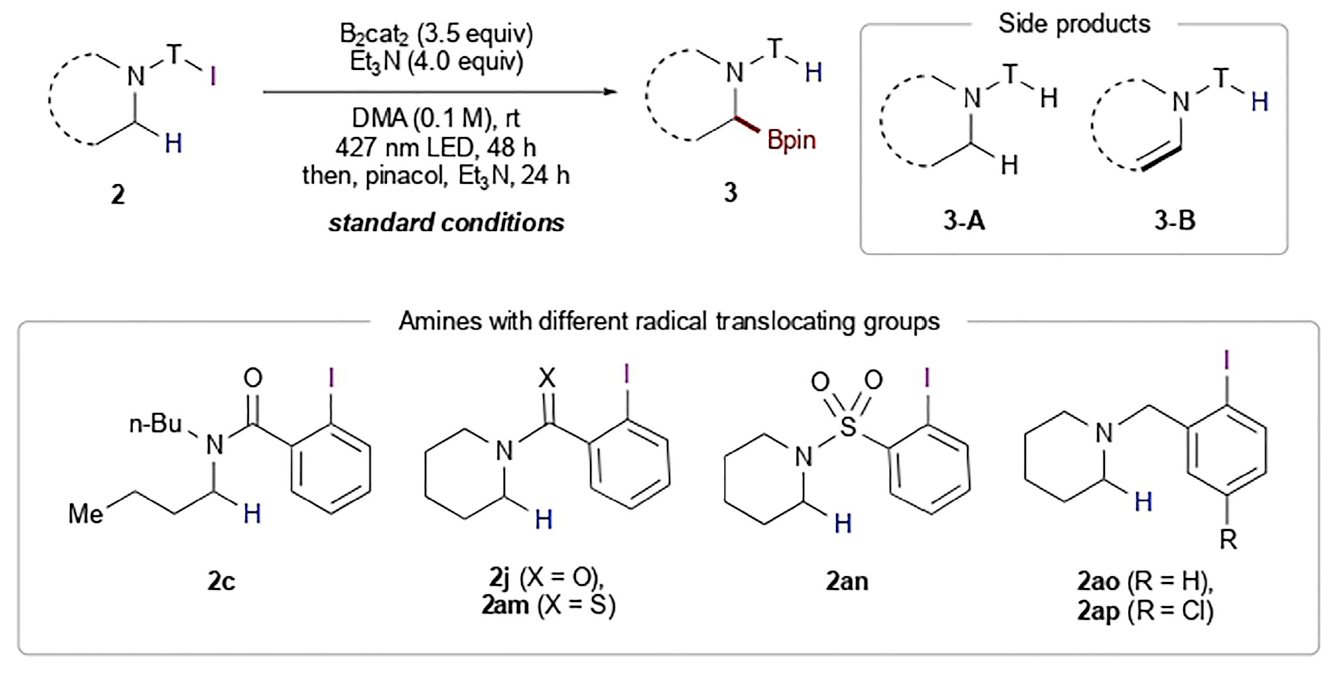
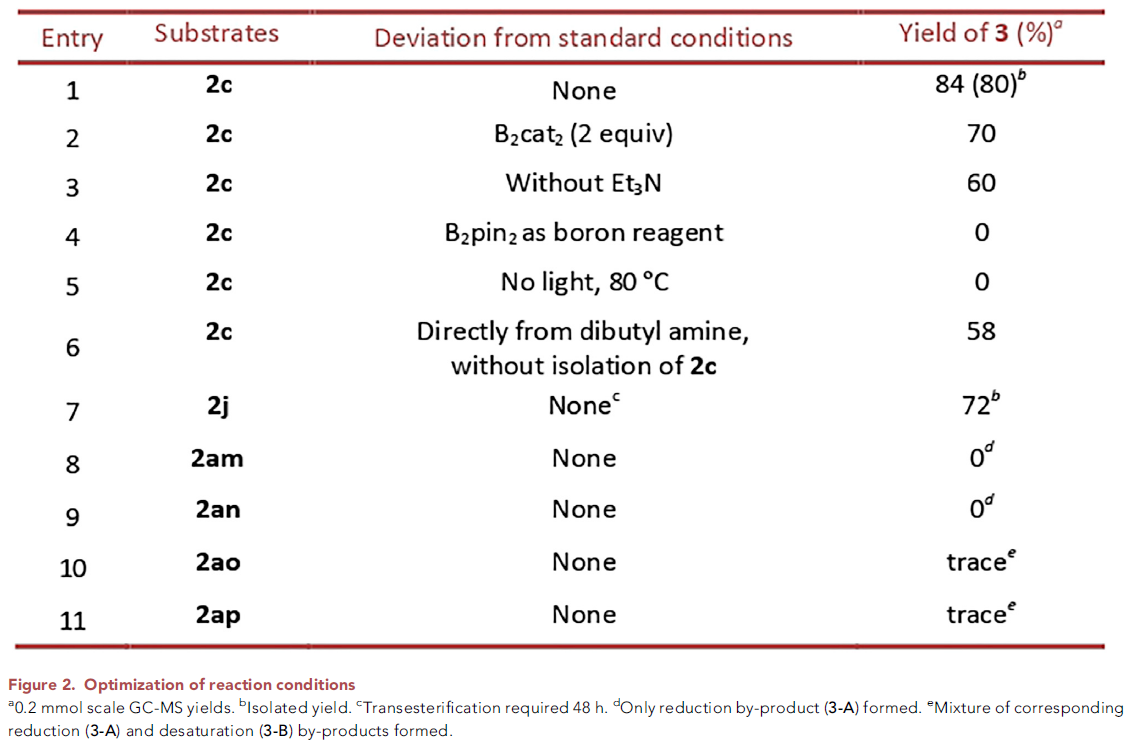
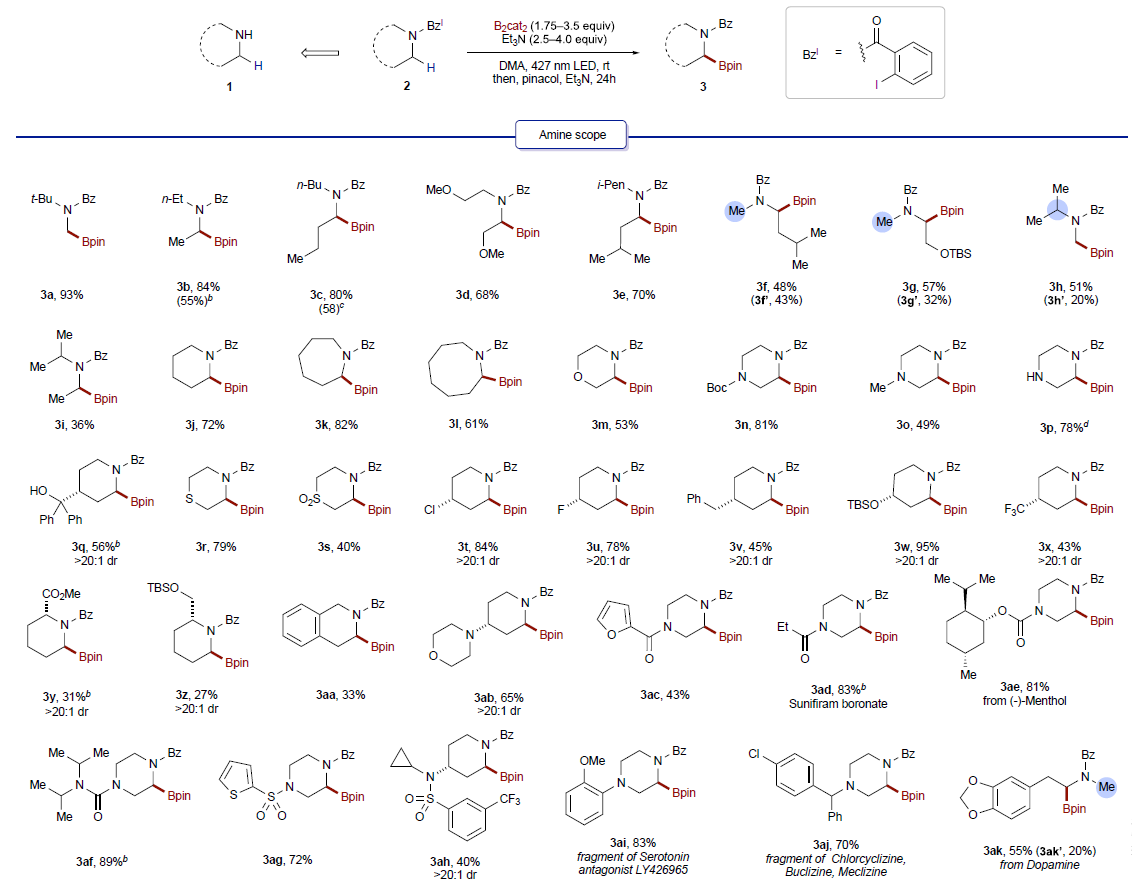
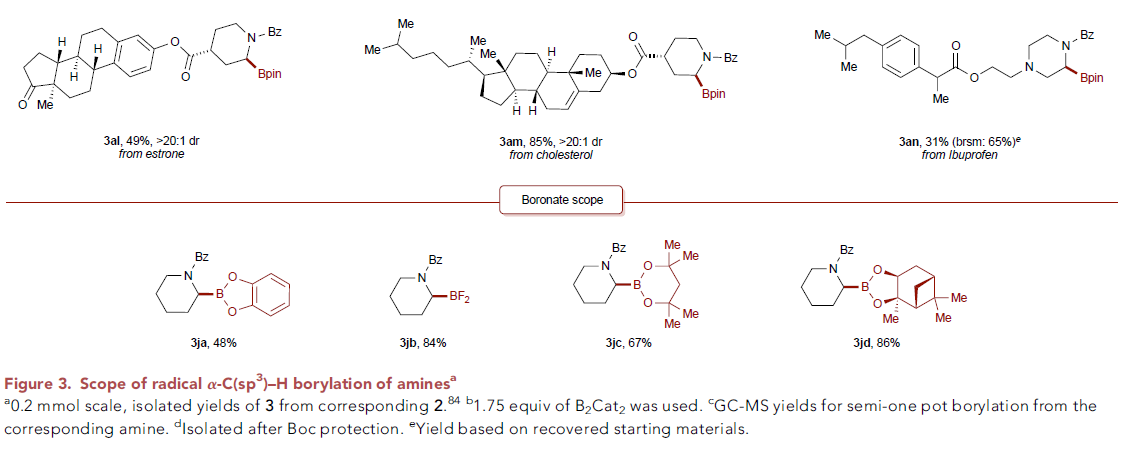
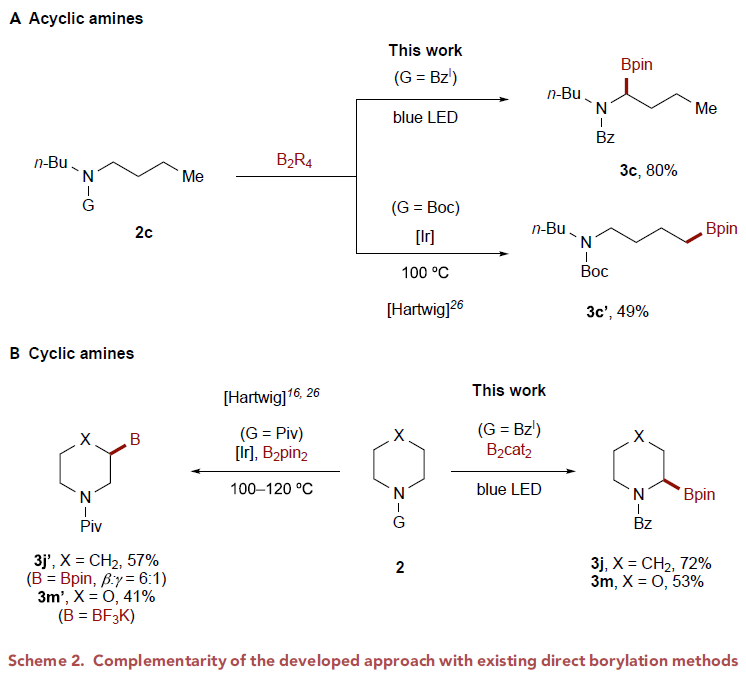
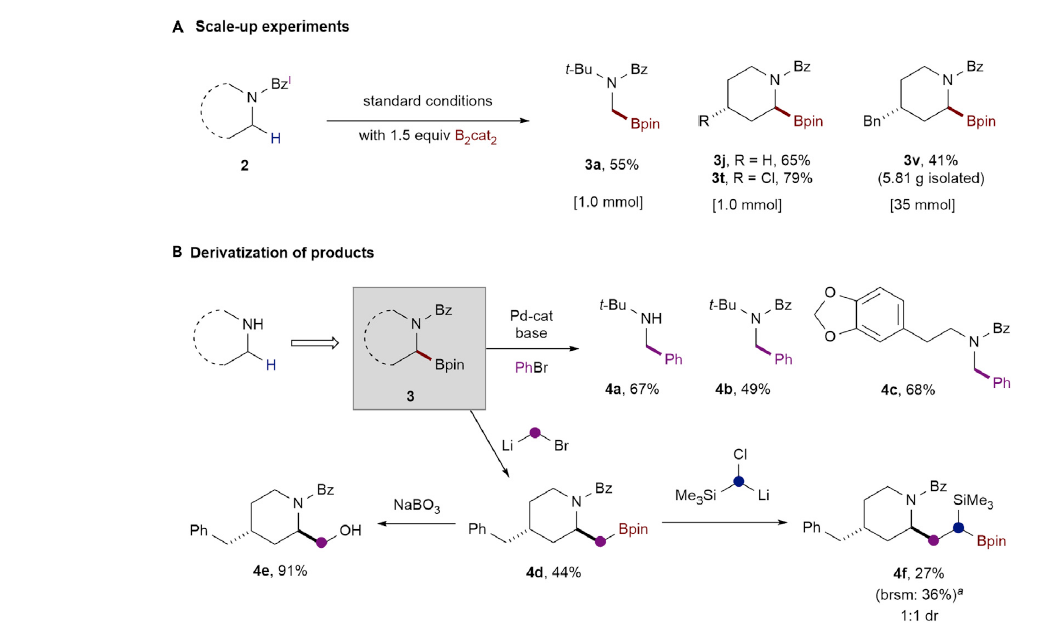
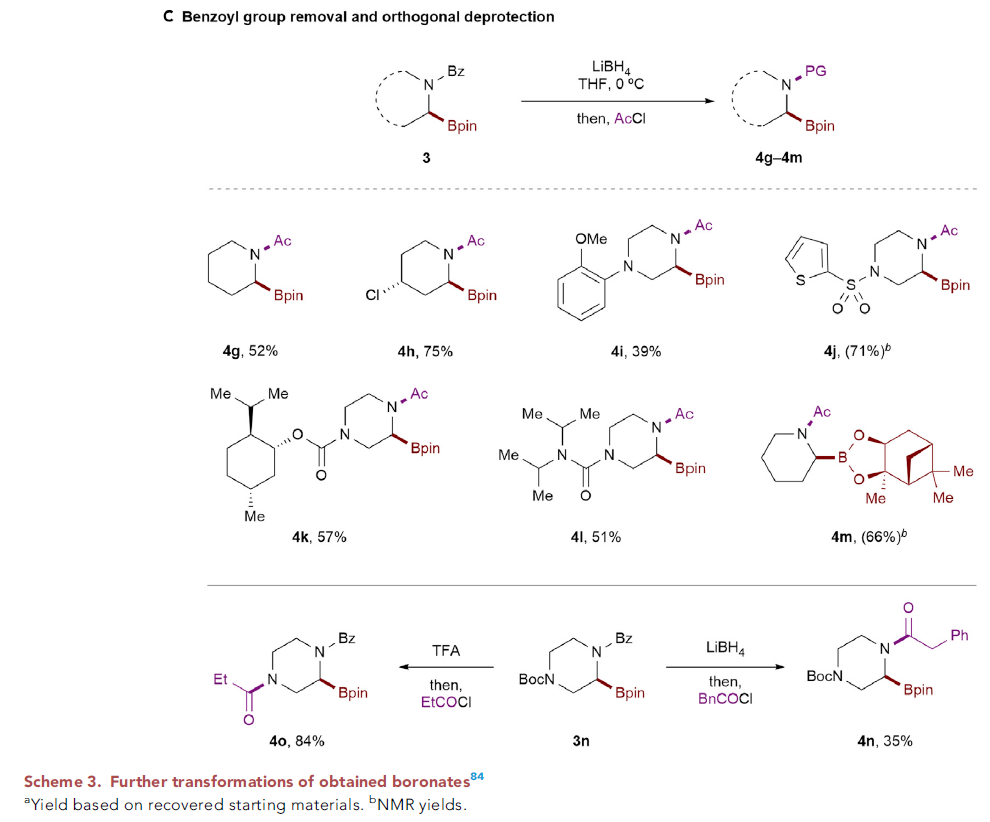
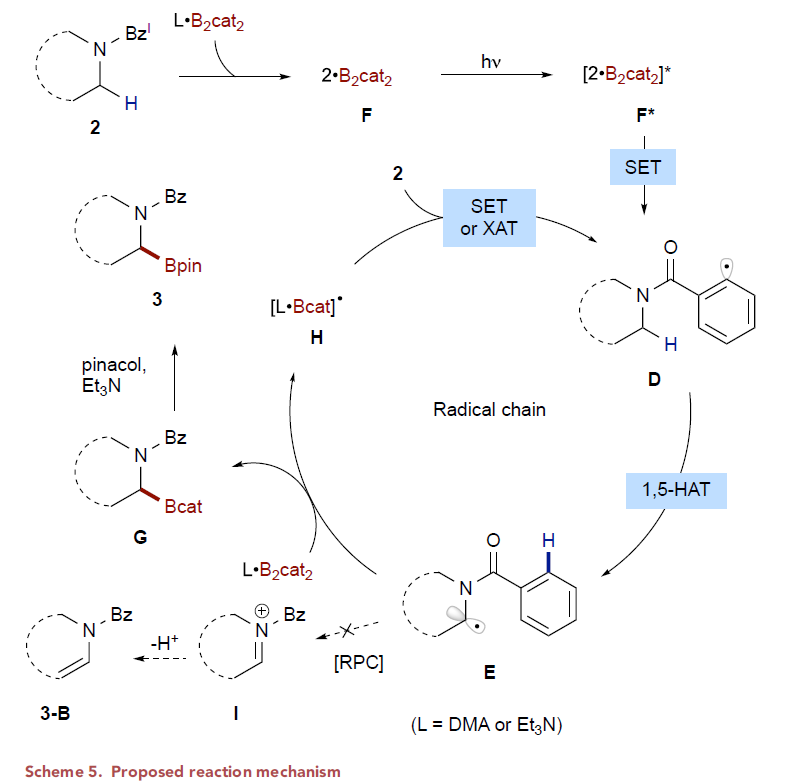
作者首先使用2-碘苯甲酰基保护的二丁基胺2c作为模板底物进行条件筛选,发现当使用 B2cat2 (3.5 equiv), Et3N (4.0 equiv), DMA (0.1 M)作溶剂,427 nm LED引发,室温下反应48小时后通过转酯化可以以80%的分离产率得到产物3(Figure 2, entry 1)。此外,作者还对不同的导向基进行了筛选,发现2-碘苯甲酰基为最优导向基(Figure 2, entries 7-11)。随后,作者对此自由基C(sp3)-H硼化反应的底物范围进行探索(Figure 3)。实验结果表明此转化具有良好的官能团兼容性和底物适用性。不同大小(6-8元环)的氮杂环均可参与转化,以61-82%的产率得到产物3j-3l。具有不同敏感官能团的氮杂环,包括醚(3m)、硫醚(3r)、砜(3s)、卤素(3t, 3u, 3x)、非保护的胺(3p)、非保护的醇(3q)、酰胺(3ac, 3ad)、磺酰胺(3ag, 3ah)、氨基甲酸酯(3ae)等也可兼容此转化。此外,作者观察到二级碳更优先发生此类C-H硼化过程(3ak)。对于复杂分子结构,如血清素拮抗剂LY426965(3ai)、meclizine(3aj)、estrone(3al)、cholesterol(3am)、ibuprofen(3an)等活性骨架也可以兼容此体系。值得注意的是,利用此方法,除了可以得到频哪醇硼酯产物外,还可以以中等的产率得到儿茶酚硼酯产物3ja和二氟化硼官能团化产物3jb。此外,利用3ja的转酯化过程还可以实现丙二醇硼酯3jc和蒎烷二醇硼酯3jd等其它硼酯产物的合成。利用此方法得到的产物(3c, 3j, 3m, α-选择性)可以和Hartwig课题组直接硼化方法(Science, 2020, 368, 736; J. Am. Chem. Soc. 2012, 134, 12422)得到的产物(3c’, 非环状胺:端位选择性;3j’, 3m’, 环状胺:β-选择性)形成互补的区域选择性(Scheme 2)。接下来,作者将此反应放大至1.0 mmol产率并未受影响(3a, 3j, 3t)。值得注意的是,当使用2v作为起始原料,并放大至35 mmol规模反应,仍可以以41%(0.2 mmol规模时产率为45%)的产率得到产物3v(Scheme 3A)。之后,作者进行了产物的衍生实验(Scheme 3B)。利用合成出的产物3a-3c可以通过Suzuki偶联实现芳基化产物的合成(4a-4c)。此外,利用Matteson同系化反应可以实现β-胺基硼4d的合成。而4d又可以进一步发生转化得到β-胺基醇衍生物4e和官能团化γ-胺基硼4f。最后,作者在温和条件下实现了产物的脱保护过程,并可以兼容多种官能团(Scheme 3C)。上述实验表明了此反应具有良好的实用性和应用性。 为了对反应有更深入的了解,作者进行了一系列控制实验。首先,自由基捕获实验(Scheme 4A)和自由基重排实验(Scheme 4B)均表明反应包含自由基中间体。随后作者通过氘代标记实验中完全的氘原子转移(2j-D→3j-D)进一步证实了选择性1,5-HAT过程的存在(Scheme 4C)。而开关灯实验结果和获得的量子产率值(2.6)表明反应可能包含自由基链式反应机理。 基于上述实验结果和文献报道,作者提出了可能的反应机理:首先2与F络合在光照下得到F*。随后F*与2发生单电子转移,使C-I键发生均裂得到亲电性的芳基自由基物种D。接着D通过1,5-HAT得到亲核性的α-氨基烷基自由基中间体E后与B2cat2发生自由基加成得到硼化产物G和硼自由基H。而硼自由基中间体H又可以与2通过卤原子转移或单电子转移机理实现自由基链传递过程。硼化产物G又可以通过转酯化过程得到最终频哪醇硼酯产物3。值得注意的是,氮原子上的苯甲酰基导向基对此反应起到了至关重要的作用:1)其提供了足够的Thorpe-Ingold效应;2)其为通过1,5-HAT生成亲核的α-氨基烷基自由基过程提供了有效的极性匹配;3)其可以有效抑制α-氨基烷基自由基生成去饱和副产物(3-B),从而有利于被二硼试剂捕获。德克萨斯大学达拉斯分校Vladimir Gevorgyan课题组发展了通用的脂肪胺α-C(sp3)-H硼化方法,高区域选择性和非对映选择性的实现了具有重要应用价值的α-氨基硼骨架的合成。此反应条件温和,且不需要使用过渡金属和强碱。反应对敏感基团和复杂生物活性分子具有良好的兼容性。克级规模实验和产物的衍生化实验表明反应具有良好的应用性。此反应的发展为脂肪胺的α-C(sp3)-H硼化过程提供了新的思路。