

(图片来源:J. Am. Chem. Soc.)
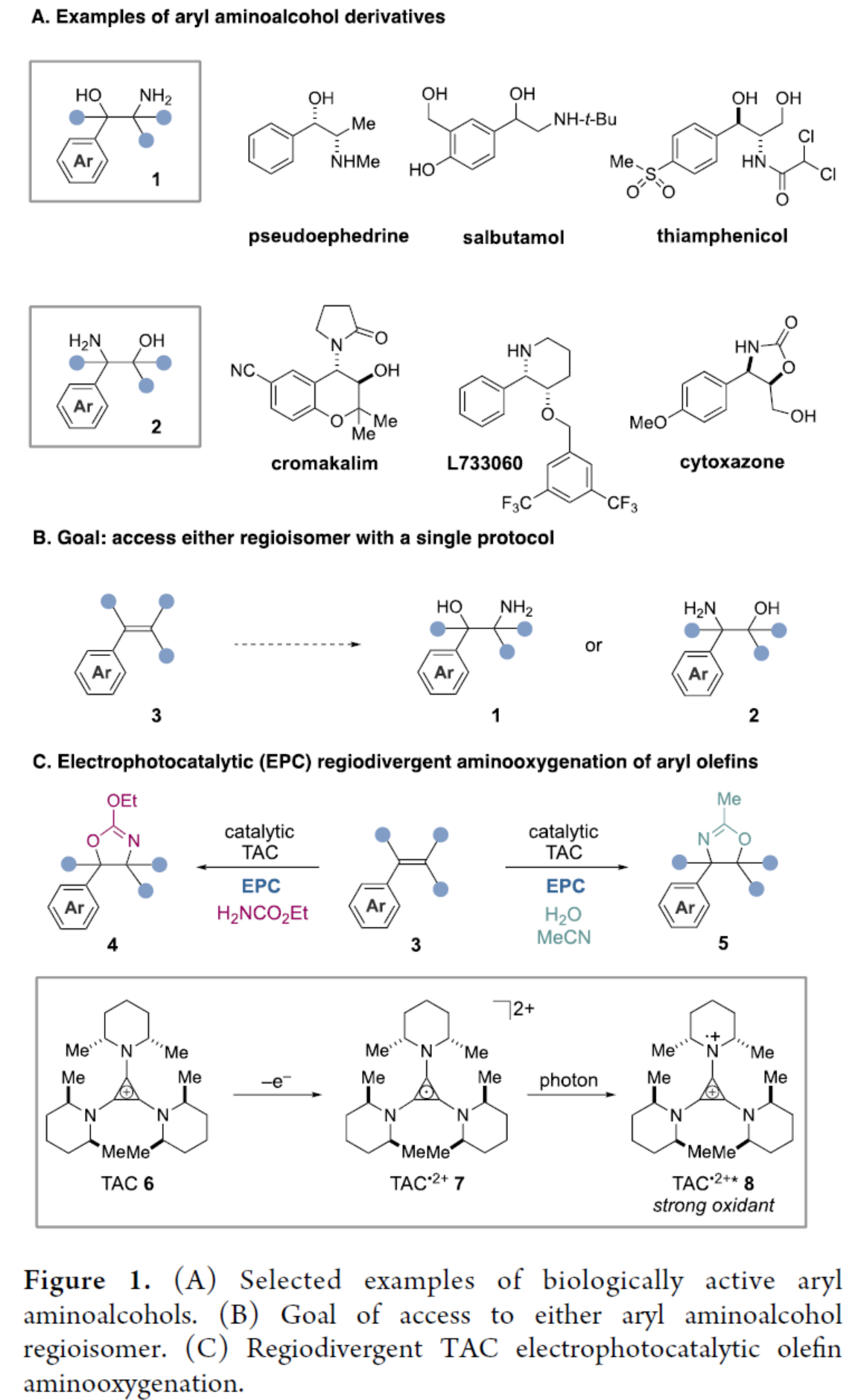
芳基取代的1,2-氨基醇广泛存在于各种复杂生物活性分子、天然产物、手性助剂、金属催化配体等中(Figure 1A)。烯烃的直接氨氧合反应是构建此类化合物最为有用的模块化方法之一,同时化学家们还开发了多种实现此类转化的方法。在Sharpless课题组报道使用锇催化的开创性例子以来,化学家们还将催化剂的种类扩展到其它的过渡金属催化剂。此外,化学家们也开发了一些非过渡金属试剂或催化剂的方法。然而,大多数方法均需使用化学计量的氧化剂,从而导致反应的环境、安全和成本问题。近年来,无需使用传统化学氧化剂的电化学方法是一种具有吸引力的可替代策略。虽然Moeller和徐海超课题组报道了电化学分子内烯烃的氨氧合反应,但对于分子间的氨氧合反应则更具挑战性。
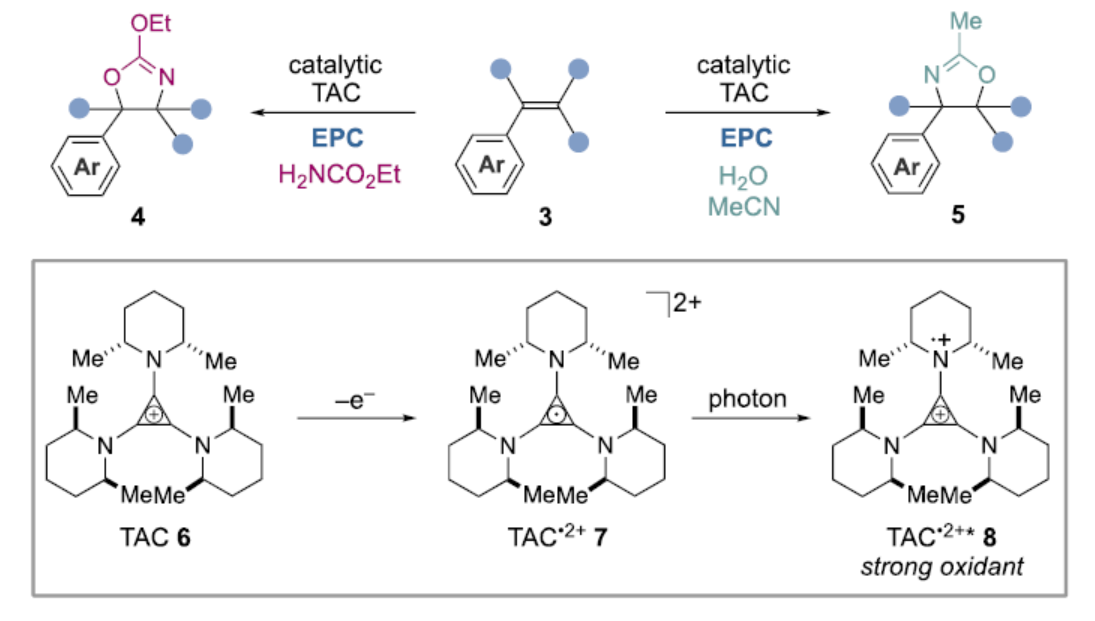
理论上,烯烃的直接电化学单电子氧化可实现烯烃分子间的氨氧合反应。然而,由于阳极生成的烯烃自由基阳离子容易自聚或氧化裂解,从而导致反应的选择性具有难度。为了解决此问题,2021年,雷爱文课题组利用原位生成亲电氯,通过氯离子形成,然后被酰胺反应物捕获,实现了噁唑啉衍生物的合成。然而,通过相同的底物3经区域发散性合成2-氨基-1-醇1或1-氨基-2-醇2衍生物则具有挑战(Figure 1B)。在开创性的研究中,Yoon课题组首先报道了一种催化剂控制策略,可选择性地从哑嗪试剂中获得相应的区域异构体产物。随后,Rovis课题组通过配体控制实现了铱催化烯烃分子内区域发散性氨氧化反应。最近,托莱多大学Li Wei课题组报道了一种碘催化分子间氨氧化策略,其中使用简单的碱或Lewis酸添加剂来控制区域选择性。近日,美国康奈尔大学Tristan H. Lambert课题组报道了一种光电催化芳基烯烃的区域发散性氨氧合反应。其中,仅需使用简单的氨基甲酸乙酯或水即可实现相应的区域选择性(Figure 1C)。在光电催化(EPC)策略中,涉及电化学和光化学能量的结合来催化反应。作者采用三氨基环丙烯(TAC)离子6作为电催化剂,通过电化学氧化生成自由基双阳离子7,随后通过光激发从而生成强氧化性配合物8。
(图片来源:J. Am. Chem. Soc.)
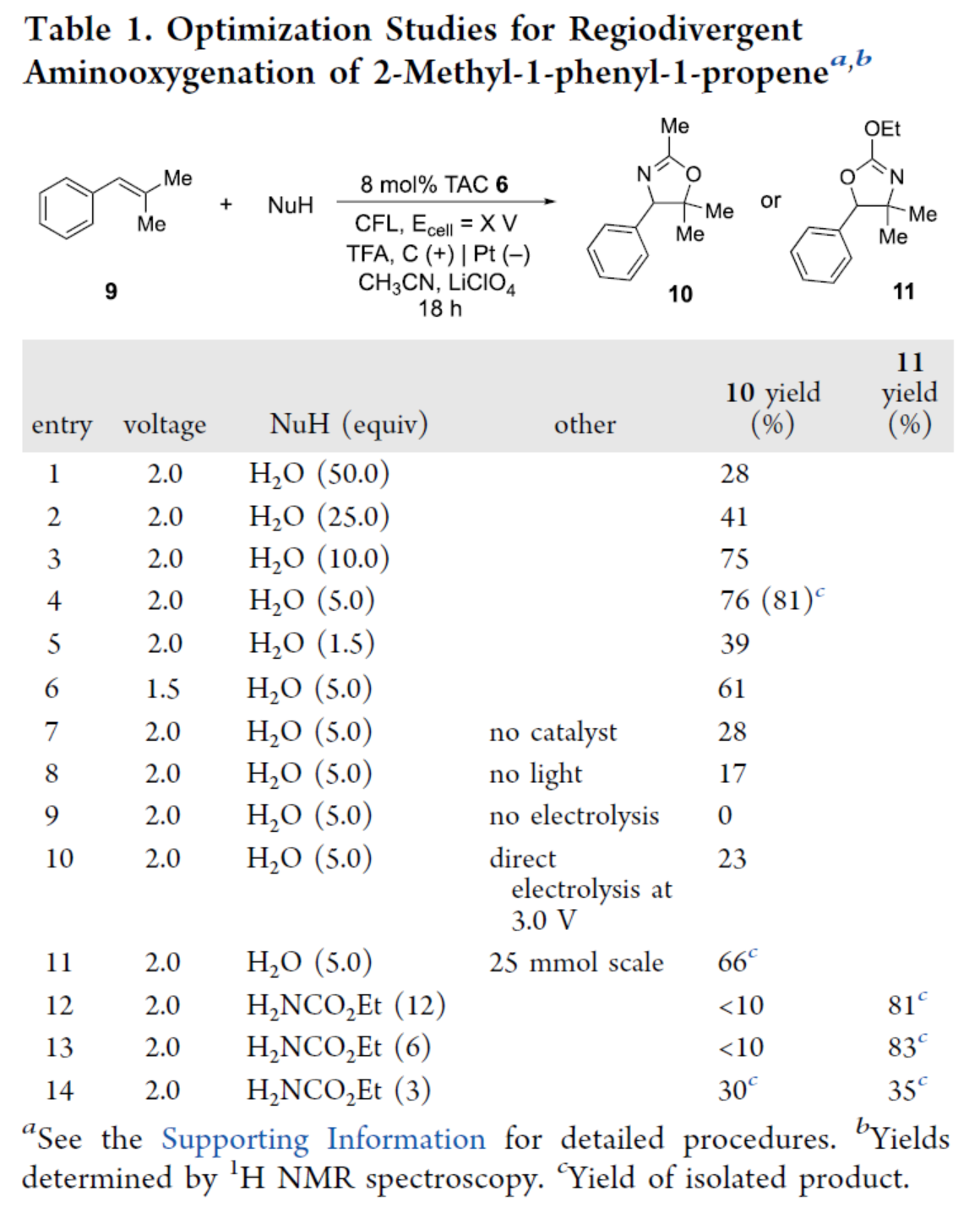
首先,作者以2-甲基-1-苯基-1-丙烯9作为模型底物,进行了相关反应条件的筛选(Table 1)。当以TAC 6作为催化剂,TFA作为添加剂,LiClO4作为电解质,碳阴极/铂阳极作为电极,CFL灯泡作为可见光源,乙腈作为溶剂,Ecell为2.0 V时,当以H2O作为亲核试剂,可以76%的收率得到产物10。当以H2NCO2Et作为亲核试剂,可以83%的收率得到区域异构体产物11。
(图片来源:J. Am. Chem. Soc.)
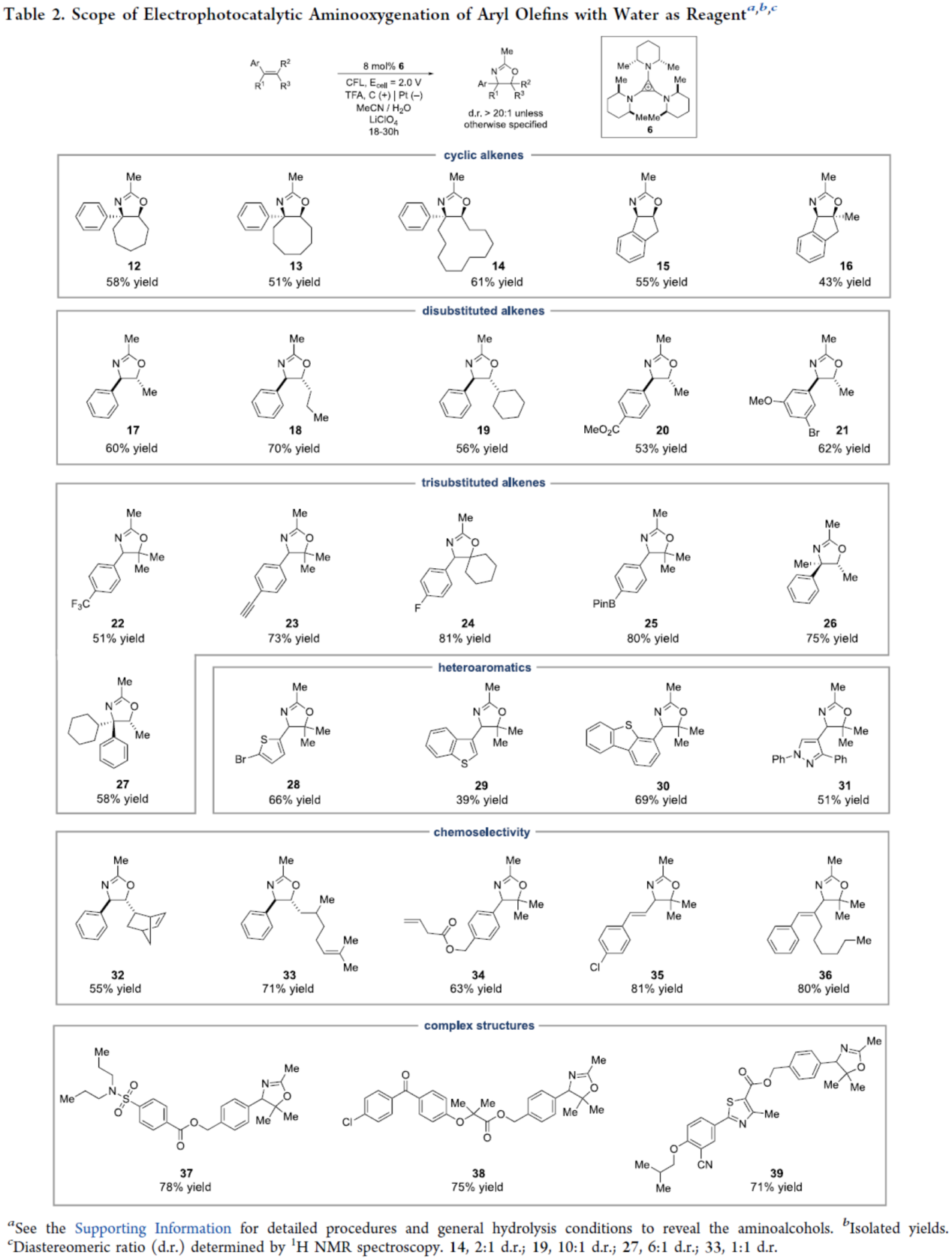
在获得上述最佳反应条件后,作者以水作为亲核试剂,对氨氧合反应的底物范围进行了扩展(Table 2)。首先,各种环状的芳基烯烃,均可顺利进行反应,获得相应的产物12-16,收率为43-61%,且具有高度的顺式非对映选择性。双取代非环状芳基烯烃,也是合适的底物,获得相应的产物17-21,收率为53-70%。具有各种官能团的三取代芳基烯烃,也与体系兼容,获得相应的产物22-27,收率为51-81%。其次,含有杂环取代的烯烃底物,如噻吩基、苯并噻吩基、二苯并噻吩基和吡唑基,也能够顺利进行反应,获得相应的产物28-31,收率为39-69%。此外,对于一系列同时含有脂肪族烯烃和芳基烯烃的底物,反应对芳基烯烃具有高度选择性,获得相应的产物32-34,收率为55-71%。对于含有双烯基的芳基烯烃的底物,反应优先发生在远离芳环的烯烃上,获得相应的产物35-36,收率为80-81%。值得注意的是,该策略还可用于一些复杂分子的后期修饰,获得相应的产物37-39,收率为71-78%。
(图片来源:J. Am. Chem. Soc.)
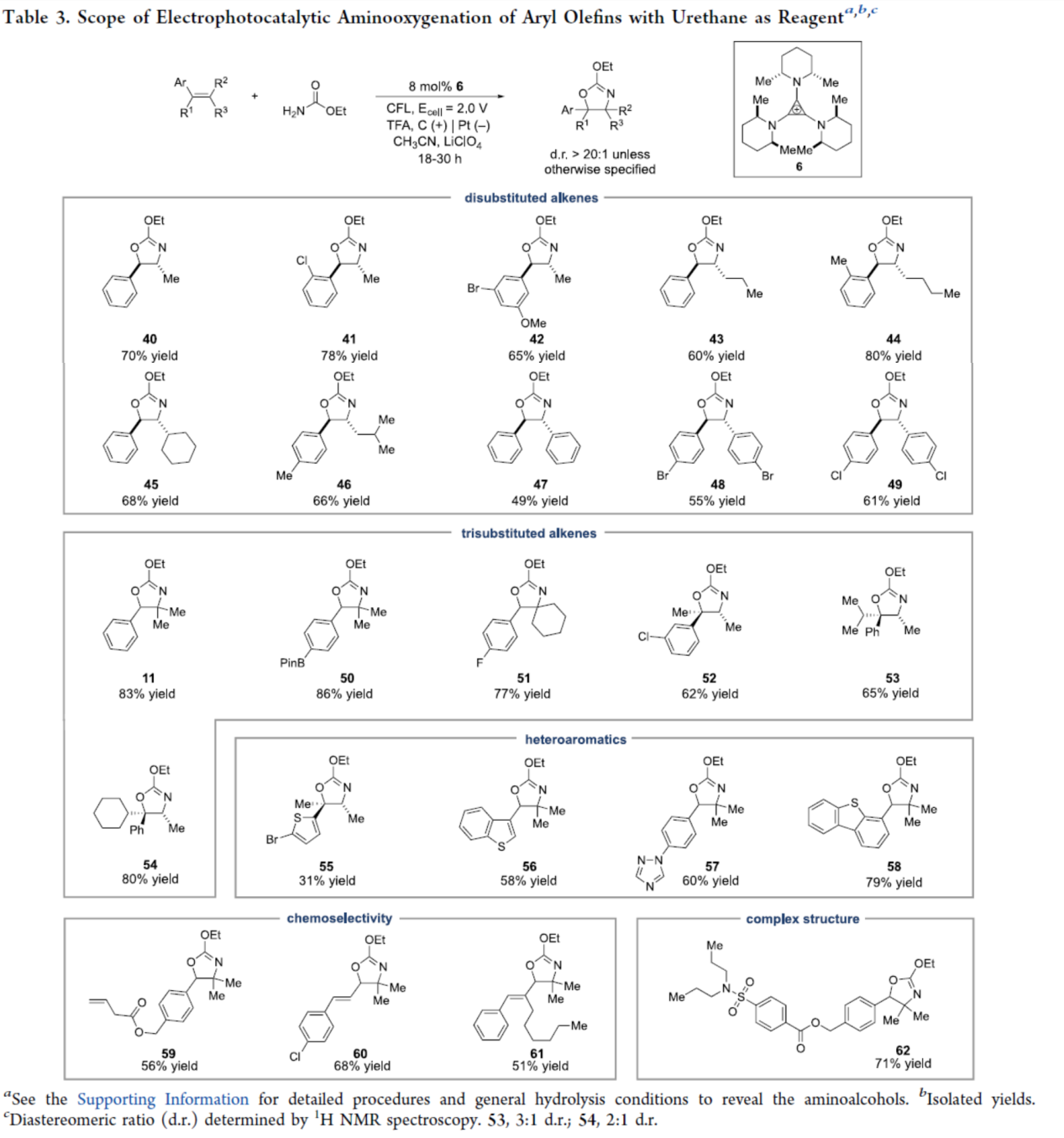
紧接着,作者以氨基甲酸乙酯作为亲核试剂,对氨氧合反应的底物范围进行了扩展(Table 3)。首先,一系列双取代的芳基烯烃,均可顺利进行反应,获得相应的产物40-49,收率为49-78%,且具有出色的反式非对映选择性。同时,三取代芳基烯烃,也与体系兼容,获得相应的产物11和50-54,收率为62-86%。其次,含有杂环取代的烯烃底物,如噻吩基、苯并噻吩基、二苯并噻吩基等,也能够顺利进行反应,获得相应的产物55-58,收率为31-79%。此外,对于一系列同时含有脂肪族烯烃和芳基烯烃的底物,反应对芳基烯烃具有高度选择性,获得相应的产物59,收率为56%。对于含有双烯基的芳基烯烃的底物,反应优先发生在远离芳环的烯烃上,获得相应的产物60-61,收率为51-68%。值得注意的是,该策略还可用于丙磺舒衍生物的后期修饰,获得相应的产物62,收率为71%。
(图片来源:J. Am. Chem. Soc.)
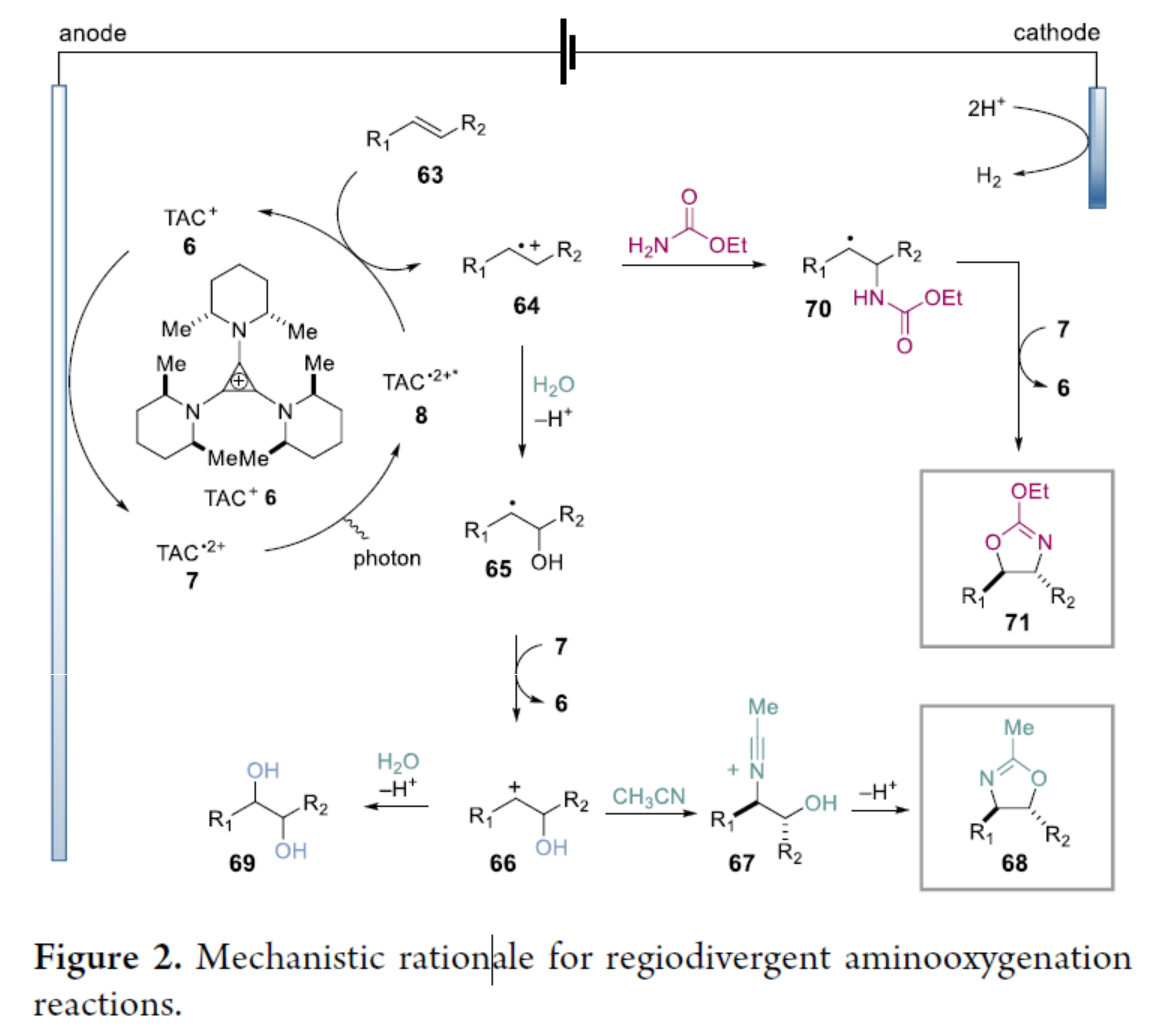
最后,作者提出了一种合理的催化循环过程(Figure 2)。首先,TAC 6可在相对温和的电位下进行电化学氧化,生成TAC自由基双阳离子7。7通过光激发生成非常强的氧化性自由基阳离子中间体8,可将烯烃63氧化为自由基阳离子64。随后,当以水作为亲核试剂时,可与64反应,生成自由基中间体65。65通过7或阳极氧化生成阳离子66。66可被乙腈亲核捕获,生成中间体67。67经分子内加成,从而获得目标噁唑啉产物68。此外,若体系存在大量的水时,反应易形成二醇副产物69。值得注意的是,当以氨基甲酸乙酯作为亲核试剂时,可与64反应,生成自由基中间体70。70的氧化导致氨基甲酸酯羰基氧进行环化,从而获得目标产物71。
(图片来源:J. Am. Chem. Soc.)
总结
美国康奈尔大学Tristan H. Lambert课题组报道了一种通过使用两种廉价易得的底物(水和氨基甲酸乙酯),可将芳基烯烃转化具有任一区域选择性的噁唑啉衍生物。同时,采用光电催化策略,可实现芳基烯烃的双重亲核加成,且无需传统的化学氧化剂。此外,该策略具有反应条件温和、底物范围广泛、官能团兼容性高等特点。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn