

(图片来源:J. Am. Chem. Soc.)
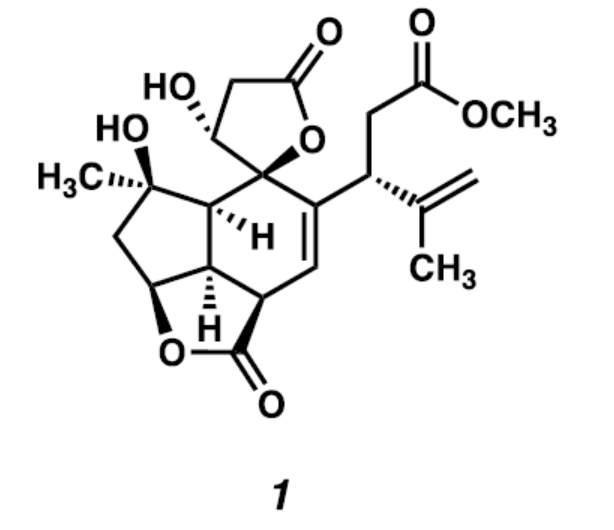
海洋生物提供了看似无穷无尽的复杂天然产物,近几十年来一直受到合成化学家的持续关注。其中,化学家们目前已从Sinularia属的软珊瑚的提取物中分离出了数十种大环和多环分子。多环呋喃丁烯内酯衍生的西松烷型(cembranoid)和去西松烷型(norcembranoid)天然产物长期以来一直是具有挑战性和难以捉摸的合成目标,迄今为止,仅有四例相关的全合成研究。Havellockate(1)是一种于1998年首次从Sinularia granosa中分离出来的C20-西松烷型天然产物,是多环呋喃丁烯内酯衍生的西松烷型家族中一个复杂且具合成挑战的例子(Figure 1A)。同时,1的特征在于高度氧化的顺式稠合三环骨架。1中还含有一个独特的螺稠合的β-羟基丁烯内酯环,这是多环呋喃丁烯内酯衍生的西松烷型家族中其它成员所没有的独特特征。除了这些特征外,1还具有八个手性中心,其中七个连续围绕在高度取代和密集官能团化的核心骨架中。虽然尚未有相关1的全合成报道,但Meht和Barriault课题组强调了该全合成的难度。
首先,作者进行了逆合成分析(Figure 1B)。1可通过烯酮衍生物2经螺环化/酯交换反应生成。2可通过三环化合物3的经氧化反应生成。4通过分子内Diels-Alder反应,可生成3。5通过酰化反应,可生成4。醛化合物6和砜化合物7,通过Julia-Kocienski烯化反应/去硅基化反应,可生成5。

(图片来源:J. Am. Chem. Soc.)
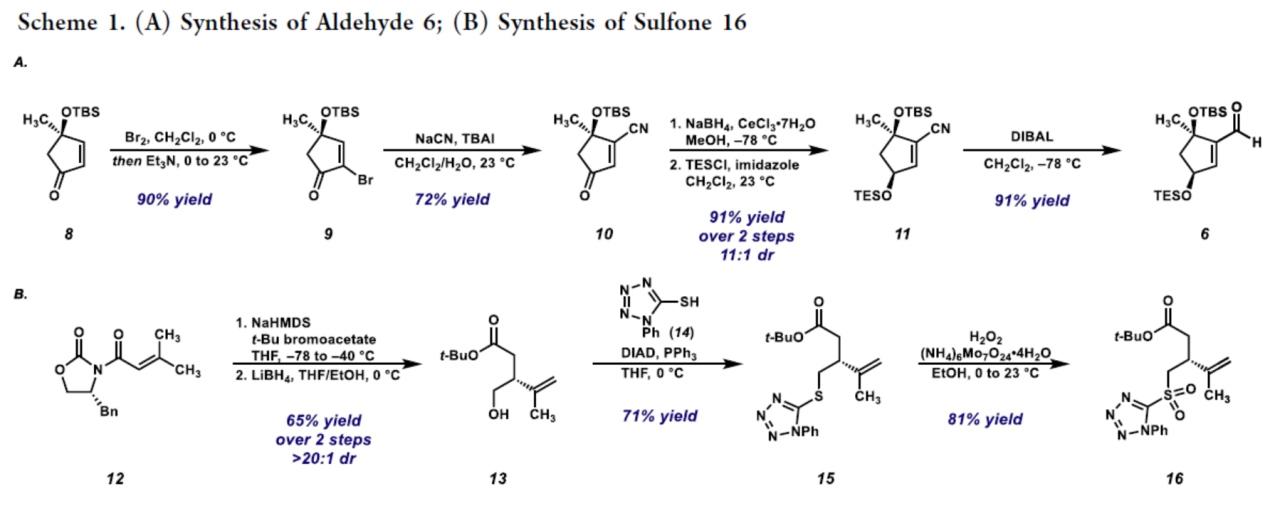
砌块6的合成(Scheme 1A)。以烯酮8为初始底物,经溴化反应,可以90%的收率得到溴化中间体9。9在NaCN、TBAl条件下进行共轭加成/消除反应,可以72%的收率得到β-氰基烯酮10。10在NaBH4、CeCl3·7H2O条件下进行还原后,再使用TESCl对羟基进行保护,可以两步91%的收率得到腈化合物11,dr为11:1。11在DIBAL条件下进行还原,可以91%的收率得到醛类化合物6。
砌块16的合成(Scheme 1B)。12经γ-去质子化,再用溴乙酸叔丁酯进行α-烷基化后,再使用LiBH4进行还原反应,可以两步65%的收率得到醇化合物13,dr > 20:1。13与1-苯基四唑硫醇(PTSH,14)进行Mitsunobu反应,可以71%的收率得到硫化物15。15通过进一步的氧化后,可以81%的收率得到砜化合物16。
(图片来源:J. Am. Chem. Soc.)
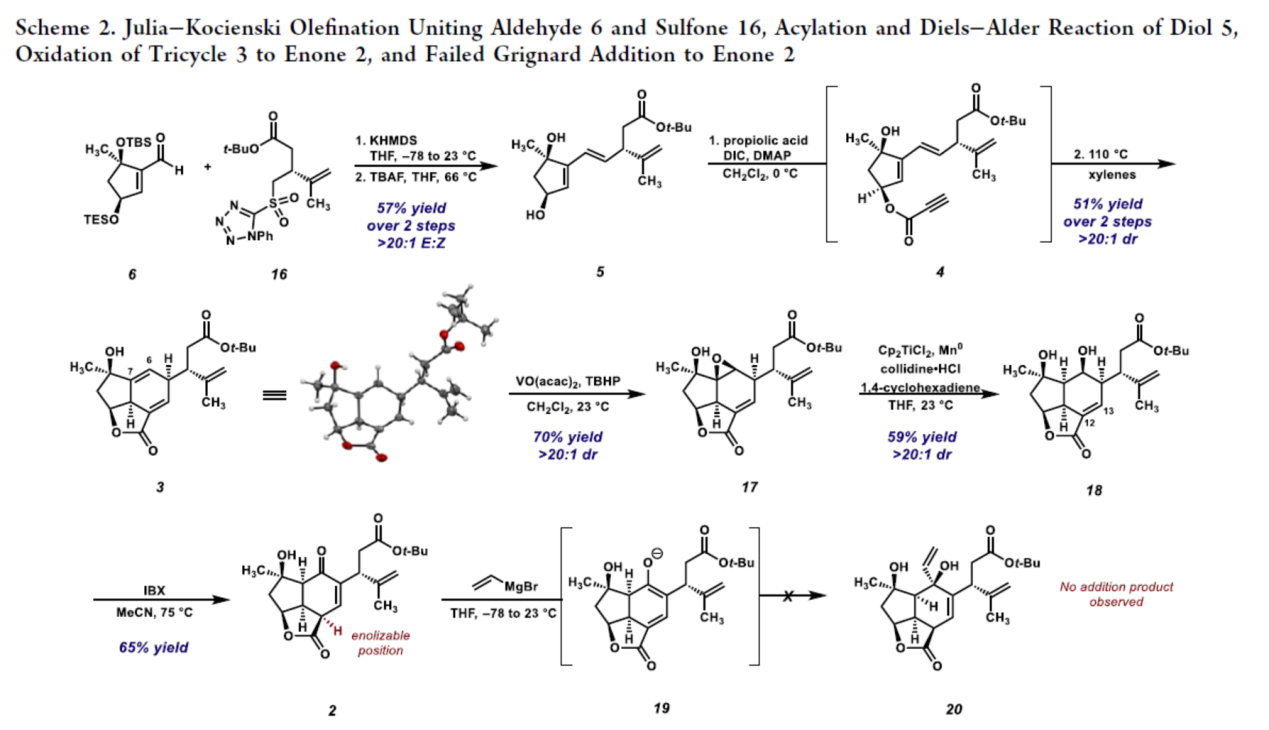
砌块2的合成(Scheme 2)。6和16在KHMDS条件下进行Julia-Kocienski烯化反应,再经去硅基化后,可以两步57%的收率得到二醇化合物5,E:Z > 20:1。5与丙炔酸在DIC、DMAP条件下进行酰化反应,再于二甲苯中进行[4+2]环加成反应,可以两步51%的收率得到化合物3,dr > 20:1。3在VO(acac)2、TBHP条件下进行氧化反应,可以70%的收率得到环氧化物17,dr > 20:1。17在Ti-催化下进行还原性环氧开环,可以59%的收率得到二醇化合物18,dr > 20:1。18在使用IBX进行氧化后(伴随着烯基的迁移),可以65%的收率得到烯酮化合物2。然而,2与乙烯基溴化镁进行非对映选择性1,2-加成反应时发现,由于Grignard试剂的碱性,可使乙烯基β-酮酯2去质子化,生成烯醇盐19,从而无法进行所需的1,2-加成反应。
(图片来源:J. Am. Chem. Soc.)
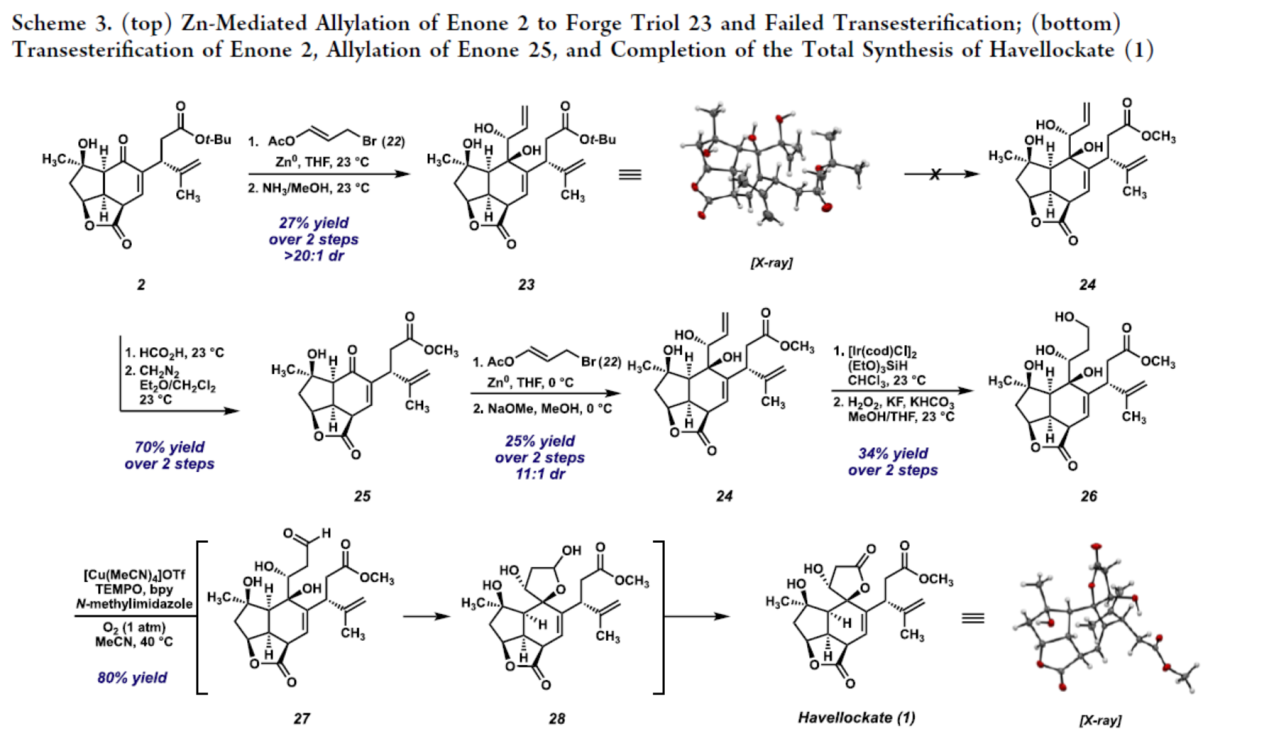
Havellockate(1)的不对称全合成(Scheme 3)。通过进一步的优化后发现,2与3-溴-1-乙酰氧基丙烯(22)在锌催化下进行加成反应后,再于NH3、MeOH条件下进行去乙酰化反应,可以两步27%的收率得到三醇化合物23,dr > 20:1。同时,23的X-射线结构表明,23的C(5)和C(6)-位的立体化学构型与Havellockate(1)中的β-羟基丁烯内酯一致。然而,23通过大量的条件筛选,均未能实现相应的酯交换反应,未能获得所需的化合物24。
通过进一步的研究后发现,使用甲酸可将2中的叔丁酯基团进行断裂,再与重氮甲烷反应,可以两步70%的收率得到甲酯化合物25。25与3-溴-1-乙酰氧基丙烯(22)在锌催化下进行加成反应后,再于NH3、MeOH条件下进行去乙酰化反应,可以两步25%的收率得到三醇化合物24,dr为11:1。24通过anti-Markovnikov的Ir-催化氢硅反应以及Tamao-Fleming氧化反应,可以两步34%的收率得到四醇化合物26。26通过铜催化需氧氧化反应,涉及两次氧化/环化过程,即初始氧化可生成醛27,27可能发生环化生成内酯28,28通过进一步的氧化,可以80%的收率得到Havellockate(1)。所有NMR和IR数据均与文献值一致,此外,通过X-射线晶体学进一步确认了立体化学的相关信息。然而,合成的Havellockate(1)的旋光度在符号或大小上都与文献报道的不匹配(αD 25-56.7° vs 文献αD 25+23.7°)。
(图片来源:J. Am. Chem. Soc.)
总结
美国加州理工学院Brian M. Stoltz课题组报道了一种呋喃丁烯内酯衍生的西松烯二萜内酯Havellockate的首次全合成。首先,作者采用了Julia-Kocienski烯烃化反应,可将两个对映体富集砌块进行连接。随后,通过分子内的Diels-Alder反应,构建了天然产物的六元环骨架。最后,采用非对映选择性烯酮1,2-乙酰氧基烯丙基化反应来构建最终的碳-碳键和剩余的立体生成中心。后期的硅氢化/Tamao-Fleming串联反应之后,再进行铜催化的氧化环化,从而实现了havellockate的全合成。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn