

(图片来源:Nat. Chem.)
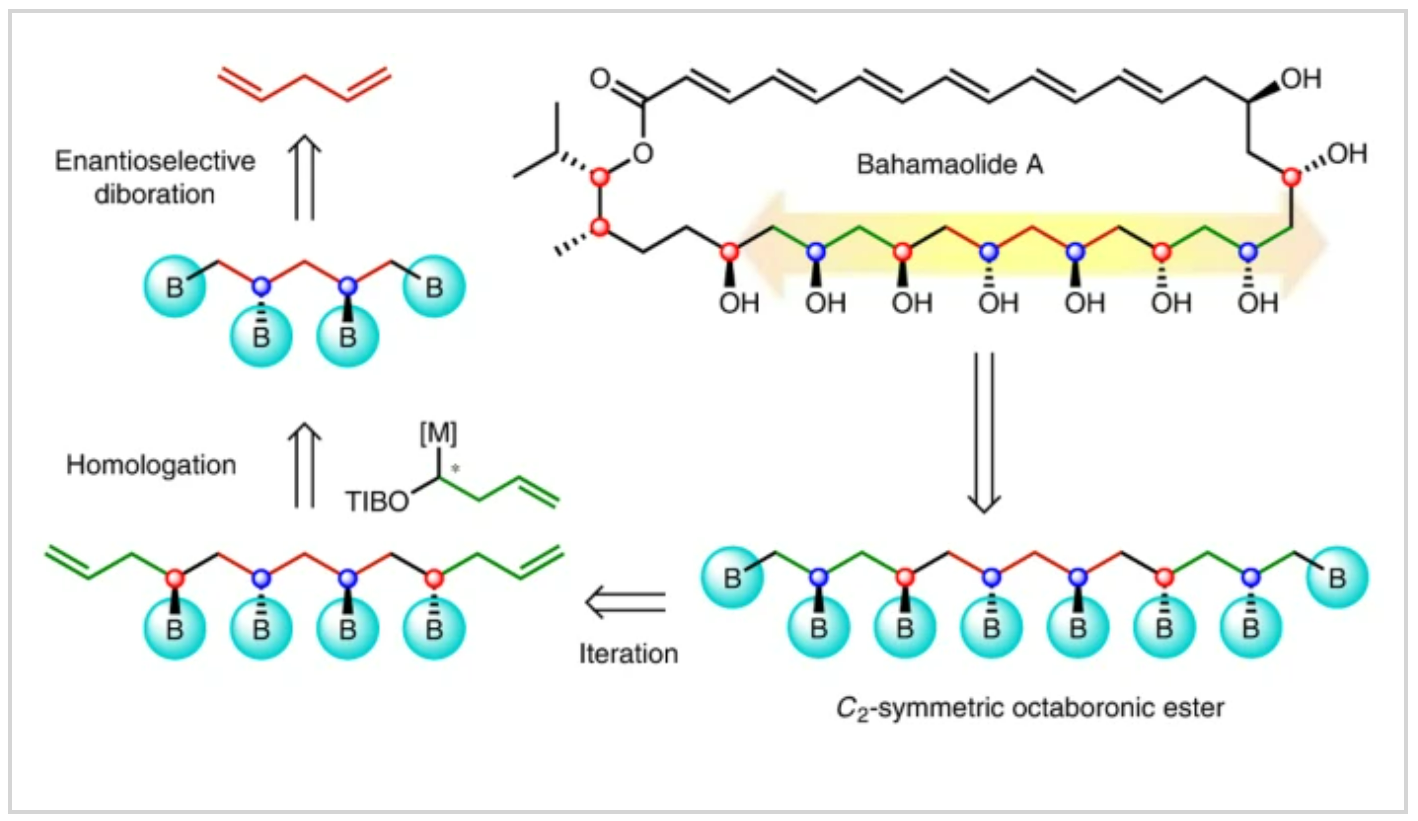
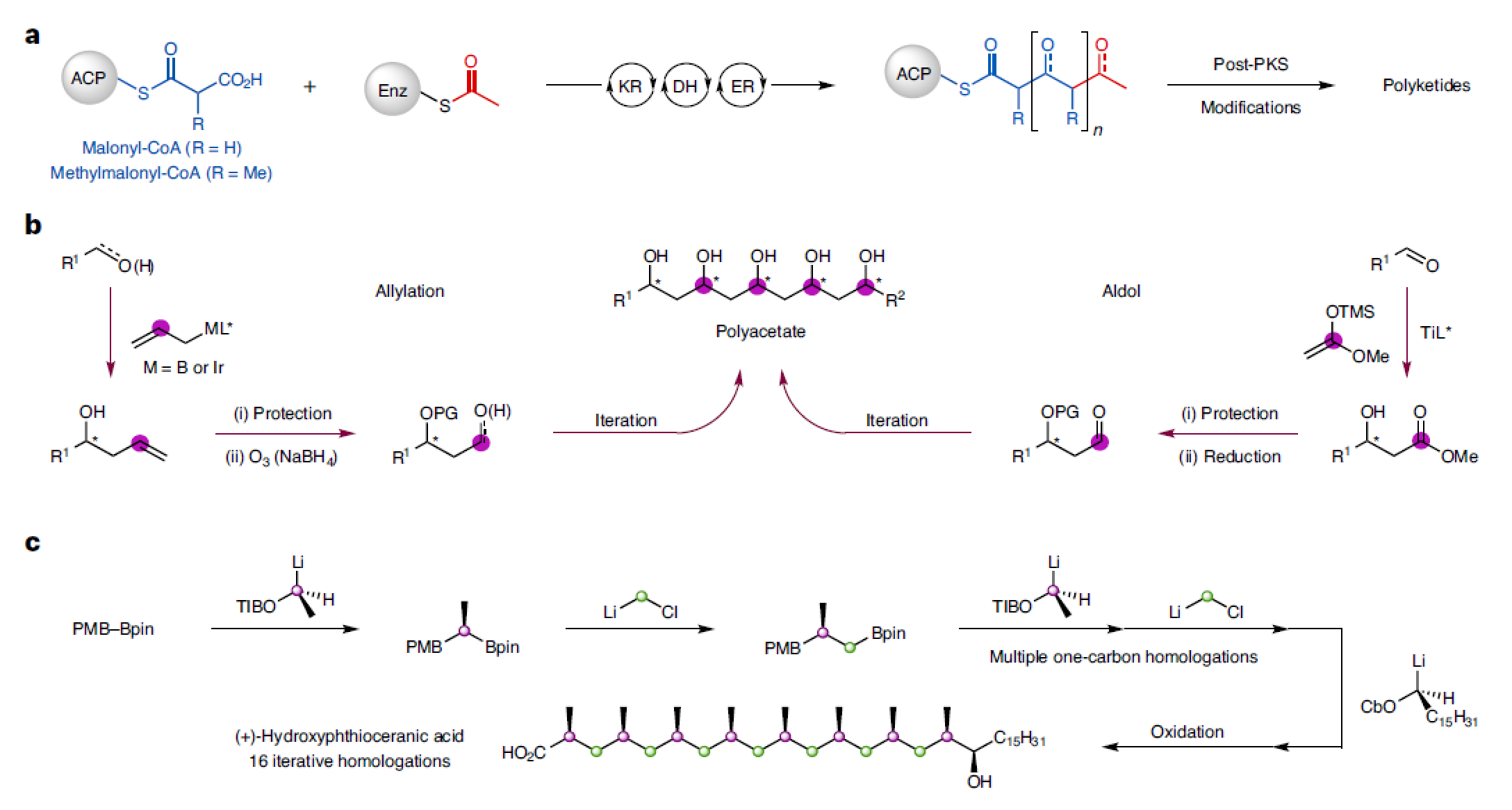
自1952年红霉素A(Erythromycin A)作为广谱抗生素引入临床治疗以来,多酮类药物对药物发现的影响是革命性的。目前畅销的小分子药物中约有20%是多酮类药物。大自然通过对少量合成砌块的迭代合成,然后进行一系列合成修饰,才构建了这样的分子,最终创造了无数的在结构和功能方面均具有高度多样性的天然产物(Fig. 1a)。目前,迭代策略在具有重复片段的多酮骨架的合成中被广泛应用,如丙酸酯、乙酸酯和脱氧丙酸酯等(Fig. 1b)。近些年,Aggarwal课题组报道了利用迭代策略,通过锂化-硼化过程实现了具有多个立体中心的非环分子的合成(Fig. 1c)。基于上述报道,最近,英国布里斯托大学Varinder K. Aggarwal课题组利用迭代策略高立体选择性的实现了1,3-多硼酸酯的合成。此外,利用此方法还可以通过14步实现多烯大环内酯Bahamaolide A的全合成(Fig. 1d)。
(图片来源:Nat. Chem.)
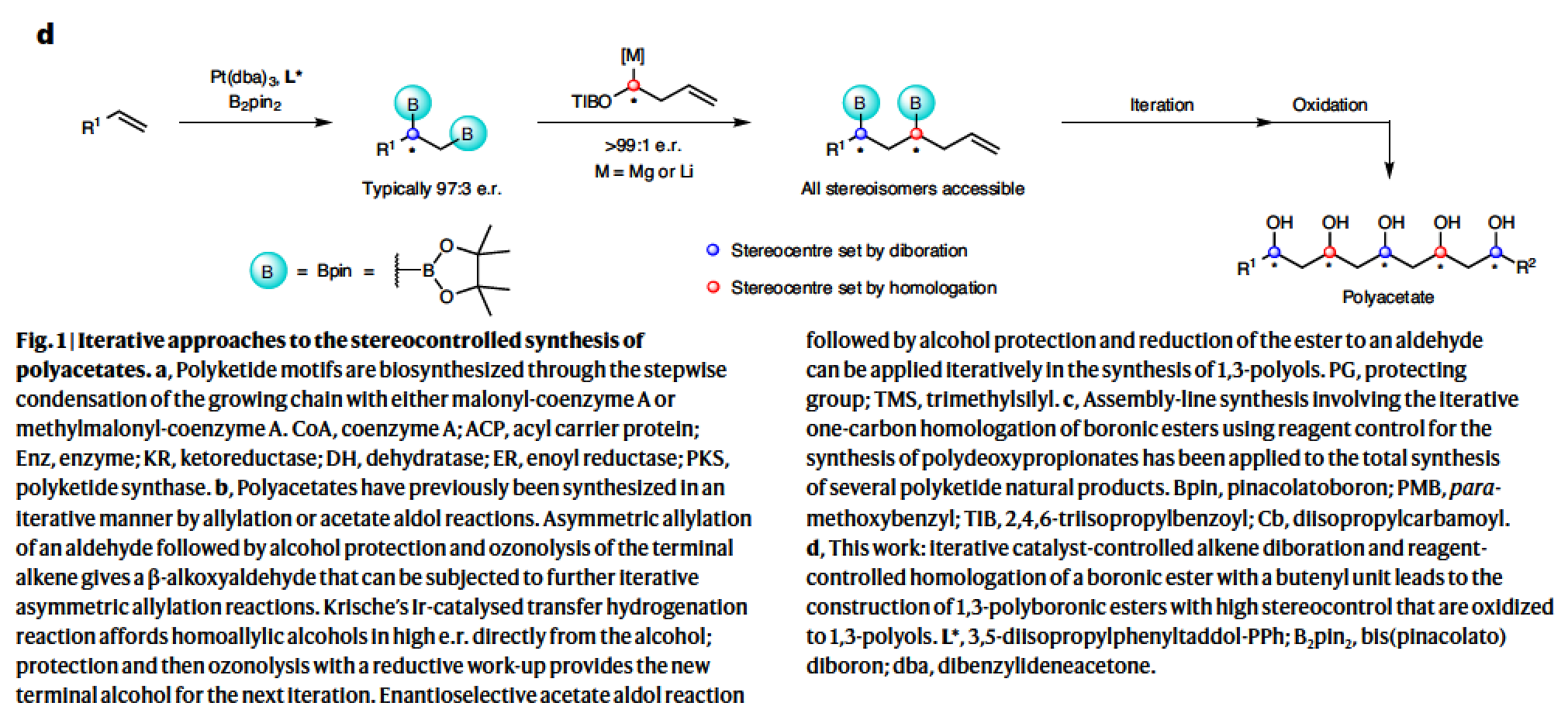
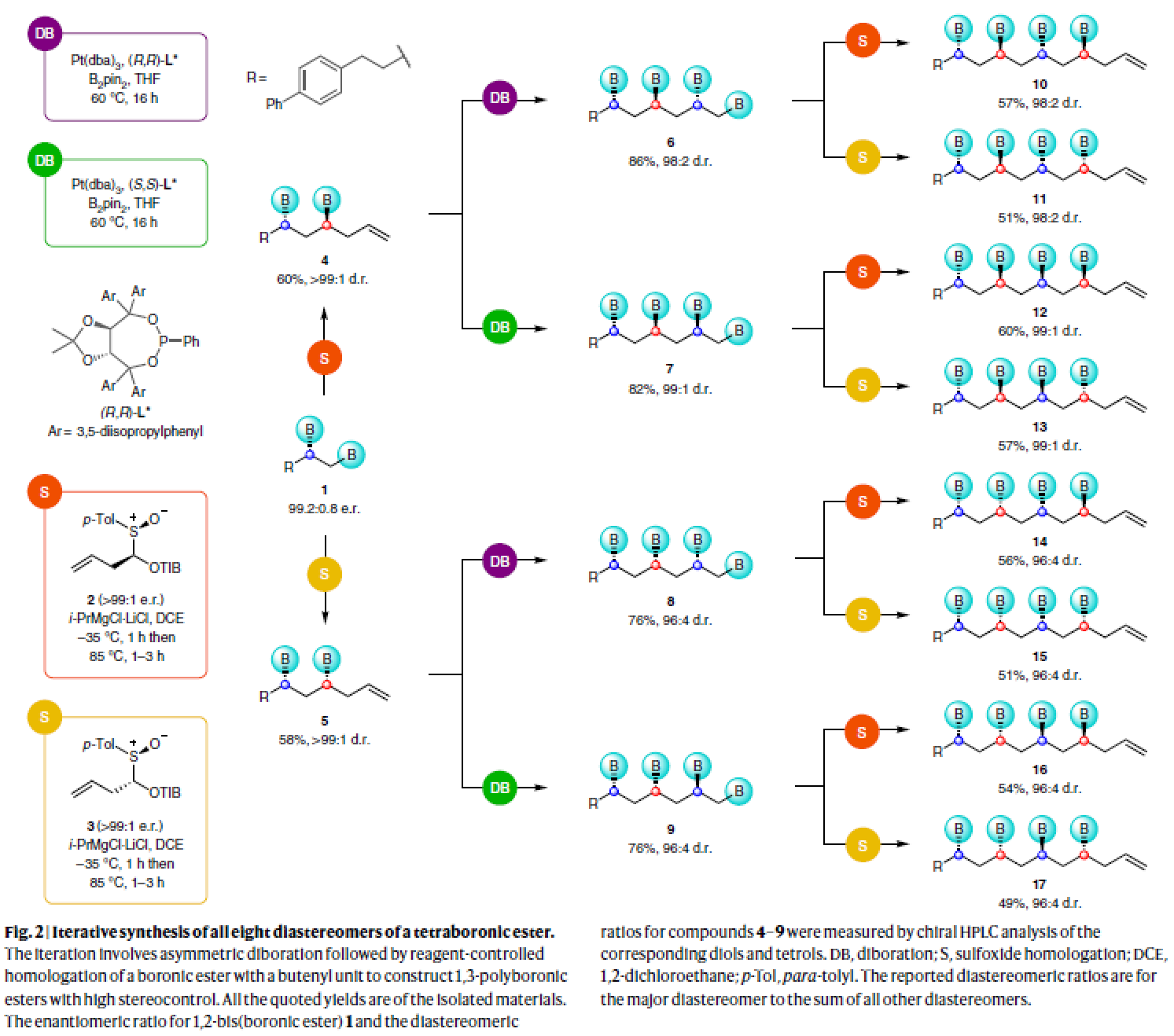
为了验证作者所提出的双硼化-同系化概念,作者利用4-(but-3-en-1-yl)-1,1’-biphenyl作为简单的模板底物,通过Morken铂催化的不对称双硼化反应以77%的产率实现了双硼酸酯产物1(e.r. = 97:3)的合成。此外,作者通过重结晶可以将1提纯至> 99:1 e.r.。接下来,作者利用2和3与1发生同系化反应可以分别实现高烯丙基硼酸酯4(60%,> 99:1 d.r.)和5(58%,> 99:1 d.r.)的合成。最后,作者通过后续的同系化过程分别实现了八个非对映异构体10-17的合成(Fig. 2)。
(图片来源:Nat. Chem.)
在确定了此迭代策略的可行性之后,作者希望将其应用到Bahamaolide A(18)(Bahamaolide A是最近发现的含9个1,3-羟基片段的多烯大环内酯家族成员)的全合成中(Fig. 3)。作者通过逆合成分析得出:首先,Bahamaolide A通过多烯片段的断裂得到高烯丙基硅醚19;而19则可以通过C2-对称的硼酸酯21与23和22的同系化反应合成。利用作者发展的双硼化-同系化反应可以以1,4-戊二烯26作为起始原料,通过三步即可实现硼酸酯21的合成。
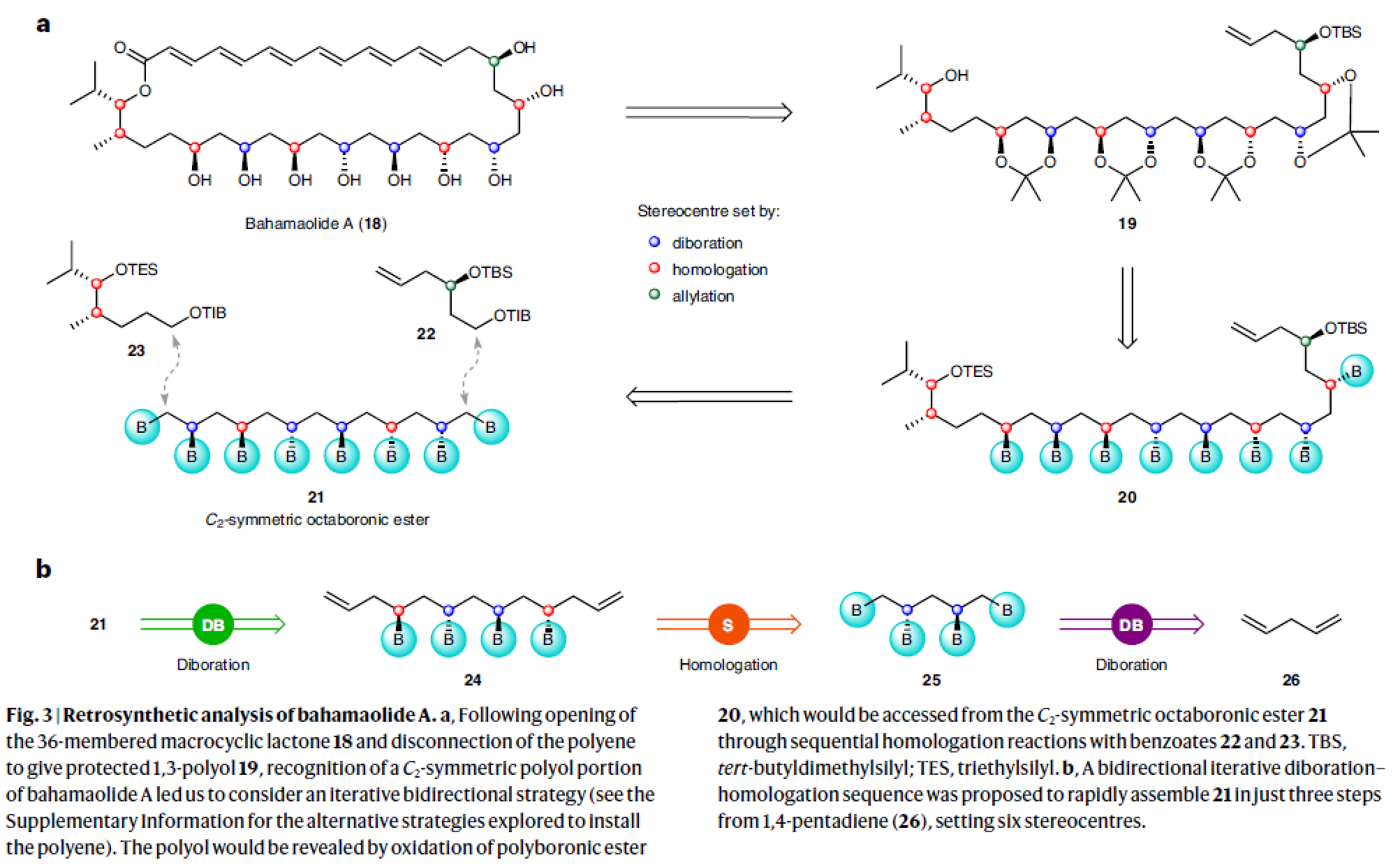
(图片来源:Nat. Chem.)
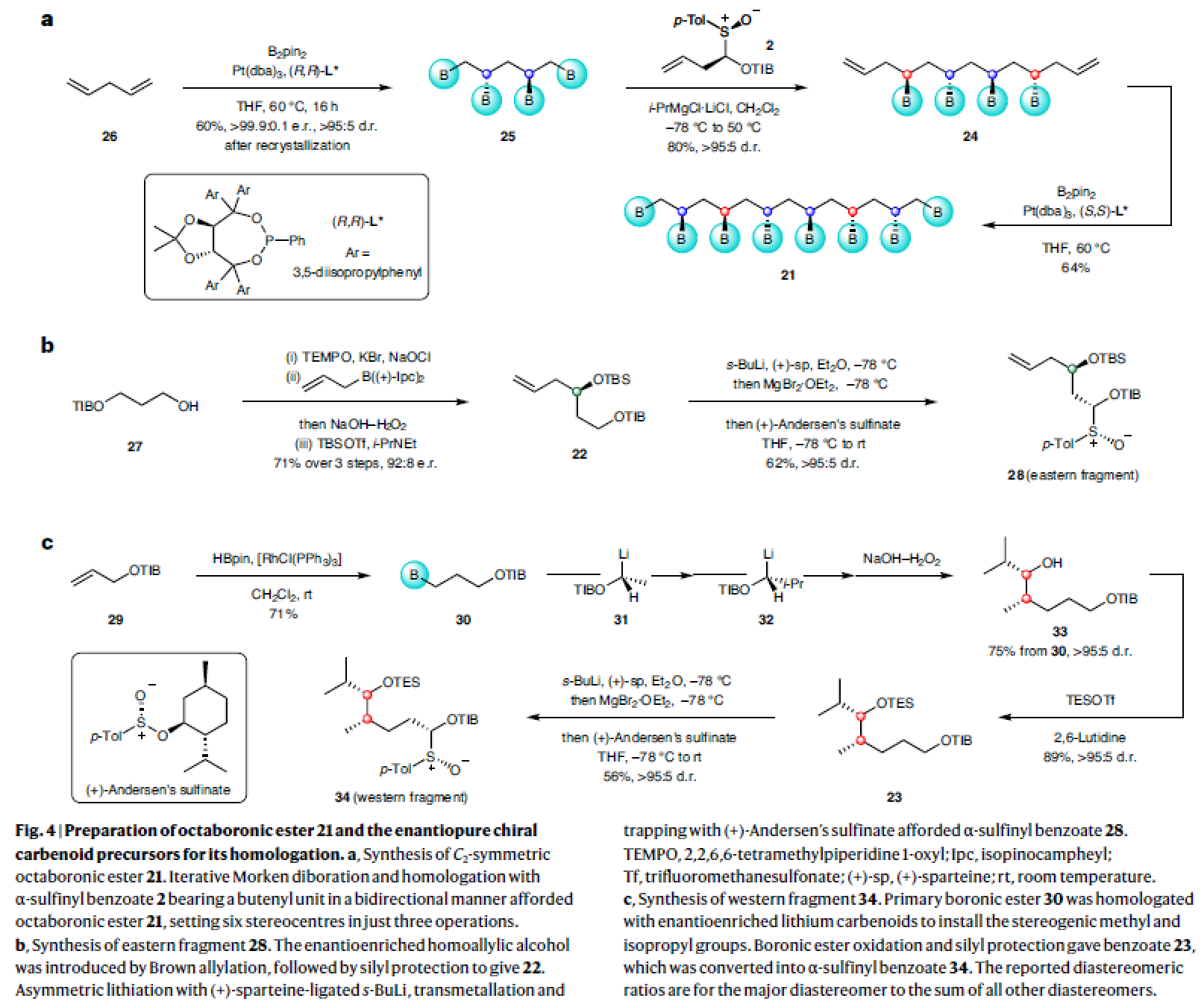
首先作者利用1,4-戊二烯26作为起始原料,通过Morken双硼化策略以89%的产率得到C2-对称的1,2,4,5-四硼酸酯25(d.r. = 95:5)。随后,作者通过重结晶可以以60%的产率得到单一立体异构体,且单晶衍射证实了此四硼酸酯的绝对构型。接下来,作者利用同系化反应策略,使用2(α-sulfinyl benzoate)和i-PrMgCl·LiCl以80%的产率,完全的非对映选择性实现了目标双高烯丙基四硼酸酯24的合成。最后,作者利用发展的双硼化策略,当增加底物浓度至1.0 M时可以以64%的产率实现21的合成,并将硼氢化副产物的产率降至7%。至此,作者仅仅利用三步合成即构建了Bahamaolide A中的六个立体中心(Fig. 4a)。
接下来,作者对21的同系化反应所需的卡宾体前体28和34进行分别合成。实现片段28的合成可以首先利用醇27的氧化、Brown不对称烯丙基硼化以及硅基保护三步以71%的产率得到22(e.r. = 92:8)。随后,22可以通过对映选择性锂化以及与(+)-Andersen’s sulfinate反应可以以62%的产率得到目标片段28(单一异构体)(Fig. 4b)。而片段34的合成需要首先通过29的硼氢化得到硼酸酯30。随后,30与对映体富集的锂卡宾体31和32反应,并通过氧化得到单一的醇异构体33。最后,33通过硅基保护以及亚磺酰基的安装得到单一异构体34(Fig. 4c)。
(图片来源:Nat. Chem.)
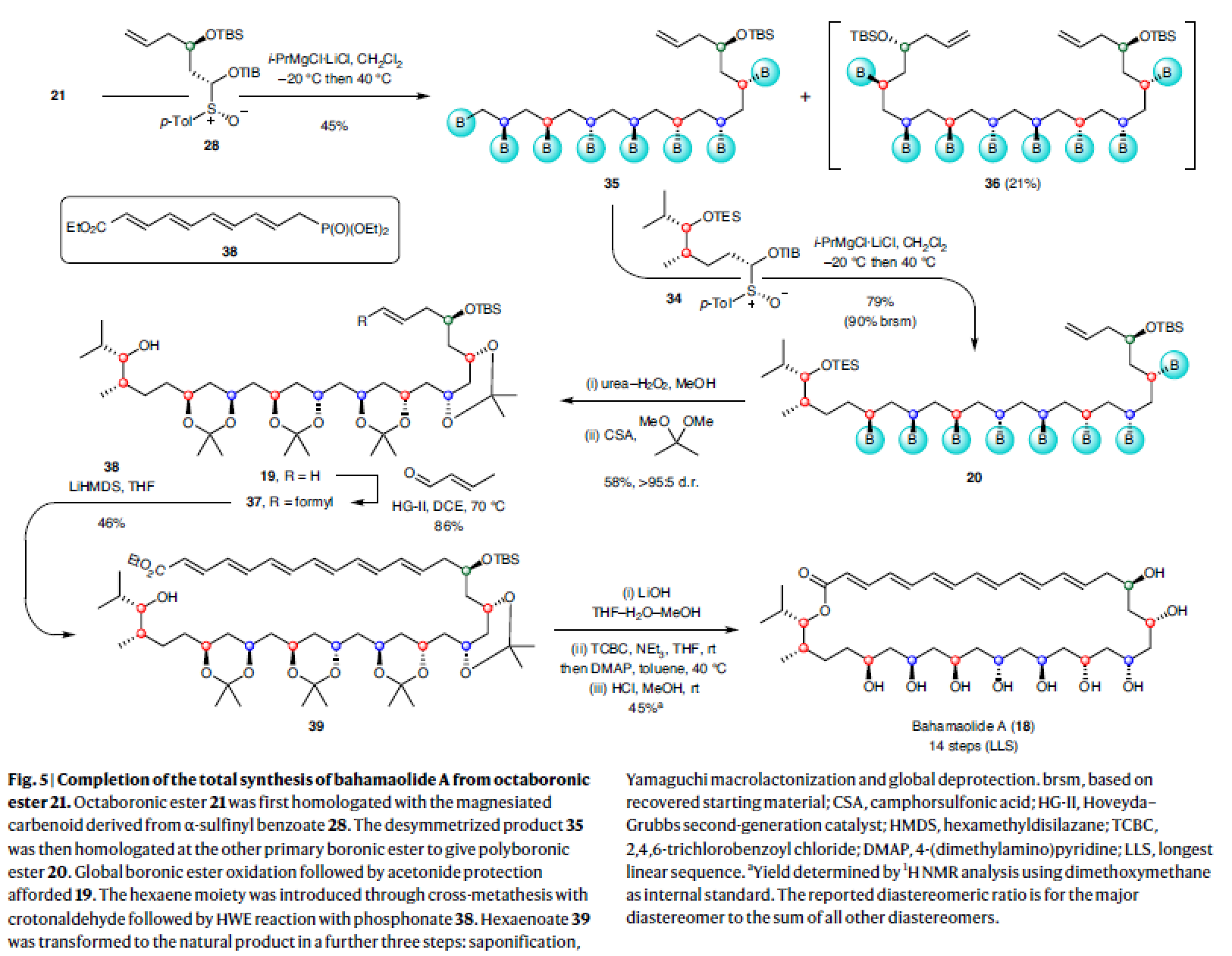
接下来,作者首先利用28与21反应以45%的产率得到去对称化产物35。随后35与34反应以79%的产率得到多硼酸酯产物20。紧接着,20经历硼酸酯的氧化和缩丙酮保护以58%的产率得到产物19。接下来,19通过与巴豆醛发生交叉复分解反应以及与膦酯38发生HWE反应得到产物39。最后,39通过皂化反应、Yamaguchi大环内脂化和脱保护三步(45%)实现了Bahamaolide A 18的合成(Fig. 5)。
(图片来源:Nat. Chem.)
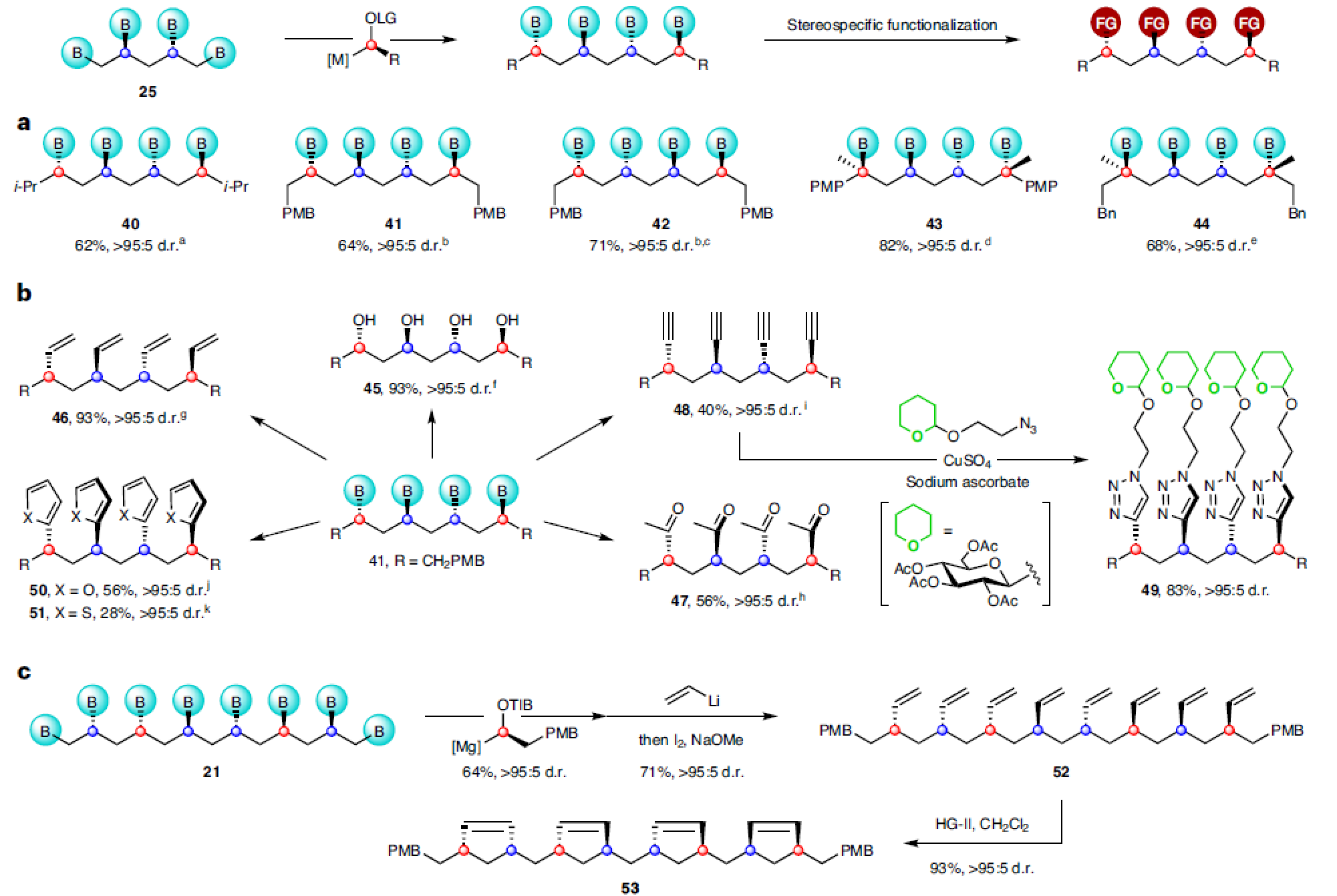
作者在实现Bahamaolide A的全合成过程中所制备的多硼酸酯为其它合成转化提供了可能性。通过硼酸酯的立体专一性转化可以实现1,3-官能团化分子库的制备。作者首先制备了一组具有不同取代基的四硼酸酯(含硼碳原子均具有不同相对构型),来探索其与不同卡宾体试剂的反应(Fig. 6a)。由一级苯甲酸酯衍生的卡宾体可以完美的实现非对映选择性控制,以较高的产率实现二级硼酸酯40-42的合成。此外,作者利用锂化的二级氨基甲酸酯和苯甲酸酯可以以较高的产率和d.r. 实现兼具二级和三级硼酸酯骨架的四硼酸酯43和44的合成。接下来,作者探索C2-对称的四硼酸酯41的合成转化(Fig. 6b)。例如:四硼酸酯41可以被脲-H2O2络合物氧化,以93%的产率得到C2-对称的四醇45。此外,作者利用改进的Zweifel烯基化反应以93%的产率实现了四烯基产物46的合成。值得注意的是,合成出的四炔48还可以通过CuAAC反应以83%的产率实现多三唑产物49的合成。最后,作者利用硼酸酯21通过镁化-硼化以及Zweifel烯基化和关环复分解反应实现了四环戊烯产物53的合成(Fig. 6c)。

(图片来源:Nat. Chem.)
总结 Varinder K. Aggarwal课题组利用迭代策略高立体选择性的实现了1,3-多硼酸酯的合成。在这其中每一步转化都独立控制立体化学构型,且在1,3-多硼酸酯立体氧化生成1,3-多元醇之前,可以对其进行迭代合成。值得注意的是,发展出的方法可用于多烯大环内酯Bahamaolide A的14步合成。此外,合成出的1,3-多硼酸酯化合物可以进行多种立体定向合成转化,进而实现一系列多烯烃、多炔烃、多酮和多芳烃化合物的合成。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn