

(图片来源:J. Am. Chem. Soc.)
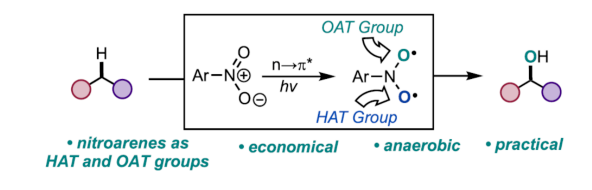
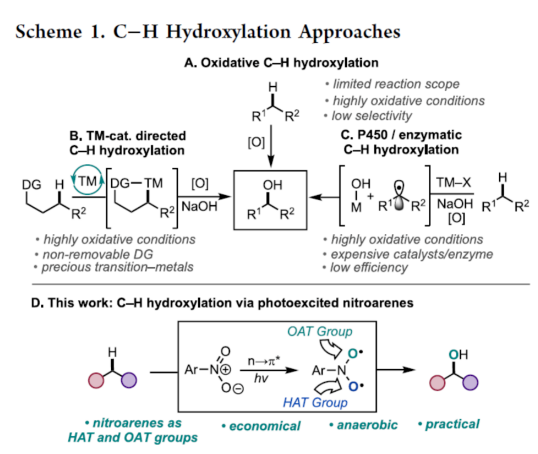
脂肪族C-H键直接转化为羟基,是有机化学中的一个具有价值的研究课题。然而,由于C(sp3)-H键的位点选择性活化难度大以及一些氧化敏感性官能团的兼容性问题,此类反应具有一定的挑战。目前,化学家们已开发出几种创新型的策略,可在脂肪族骨架上引入氧原子(Scheme 1)。然而,由于C-H键的直接氧化条件苛刻,从而限制了底物的范围。此外,使用这种方法很难实现位点选择性的C-H氧化功能化和对醇优于其它过氧化副产物的偏好(Scheme 1A)。为了解决位点选择性的问题,化学家们在过渡金属催化的C-H羟基化反应使用了导向基团,但存在导向基团的引入与去除的繁琐过程以及贵金属催化剂的使用(Scheme 1B)。最近,仿生Mn/Fe-催化或酶催化C-H羟基化反应是贵金属方法的一种有效的替代策略,但也存在反应效率低、过度氧化、配体与酶的成本高等问题(Scheme 1C)。同时,上述三种方法都需要使用额外的氧化剂,从而限制了反应的底物范围。近日,美国纽约大学Marvin Parasram课题组报道了一种光激发硝基芳烃介导脂肪族化合物的无氧C-H羟基化反应(Scheme 1D)。值得注意的是,光激发硝基芳烃的双自由基性质使C-H活化和氧原子转移步骤都成为可能,从而消除了对额外氧化剂的需要,并为C(sp3)-H羟基化提供了一种温和、通用且经济高效的方法。
最近,化学家们研究发现,硝基芳烃的可见光激发可生成三重态的双自由基中间体,可使烯烃发生断裂生成羰基化合物。机理研究表明,上述的三重态双自由基中间体能够与硝基芳烃的邻烷基通过分子内氢原子转移(HAT)活化C-H键。同时,在苛刻的紫外线照射下,硝基芳烃的氧原子转移(OAT)可以实现C-H氧化。此外,光激发的β-芳基取代的硝基芳烃可引发分子内OAT,生成三级二芳基醇。虽然上述的两种方法都具有显著的新颖性,但其仍存在底物范围有窄以及过度氧化的问题。基于光生硝基芳烃作为C-H键活化剂和氧原子源的能力,作者设想,在可见光照射下能否实现脂肪族前体的选择性、分子间无氧C-H键的羟基化反应。
(图片来源:J. Am. Chem. Soc.)
首先,通过对反应条件的优化后发现,2-氯-4-硝基吡啶和3,5-双(三氟甲基)硝基苯分别对苄基和非活化C-H键的羟基化是高效的;(2)使用六氟异丙醇(HFIP)作为添加剂,对于抑制羟基化产物的过度氧化至关重要,可能是通过氢键的相互作用;(3)对照研究表明,光和其它反应组分是转化所必需的。
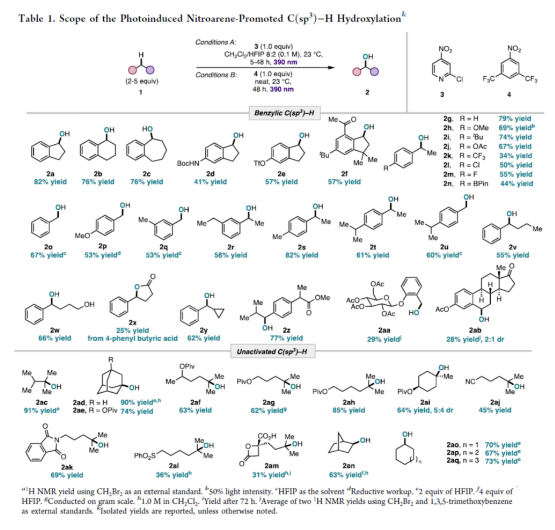
随后,作者对底物范围进行了扩展(Table 1)。在Conditions A条件下,具有不同环尺寸的环状苄基化合物,均可顺利进行反应,获得相应的产物2a-2c,收率为76-82%。茚的芳基上含有-NHBoc和-OTf时,也是合适的底物,获得相应的产物2d-2e,收率为41-57%。Celestolide是香精和香料中的一种有价值的分子,也可以57%的收率得到产物2f。其次,一系列具有不同电性取代的乙苯,均可顺利进行反应,获得相应的产物2g-2n和2r-2t,收率为34-82%。当甲苯底物的芳基上含有烷氧基、甲基、异丙基时,也与体系兼容,获得相应的产物2o-2q和2u,收率为34-79%。值得注意的是,基于2s-2t的反应结果表明,苄基C(sp3)-H氧化反应的选择性为二级>一级>三级。具有不同链长和官能团的其它二级苄基底物,也能够顺利反应,获得相应的产物2v-2y,收率为25-66%。同时,该策略还可用于一些药物分子的后期修饰,如2z和2aa-2ab,收率为28-77%。
在Conditions B条件下,非活化底物中较弱的3°C-H键,可顺利进行羟基化反应,获得相应的产物2ac-2ad,收率为90-91%。含有远端新戊酸酯基的底物,也可选择性的在3°C-H键进行羟基化,获得相应的产物2ae-2ai,收率为62-85%。含有各种敏感性的极性基团,如腈、邻苯二甲酰亚胺和磺酰基,也与体系兼容,获得相应的产物2aj-2al,收率为36-69%。同时,该策略还可用于生物活性分子的后期衍生化,如2am。此外,一系列具有挑战性的二级C-H键也可顺利进行C-H羟基化反应,获得相应的产物2an-2aq,收率为63-73%。
(图片来源:J. Am. Chem. Soc.)
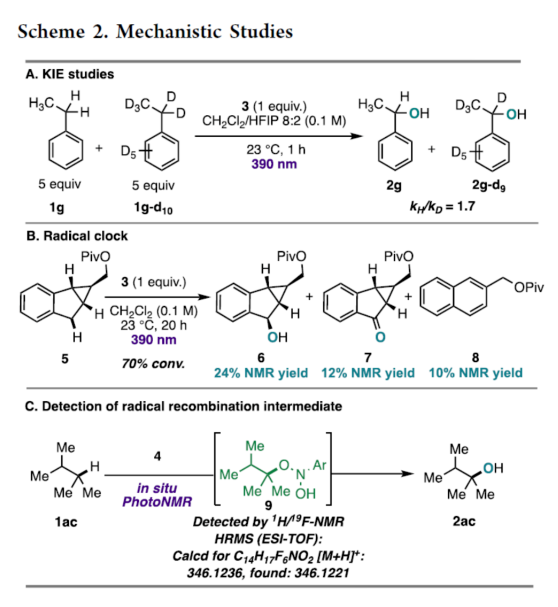
此外,作者还对反应机理进行了进一步的研究(Scheme 2)。首先,KIE研究表明,C(sp3)-H键与光激发硝基芳烃的HAT参与了限速步骤(Scheme 2A)。其次,自由基钟实验表明,反应形成了碳中心的自由基中间体(Scheme 2B)。此外,通过对自由基重合中间体的检测发现,自由基重组产物(12)的断裂,可生成所需的C-H羟基化产物(2)和nitrosoarene副产物(Scheme 2C)。
(图片来源:J. Am. Chem. Soc.)
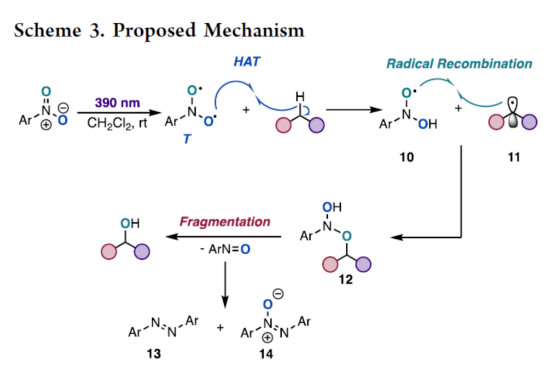
基于上述的研究以及相关文献的查阅,作者提出了一种合理的催化循环过程(Scheme 3)。首先,硝基芳烃的直接光激发可生成三重态双自由基中间体,可与烷烃中的C(sp3)-H键发生HAT,生成烷基自由基11和以氧中心的二羟基苯胺自由基10。10和11通过自由基重合后,生成中间体12。最后,12断裂后,可生成氧原子转移产物和亚硝基副产物,后者在反应条件下迅速缩合形成副产物13和14。
(图片来源:J. Am. Chem. Soc.)
总结
美国纽约大学Marvin Parasram课题组报道了一种光激发硝基芳烃介导脂肪族化合物的无氧C-H羟基化反应。基于光激发硝基芳烃的双重官能团化的反应性,形成的三重态双自由基激发态可以活化C(sp3)-H键和促进氧原子转移。值得注意的是,该策略不需要使用额外的氧化剂或过渡金属催化剂,具有低成本与高原子经济性。此外,由于体系的无氧性质,一些具有氧化敏感性官能团的脂肪族底物,也在未发生过度氧化的状态下顺利进行。
文献详情:
Joshua M. Paolillo, Alana D. Duke, Emma S. Gogarnoiu, Dan E. Wise, Marvin Parasram*. Anaerobic Hydroxylation of C(sp3)−H Bonds Enabled by the Synergistic Nature of Photoexcited Nitroarenes. J. Am. Chem. Soc. 2023
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn