

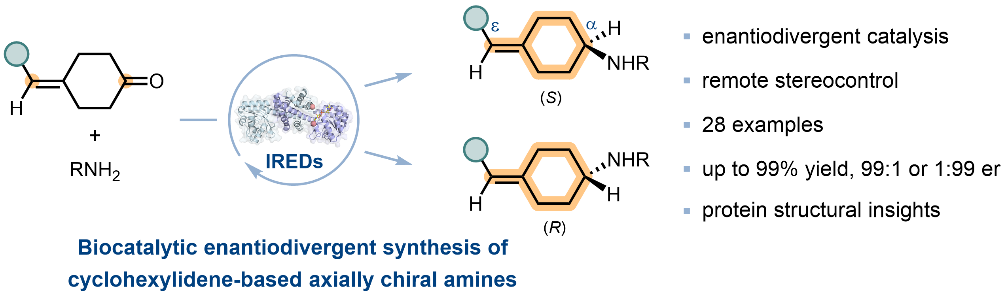
目前光学纯环己亚基手性胺的合成仍主要依赖传统的手性拆分,其不对称合成面临的挑战包括:一方面,由于四个手性相关基团分布在手性轴的两端,空间距离较远,传统小分子催化剂难以实现有效的远程立体化学控制;另一方面,同时高效制备R和S两种构型的轴手性胺也极具挑战。近日,中国医学科学院/北京协和医学院医药生物技术研究所付海根课题组利用亚胺还原酶(IREDs)成功实现了环己亚基轴手性胺的高效不对称合成(图1)。研究团队通过筛选和优化一对立体选择性互补的IREDs,建立了对映发散性合成策略,以最高99%的产率和优异的立体选择性(R/S比例达99:1或1:99 er)精准构建了目标手性分子,为环己亚基轴手性胺的定向合成提供了高效、绿色的生物催化途径。
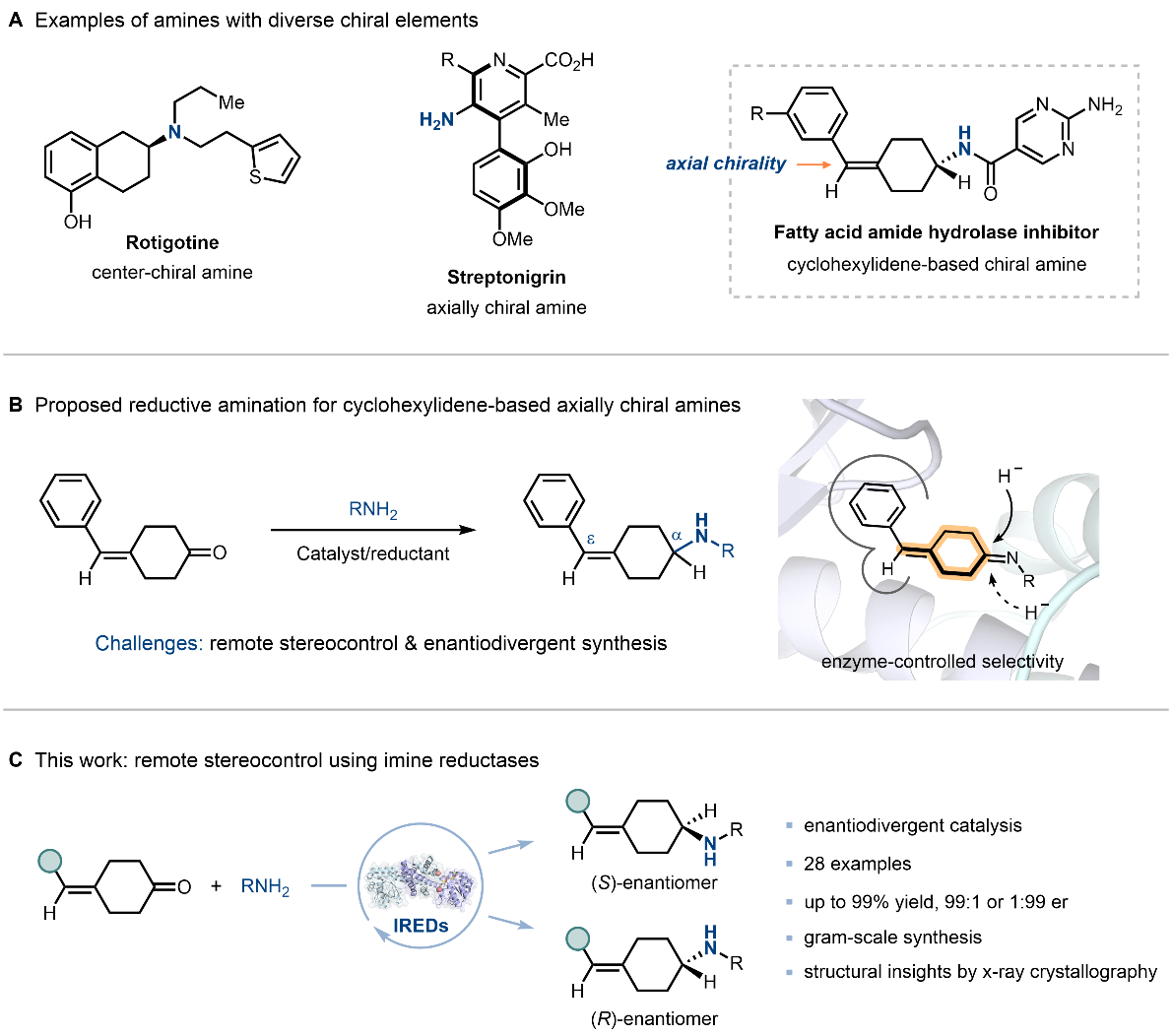
图1.生物催化合成轴手性环己亚基轴手性胺。图片来源:Angew. Chem. Int. Ed
作者以亚苄基环己酮(1a)与烯丙胺(2a)为模型底物,通过初筛粗酶、随后采用纯酶验证的方法,发现IRED-08和IRED-15可催化模板反应并以80%收率和99:1er生成(R)-3;IRED-27则以84%产率和1:99er生成(S)-3。随后通过系统优化反应条件,可将IRED-08和IRED-15的产率分别提升至91%和94%,IRED-27的产率提升至97%,同时均保持高立体选择性(图2)。
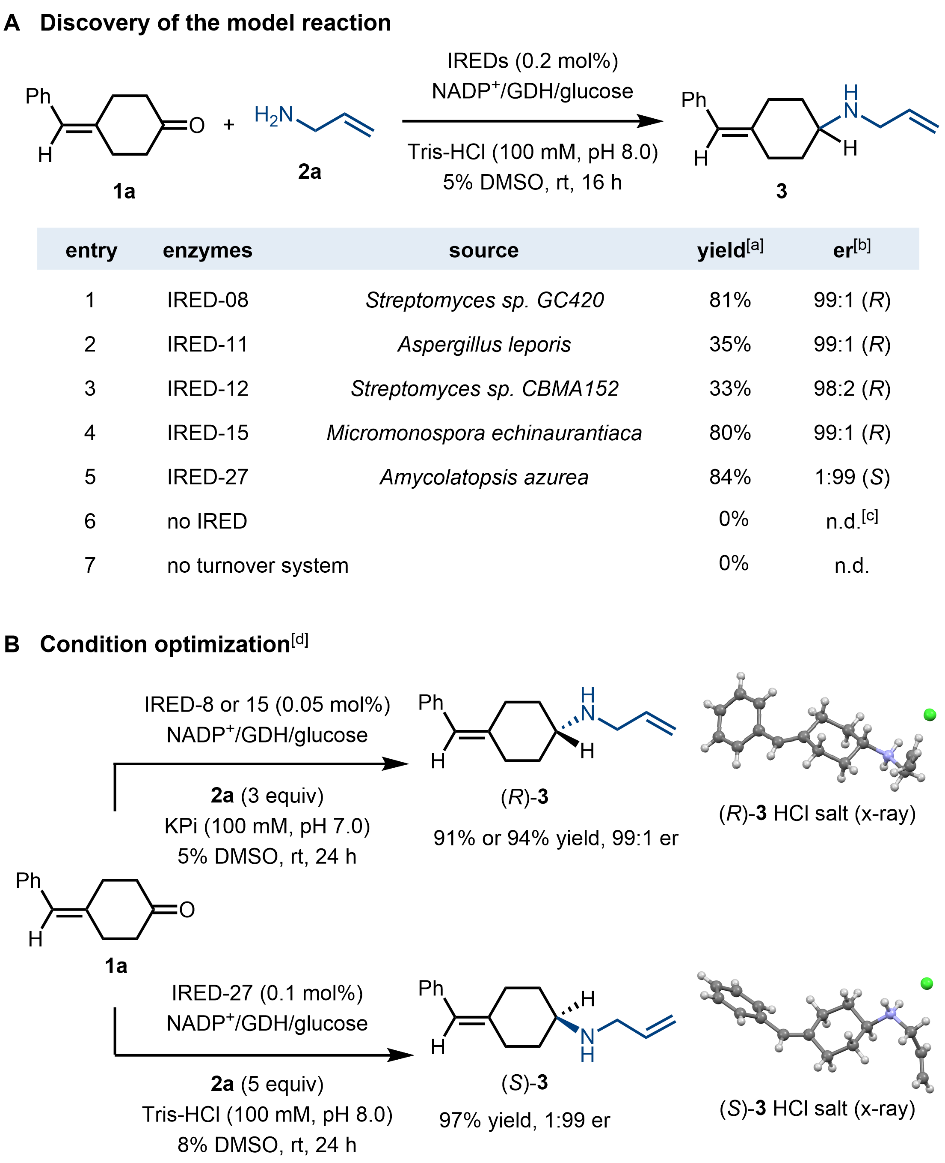
图2. 模板反应筛选与优化。图片来源:Angew. Chem. Int. Ed
在获得对映互补的IREDs后,作者对该体系的底物适用范围展开探索。对于胺供体而言,多种一级胺,包括短链胺(3-4)、取代苄胺(5-14)和杂环(15-17)等均能高效生成相应的轴手性胺产物,且具有优异的对映选择性(产率最高可达99%,er最高可达99:1或1:99),体系对于二级胺或芳香胺则兼容性较差。在考察亚苄基环己酮类底物时,作者发现部分底物在水相体系中溶解性较差,导致反应产率降低。通过引入非离子表面活性剂TPGS-750-M,显著提高了疏水性底物的溶解度,使反应效率大幅提升。优化后的体系可兼容多种取代基(芳基、烷基、烯基、炔基)的4-亚甲基环己酮,能以良好至优异的产率和对映选择性得到目标产物(18-30,图3)。此外,作者还选取代表性化合物展开克级制备反应,进一步验证了该IREDs催化体系的合成潜力。
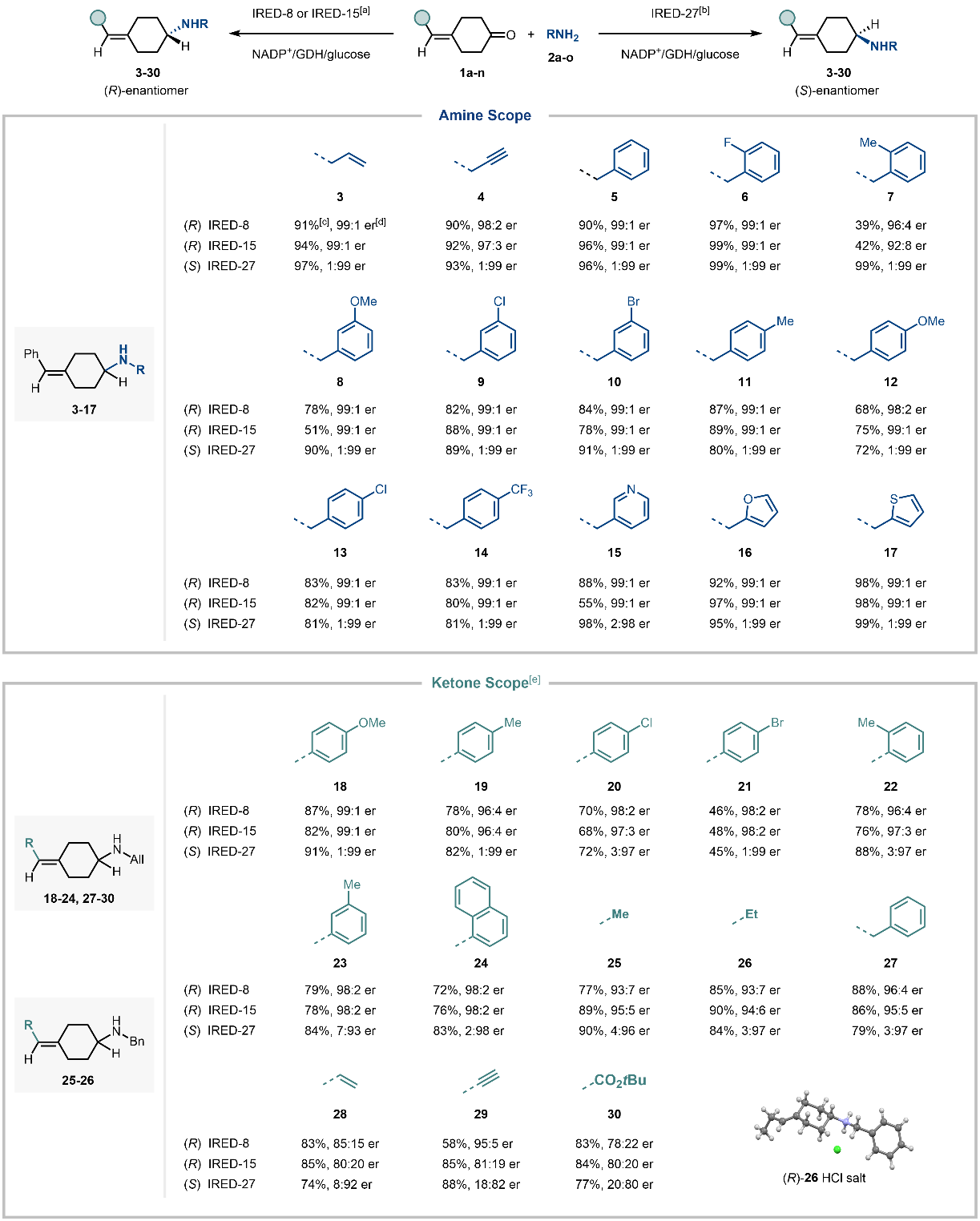
图3. 底物范围拓展。图片来源:Angew. Chem. Int. Ed
最后,作者通过蛋白晶体学研究与分子对接实验,揭示了IRED远程立体选择性的机理。基于晶体结构的对接结果显示,对于(R)-选择性的IRED-15而言,前手性亚胺底物31的苯基嵌入由M214、W210、M179、S235和V125形成的疏水口袋,烯丙基位于L176和M239之间的空腔,该结合模式使底物31以pro-R构象si-面接受辅酶NADPH的氢负转移,从而生成(R)-3。对于(S)-选择性的IRED-27而言,前手性亚胺中间体31的苯基则结合于W274、M233和P118构成的疏水口袋,烯丙基定向于F172和M116形成的空腔,底物以pro-S构象re-面接受氢负转移,生成(S)-3。简而言之,酶活性口袋对前手性亚胺中间体31反应构象的特异性结合是实现远程立体控制的关键因素。此外,定点突变实验发现D172N突变(IRED-15)和Y165F突变(IRED-27)均导致酶活显著丧失,表明D172(IRED-15)和Y165(IRED-27)在IREDs催化循环中作为关键质子供体的发挥重要作用。
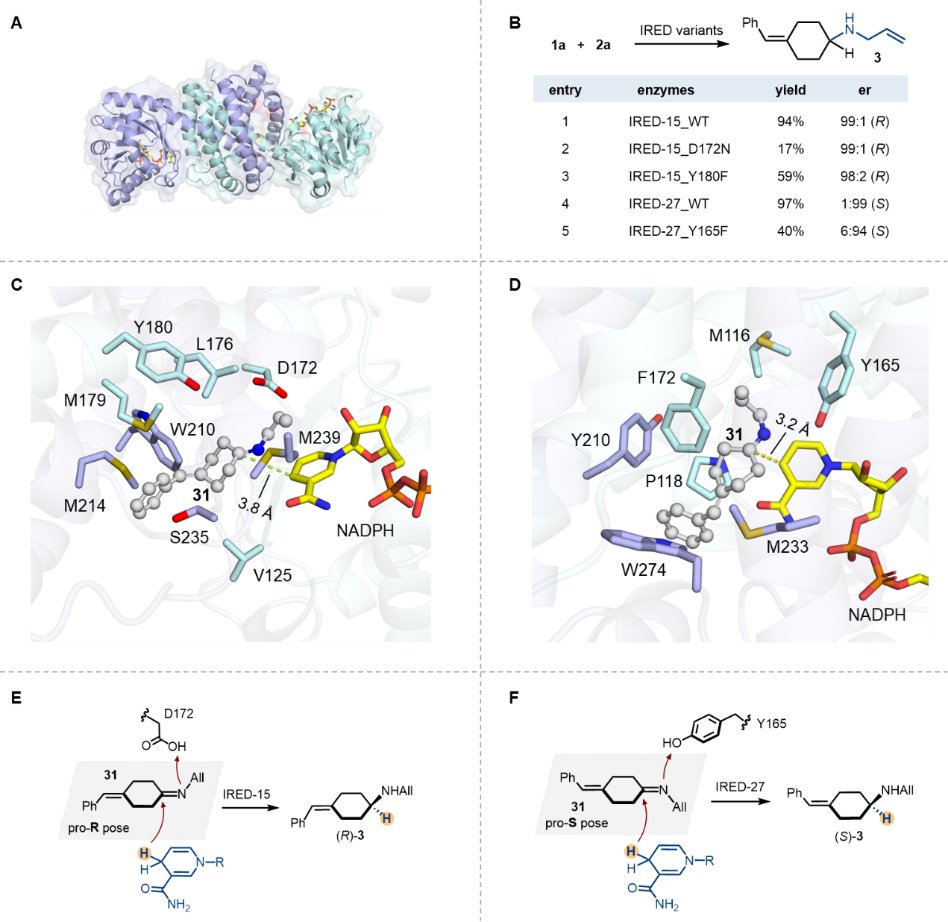
图4. 结构及机理解析。图片来源:Angew. Chem. Int. Ed
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn