

近年来,人工酶和光酶催化等策略的发展,不断突破生物合成的边界。另一方面,电化学合成作为化学合成领域快速发展的创新工具,具有廉价、电势可控和可持续等多重优势。当前电化学合成与酶催化的结合主要集中在以下两类(图1):通过电化学来实现酶的辅因子再生,继而实现酶的天然反应;电化学生成的中间体或底物参与后续酶催化天然转化中(电化学/酶级联)。然而,如何利用电化学驱动酶催化,去解锁非天然的新催化模式,仍待突破。
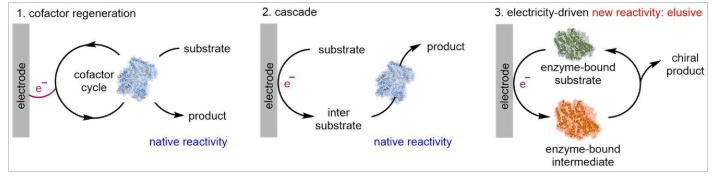
图1.电催化与酶催化结合现状
我校黄小强研究员,自2021年开展独立研究以来,通过酶学机制设计和蛋白定向进化改造策略,成功开发了几类新酶催化功能。在光酶催化领域,黄小强团队首创焦磷酸硫胺素(ThDP)依赖的自由基酰基转移酶(Nature 2024, 625, 74:南京大学黄小强/梁勇及合作者Nature:创制新光酶元件,引领光生物制造新方向;Nature 2025, 637, 1118:Nature!南京大学黄小强团队推动光酶领域到复杂多组分转化),突破了不对称生物合成的边界。在此基础上,团队在不对称电酶催化领域取得新突破:融合二茂铁甲醇介导的阳极氧化和ThDP依赖酶催化,解锁了电酶催化的动态动力学氧化新体系(图2)。团队开发的电酶协同催化策略,创新性地将2次单电子氧化机制引入酶中,结合定向进化技术优化蛋白的活性中心,最终成功赋予了ThDP依赖酶催化动态动力学氧化的新活性。该体系以清洁电能替代传统化学氧化剂,可在较低酶负载量下(0.05 mol%),实现布洛芬、萘普生等十种(S)-芳基丙酸类抗炎药物的高效合成,对映选择性高达99% ee,并兼容全细胞催化与规模化制备。
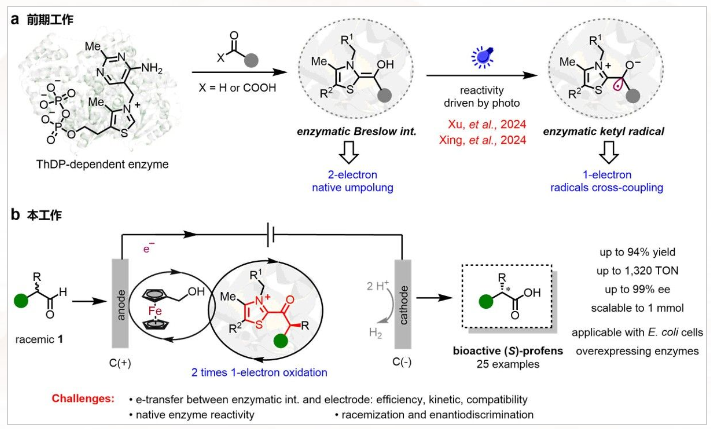
图2:新型电酶不对称催化体系的开发
研究团队选择以外消旋2-([1,1'-联苯]-4-基)丙醛为模板底物,含有ThDP和Mg2+的MOPS(pH = 6.5)为缓冲液,二茂铁甲醇(FcMeOH)为电介质,廉价易得的石墨电极为阴阳极,探索电酶的立体选择性氧化过程。在经过酶库筛选、电极筛选、电介质筛选等条件筛选之后确定了最佳反应条件(图3)。
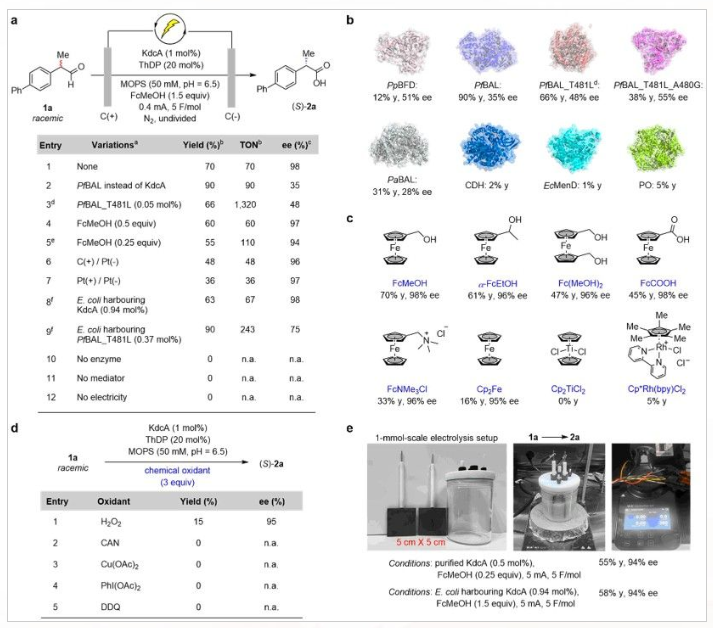
图3:条件筛选与规模化制备
该电酶催化体系展现出卓越的底物普适性与官能团兼容性(图4)。针对结构多样的外消旋α-支链醛类化合物,可实现精准的手性控制,高效转化为α-手性羧酸产物(最高99% ee)。文章展示了25个例子,实验成功制备了十种具有生物活性的(S)-丙酸类药物(2p-2y),包括氟比洛芬、布洛芬、萘普生等,产率良好至优异,对映选择性最高达99% ee。同时,该电酶催化方案可以以相同的效率和对映选择性放大到1 mmol级别。
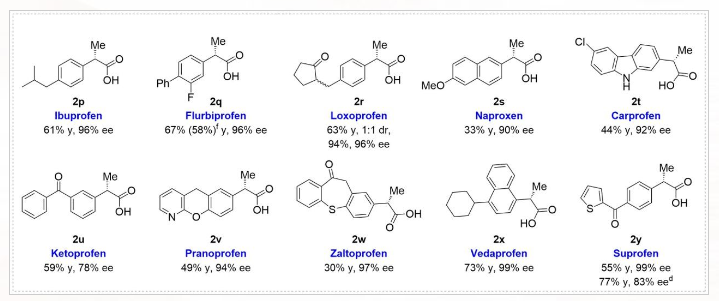
图4:代表性底物谱
研究团队运用湿实验、电子顺磁共振(EPR,中科大/强磁场中心于璐教授团队完成)及计算模拟等手段,阐明了电化学驱动下ThDP酶活性中心的催化机制及其立体选择性的来源。详细内容请参考原文。
该工作通讯单位为南京大学配位化学全国重点实验室、化学和生物医药创新研究院、化学化工学院、前沿交叉科学研究中心。南京大学化学化工学院2022级博士研究生赵贝贝和许园园为论文的共同第一作者;黄小强特聘研究员为通讯作者。该工作得到了南京大学启动经费、国家重点研发计划项目(2022YFA0913000)、国家自然科学基金(22225703, 22277053, 224B2705, 223B2703, 22437005)、中央高校基本科研业务费专项基金项目(0205/14380346)等项目的支持。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn