

(图片来源:Science)
正文
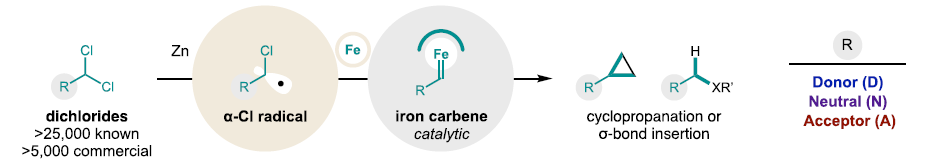
金属卡宾作为有机合成中极具价值的高活性中间体,其催化合成仍面临两大挑战:1)并非所有极性类型的卡宾都能通过催化途径获得;2)缺乏能制备全系列电子特性卡宾的通用前体。最近,美国俄亥俄州立大学David A. Nagib课题组突破性地开发了铁催化的反应策略,其可合成包含供电子(OMe、NR2、烷基)、吸电子(CN、CO2R)及电中性(H、BR2、SiR3、卤素、芳基/杂芳基)取代的卡宾。该策略通过α-氯自由基途径,实现了(2+1)环丙烷化和σ键插入反应的广谱卡宾偶联。这一温和、高效且电子特性可调的合成方法,不仅建立了基于动力学和热力学参数的金属卡宾分类新标准,还衍生出类似于点击化学的卡宾反应及其水相适配的反应体系,为化学生物学应用提供了新工具(Fig. 1)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
(图片来源:Science)
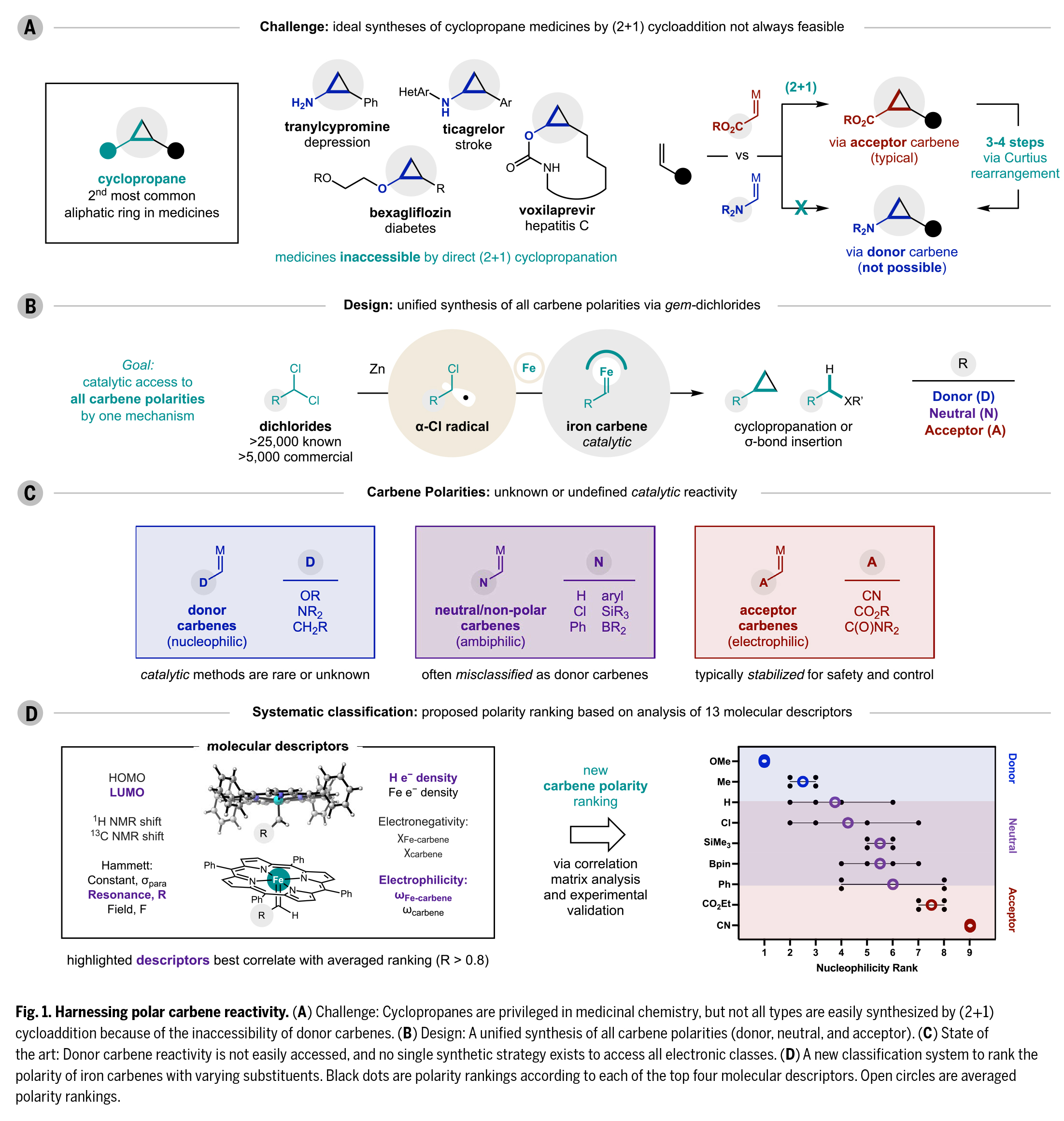
首先,作者成功开发了一种基于商业可得的偕二氯化合物与烯烃的(2+1)环丙烷化反应(FeTPPCl为预催化剂,Zn为还原剂,LiI为自由基介导物)(Fig. 2A)。该策略适用于多种极性卡宾,包括供电子卡宾(R = OMe或NR2,1-3,65-96%)、烷基卡宾(4,93%)、CH2Cl2/CD2Cl2前体产生的卡宾(R = H/D,5-6,99%)以及偕二烷基卡宾(7,41%)。特别值得注意的是,中性铁卡宾可通过卤仿(8-10,70-82%)、硅基/硼基二氯化合物(11-12,70-90%)等前体制备,且所得的连有卤素、硼酸酯等官能团的环丙烷产物可进一步官能团化。此外,芳基卡宾(13-16,75-93%)和连有吸电子基团修饰的卡宾(酯基17,85%、氰基18,99%)也表现优异。
此外,该反应对烯烃底物同样展现出广谱适用性(Fig. 2B)。其中,1,1-二取代脂肪族烯烃与苯乙烯类似物可高效反应,环外烯烃可构建含氮杂环丁烷、环丁烷等药用常见结构的螺环产物(19-20,95%)。烯酰胺(21,60%)、乙烯基邻苯二甲酰亚胺(22,81%)和烯醇醚(23,70%)等杂原子烯烃也可顺利转化,立体选择性优异(dr > 10:1)。以硼酸酯修饰的环丙烷24为例,其可通过氧化、格氏加成、交叉偶联等反应衍生为醇25(73%)、烯烃26(56%)和芳烃27(98%),且完全保持立体构型。
值得注意的是,该反应在酮、酯、醇、硫醚等添加剂存在下仍能保持> 50%的产率(35),展现出优异的官能团兼容性(Fig. 2C)。三级胺可完全兼容,而伯/仲胺、酰胺和醛类则会发生副反应。这一模块化策略为复杂分子中环丙烷结构的构建提供了高效途径。
(图片来源:Science)
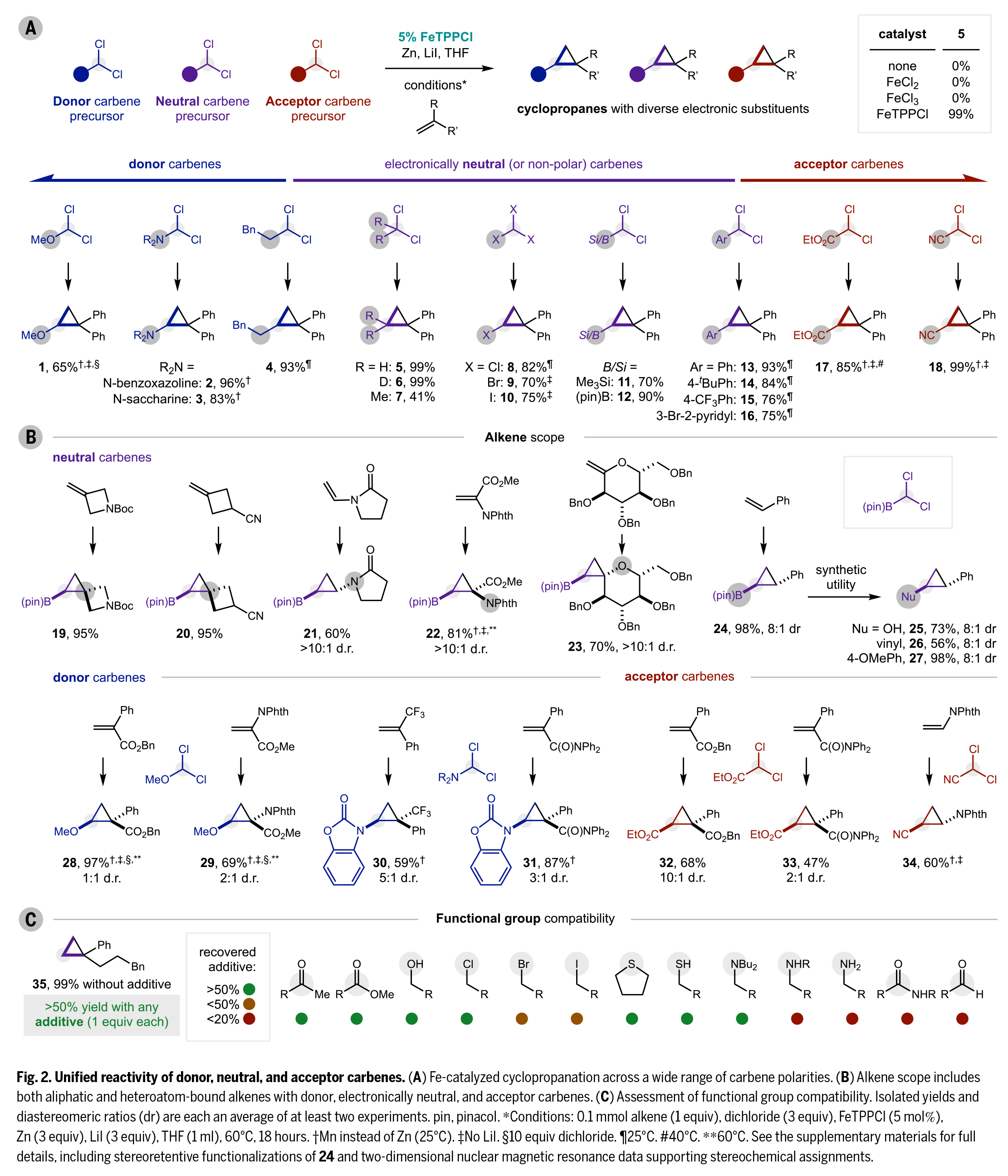
接下来,作者通过三种策略系统研究了卡宾极性对反应活性的影响机制(Fig. 3)。首先,针对九类代表性R基团,分别选用两种缺电子受体捕获剂(丙烯酰胺和三氟甲基烯烃,Fig. 3A红色)和两种富电子供体捕获剂(硫醇和硅烷,Fig. 3A蓝色)进行平行实验。标准条件下16小时的实验数据显示(Fig. 3B):供体卡宾与受体捕获剂反应活性最高(产率显著高于中性/受体卡宾),而受体卡宾则与供体捕获剂反应更优(Fig. 3C),中性卡宾介于两者之间。动力学研究表明(Fig. 3D-E),供体(烷基)卡宾与受体捕获剂的反应初速度是受体(氰基)卡宾的5倍;而受体(酯基)卡宾与供体捕获剂的反应速度则比供体卡宾快10倍以上,这解释了受体卡宾在σ键插入反应中的优势。
作者进一步通过四组Hammett研究定量表征卡宾极性(Fig. 3F):以对位取代苯乙烯为底物,测得供体(OMe)、中性(H)和受体(CN)卡宾的反应常数ρ分别为+1±0.2、-0.3±0.1和-2±0.5,准确反映了其电子特性。值得注意的是,芳基卡宾(Ph)实际表现为中性电性(ρ = -0.4±0.1),比CH2卡宾更具亲电性,这与以往"供体卡宾"的认知不同。
(图片来源:Science)
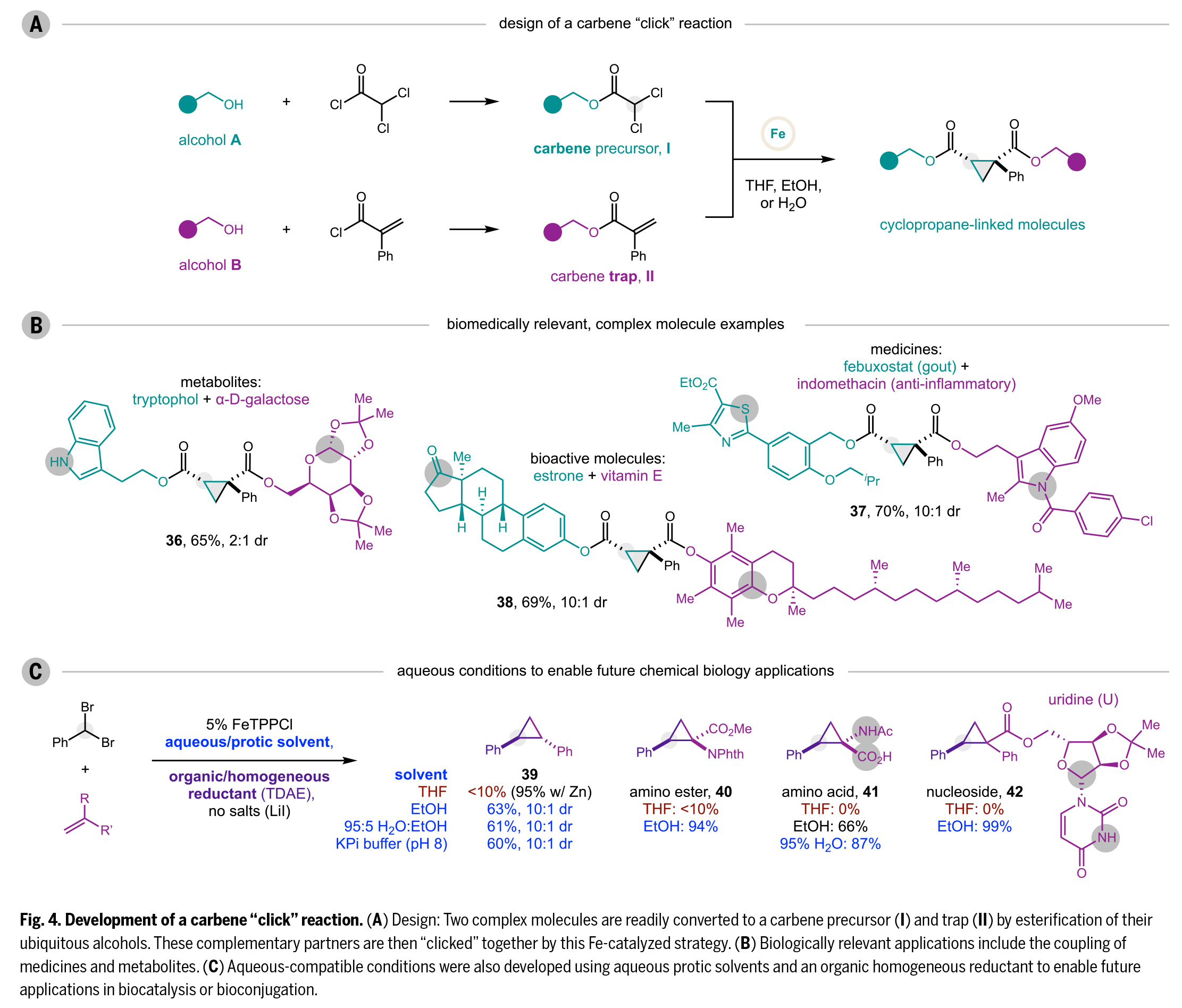
基于该方法的简便性,作者开发了一种类点击化学的卡宾偶联反应(Fig. 4A),其高效性、选择性和实用性可媲美(3+2)Huisgen环加成反应。与炔-叠氮环加成产生的三唑环相比,(2+1)环丙烷化能构建更小、更强且具有独特空间取向的全碳环,这些特性使其在药物设计中备受青睐。该策略的创新之处在于:通过简单的酰化将生物分子中的羟基转化为互补反应模块。醇A经α,α-二氯酰氯修饰形成卡宾前体I,醇B经α-苯基丙烯酰氯修饰形成卡宾捕获剂II。如Fig. 4B所示,该方法成功实现了多种生物分子的高效偶联,包括代谢物(色氨醇与α-D-半乳糖,36,65%)、药物(非布索坦与吲哚美辛,37,70%)和生物活性分子(雌酮与维生素E,38,69%)。其中灰色圆圈标示了传统生物偶联技术难以兼容的官能团,为重氮环丙烷方法提供了新的选择。
针对水相体系的应用需求(如生物催化、生物偶联或DNA编码库合成),作者进一步优化了反应条件(Fig. 4C):(1)以有机还原剂TDAE(四(二甲氨基)乙烯)替代无机还原剂(Zn/Mn);(2)去除LiI盐;(3)采用活性更高的偕二溴化物。该体系在乙醇中的反应效率优于THF,且适用于含5%乙醇的缓冲水溶液(95:5 H2O:EtOH,KPi缓冲液pH 8)。除苯基卡宾与苯乙烯的模板反应(39)外,氨基酯40(94%)、氨基酸41(87%)和核苷42(99%)等质子性生物分子在质子溶剂中也表现出更佳的环丙烷化效率,这可能归因于其溶解度的改善。
(图片来源:Science)
总结
David A. Nagib课题组开发了一种基于商业可得试剂的通用催化策略,可通过统一机制调控各类卡宾极性。首次实现了全极性卡宾的催化统一合成,解决了供体卡宾难以直接生成的难题。通过实验与计算结合,建立了卡宾极性的定量分类标准。为药物设计(尤其是含环丙烷结构)提供了高效工具,将推动生物偶联与材料化学发展。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn