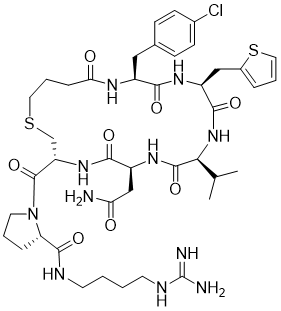
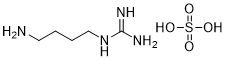
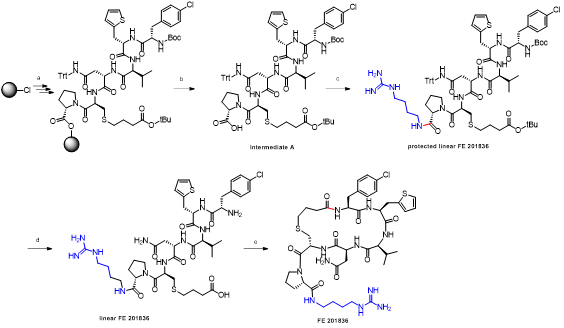
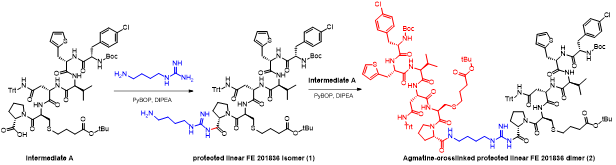
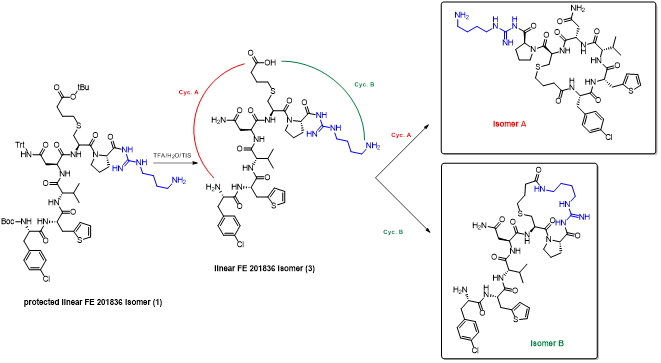
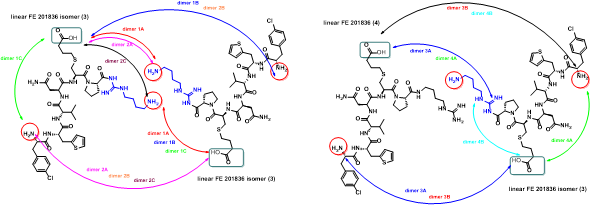
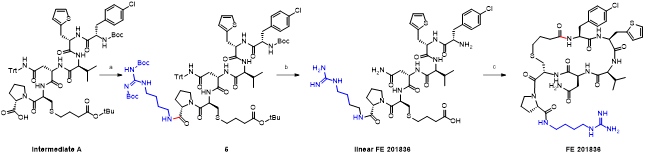
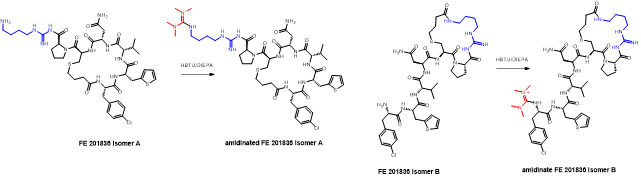胍丁胺又名1-(4-氨基丁基)胍,是一种精氨酸经精氨酸脱羧酶 (ADC)脱羧作用而衍生的化合物。它具有广泛的治疗应用,包括糖尿病、神经外伤和神经退行性疾病,阿片类药物成瘾,情绪障碍,认知疾病和癌症。胍丁胺结构也存在于多种天然化合物,如 E-642 或以及像 blenoxane 的多肽类药物,并经常用作精氨酸在肽 C 末端替代以探索受体-配体作用。氨基的amidination是最常见的一种合成胍化合物的方法。碳二亚胺、O-甲基异脲、硫脲、异硫脲、 氨基(亚氨基)甲磺酸、氯甲脒、1H-吡唑-1-甲脒,N-三氟甲脒,和氰胺 传统上被用于将胺转化为相应的受保护或未受保护的胍化合物。尽管在合成方面取得了某些应用,在工业中大量生产胍丁胺多肽药物仍然受到传统工艺的限制。因为相应的amidination条件通常要求金属基催化剂、加热、氧化剂或长反应时间。此外,多肽中亲核官能团的存在,可能进一步限制amidination策略的应用。去氨加压素的类似物多肽FE 201836, 一种作为血管加压素-2受体激动剂和针对夜尿症的环状硫醚肽,在其多肽的 C 端带有胍丁胺残基(Scheme 1)。FE 201836 有一个 Thi (噻吩基丙氨酸)残基和硫醚结构,它们都对亲电试剂高度敏感,可以发生例如氧化和碘化的副反应。目标胍丁胺部分可以通过1,4-丁二胺前体上氨基的amidination反应实现,但这个过程可能会对Thi和硫醚产生副反应。鉴于这些限制,一个使用温和的合成策略引入胍丁胺成为重点内容。胍丁胺硫酸盐(Scheme 2) 是一种市售化合物,对很多疾病具有广泛的治疗潜力。它也经常被用作营养补充剂。这种原料可能被用作胍丁胺替代品制备 FE 201836 肽。在 FE 201836 合成过程中,前体线性肽中间体 A 首先在 CTC 树脂上进行固相合成, 然后被 10% (v/v) HFIP(六氟异丙醇)/DCM(二氯甲烷)切割,并在MTBE (甲基叔丁基醚)中沉淀分离。胍丁胺硫酸盐在随后的步骤中与中间体 A 缩合,制备侧链保护的线性 FE 201836。然而,胍丁胺硫酸盐难溶于普通有机溶剂,不能直接与浓度合适的多肽溶液偶联。因此,胍丁胺硫酸盐首先在水溶液中用 2 equiv NaOH 中和,然后冻干分离;通过如此手段获得的free base 胍丁胺硫酸盐溶解在 DMF 中(1.92当量),与 1当量的多肽中间体 A ,在1.05 当量 PyBOP和 2.5当量的 DIPEA(二异丙基乙胺)存在下进行液相缩合反应,组装侧链保护的线性 FE 201836。后者受到TFA(三氟乙酸)/TIS(三异丙基硅烷)/H2O的脱保护处理得到线性 FE 201836。在随后的酰胺环化反应中,线性 FE 201836多肽的羧酸与氨基在1.3 equiv HBTU 作用下对接,并合成目标FE 201836多肽。FE 201836的流程合成Scheme 3 所示。Scheme 3. Free base 胍丁胺介导的FE 201836合成路线 (a: 固相多肽合成; b: 10% HFIP/DCM; c: freebase agmatine/PyBOP/DIPEA/DMF; d: TFA/TIS/H2O; e: HBTU/DIEPA/DMF)Free base胍丁胺的偶联反应在室温下2小时内完成。侧链保护线性 FE201836中间 产品经 RP-HPLC 分析,检测到两个丰度为 9.5 和 10.9% 的杂质。LC/MS 分析显示它们可能是异构体 1,以及通过胍丁胺交联的侧链保护线性 FE 201836 二聚体 2。随后,该侧链保护的线性 FE 201836 中间品粗产物用浓缩的 TFA 溶液以去除保护基团。同时产生的线性 FE 201836 位置异构体杂质 3 和胍丁胺交联的线性 FE 201836 二聚体,其化学结构的认证得到NMR数据的支持。该位置异构杂质和二聚杂质产生的根本原因在于多肽中间体 A 的羧基与胍丁胺胍基之间的反应。一般认为,胍基的亲核性在酸性到弱碱性的情况下基本上受到抑制。胍基的亲核性在普遍有机反应的pH 条件下通过质子化显著减弱。然而,胍化合物被视为超级有机碱并具有明显的亲核性,这种性质可以赋予它们亲核催化剂的作用。在本课题反应中,胍丁胺中的胍基在与肽分子偶联之前被中和,其亲核性被唤醒。去质子化的胍基因此与其4-氨基形成竞争反应,与肽分子上羧基反应而形成位置异构体杂质 1。这个过程原则上类似于在 Fmoc-Arg-OH在其羧基活化过程中的内酰胺副反应。位置异构杂质 1上有一个未配对的氨基,可以在反应中与另一个多肽中间体 A 肽分子作用,产生胍丁胺交联的二聚体杂质 2 (Scheme 4)。Scheme 4. Free base 胍丁胺介导的位置异构体以及二聚体杂质的形成过程。线性 FE 201836 位置异构体杂质的命运研究 (Fate Study)值得注意的是,侧链保护的线性 FE 201836 位置异构体 1 会干扰后续环化反应。在经过TFA处理后,所得线性 FE 201836 位置异构体 3 带有一个羧基和两个氨基,理论上可以引发两种位置异构杂质(异构体A和B)(Scheme 5)。此外,线性 FE 201836 位置异构体 3 也可以在环化步骤中与另一个分子 3 或普通线性 FE 201836分子4作用,分别产生六种或四种二聚杂质 (Scheme 6)。Scheme 5. 由侧链保护的线性FE 201836位置异构体杂质1 所引发的FE 201836 异构体 A/B 的形成。Scheme 6. 两分子线性FE 201836位置异构体杂质3形成的二聚体杂质,以及一分子线性FE 201836位置异构体杂质3与一分子线性FE 201836形成的二聚体杂质。探寻从中间体里检测到的异构杂质的命运总是很有必要的,包括它们在随后的合成步骤中的转化,最终异构体杂质的化学结构,这些异构体杂质在产品中的可检测性和去除率。为此,通过色谱纯化分离得到线性FE 201836位置异构体杂质3,并作为反应物进行接下来的环化。通过LC/MS分析产物,异构体 A 和异构体B被检测出,其丰度为60.8% 和5.1%(对应性并不确定)。FE 201836 异构体 A 和 B 均有一个未配对的氨基,它们可能在环化反应中与过量的 HBTU 反应,转化为相应的胍对应物(Scheme 7)。如此得到的amidinated异构体 A 和 B 均已在粗品中检测到,其中之一的含量高达 23.0%。此外,在反应混合物中检测到二聚体,这应该归因于由线性 FE 201836 异构体所诱导六种可能的异构二聚体之一(Scheme 6)。因为这六个二聚体杂质中的每一个都有一个未配对的氨基,它们仍然容易受到HBTU的amidination的影响。事实上,在粗产物中已经检测到2 个amidinated的异构二聚体。Scheme 7. FE 201836异构体A/B的amidination产物。综合以上实验和分析可以得出的结论是,线性 FE 201836 位置异构体可以进行多种反应,包括环化、二聚化和amidination。两个线性 FE 201836 位置异构体杂质之间的二聚化实际上是有利于目标肽的合成,因为两个位置异构体杂质被消耗以形成另一种二聚体杂质,该二聚体杂质可以通过色谱纯化从产品中轻松去除。然而,线性 FE 201836位置异构体也可以与线性FE 201836分子二聚化而形成混合二聚体,如Scheme 6 所示。此类副反应消耗线性 FE 201836 分子并降低反应收率。命运研究得出的最突出结论是,由线性 FE 201836 位置异构体杂质所导致的FE 201836 异构体A/B,以及二聚杂质,一旦形成,可以采用反相高效液相色谱法检测到,其检测方法具有高可检测性并明确区别于目标产品 FE 201836。因此,从FMEA 的视角(Failure Mode Effect Analysis),产品质量的完整性将通过如此高的可检测性得以保障,因为它们的去除可以明确地遵循和评估。通过 Bis-Boc-胍丁胺合成FE 201836鉴于由free base胍丁胺所引发的位置异构体杂质,以及该工艺的低收率和低粗品低纯度(71.0%),应该在FE 201836 合成中使用合适的胍丁胺替代品。胍基上的 Boc 保护基团可以显着提高提高母体胍丁胺分子在有机物溶剂中的溶解度,因此可以避免不必要的胍基中和步骤。实际上,Fmoc-Arg(Boc)2-OH 已经广泛用作肽合成。同样,Bis-Boc-胍丁胺也被认为是FE 201836合成中一种潜在可行的构建块,以绕过胍丁胺硫酸盐中和的步骤,并彻底避免各种位置异构体和相关二聚杂质的形成。Bis-Boc-胍丁胺定向合成FE 201836的过程如Scheme 8 所示。Scheme 8. Bis-Boc-Agmatine 引导的 FE 201836 合成路线 (a: Bis-Boc-agmatine/PyBOP/DIPEA/DMF; b: TFA/TIS/H2O; c: HBTU/DIEPA/DMF).事实证明,1.05 equiv bis-Boc-agmatine, 1.05 equiv PyBOP 和 2.5 equiv DIPEA足以使缩合反应在室温条件下 30 分钟内完成。在这个过程中没有异构体或二聚体杂质产生。得到纯度为 92.8% 的中间体 5,未校正的收率为 96.7%。使用由 60 equiv TFA, 1.5 equiv TIS 和 6 equiv H2O溶液对 多肽5 进行脱保护,得到纯度为 91.0%线性 FE 201836 中间体,其未校正收率为100%。所得的线性 FE 201836通过“伪高稀释策略“环化反应获得最终产品 FE 201836,粗品纯度为 87.8%,在这个过程中产生的常规二聚杂质小于含量 1.5%。粗品通过 LC/MS进行分析,不含环状异构体、amidinated二聚体、胍丁胺交联二聚体、和二聚体异构体。粗品纯度从 70.9%(free base 胍丁胺工艺)显著提高到 87.8%(Bis-Boc-胍丁胺),并且下游纯化工艺的复杂性明显减轻。Bis-Boc-胍丁胺代替free base胍丁胺因此全局显著优化了整体生产工艺。
在本研究阐述了胍丁胺中胍基所引发的副反应。来自free base胍丁胺的去质子化胍基与其4-氨基产生竞争反应,产生位置异构杂质。该位置异构杂质上的未配对氨基可以参加合成路线上的下游反应并形成多种杂质。Bis-Boc-胍丁胺,可以很容易地制备并应用于胍丁胺肽的合成。在这个过程种没有引发异构杂质和相关二聚体杂质。胍基官能团上的双 Boc 保护基团可以很容易地被 TFA 定量去除。使用Bis- Boc-胍丁胺原料合成FE 201836可以显着提高产品纯度和产率。这项研究还强调了中间产品异构杂质的研究方法,这种理念和策略对于确保API 产品质量的完整性至关重要。
文献详情:
Yi Yang* and Lena Hansen. Regioisomer Formation with Agmatine Guanidino Group, Its Implications for Agmatine Peptide Cyclization, and Application of Bis-Boc-Agmatine. Organic Process Research & Development. 2022. https://doi.org/10.1021/acs.oprd.2c00098